
iff
-
Постов
198 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные iff
-
-
а вот што ещё придумал:
1)Производим электролиз с свинцовым анодом в р-ре соды.
2)Выпавший осадок основного карбоната свинца фильтруем, промываем (наверно, его уже можно использовать кака индикатор сераводорода)
3)растворяем карбонат свинца в уксусе или любой другой кислоте (для получения других солей, кроме селиката)
4)Фильтруем р-р
5)кристаллизуем
Ну как? И не какой перекиси , и никакого избытка уксусной кислоты
-
СО2 лучше получать из соды и уксуса=) При электролизе того, что останется после реакции уксуса и соды, получится метан.
Странно, я читал, что получится смесь этана и метана
Мыло - это в роде стеорат натрия. Наверно должна выделяться стеориновая кислота(на аноде) (она нерастворима), но ведь будет получаться ещё и гидроксид натрия (на катоде). он прореагирует со стеариновой кислотой и ничего не получится. Объясните, какие же реакции идут?
-
-
А какое уровнение реакции?
Так чтоли: H2O2 + 2 H(+) = 2 H2O



-
ток не обязателен
Да. Свинец и сам по-себе растворяется в уксусе. Но я подумал, что ток ускорит этот процесс (совмесно с перекисью водорода)
-
Вполне могут и в осадок выпасть
Осадка нет.
А при кристаллизации? При выпаревании уксусная к-та испарится и ее избытка не будет.
-
1. Я провёл реакцию уксусной к-ты и основного карбоната меди(2). Выпарил раствор. Я получил моногидрат ацетата меди или гидроксоацетат меди?
2.В р-р, про приготовление которого, было сказано выше, положил железные гвозди, р-р стал не сине-зелёным, а светло-зелёным. Думаю, это ацетат железа(2). Но постояв в пузырёчке продолжительное время, он приобрёл бурый цвет (но осадка нет). Вероятно, это он прориогировал с кислородом воздуха и с избытком уксусной кислоты (судя по запаху, там был излишек уксусной кислоты). Пологаю, продуктами реакции являются вода и ацетат железа(3). Это так?
3. При нагревании ацетат кальция расподается на ацетон и мел. А как обстоит дело с ацетатами натрия, меди(2), железа(2) и железа(3)?
-
А зачем дальше проводить дискуссию?
Лично я, предложил способ, что-бы узнать правелен ли он. Оказалось нет. Что-то я не подумал о том, что серная кислота диссоциируют на ионы, (содержит сульфат-ион)
-
видимо, уровнение реакции очень-очень сложное...
:mellow:
-
почитайте Чувырина
Читал, там написано, что для получения хлор пропускают через тёплый р-р нитрата или хлорида аммония, и в итоге, там получаются капли маслянистой жидкости. Но меня интересуют уровнения реакций.
NH4NO3 + Cl2 = ...
-
-
Это не нормально в плане такое смешивать - реагирует бурно
Взорвётся что-ли? Этож не так плохо.
А почему с серебрянкой не выйдет? Там много примесей, но вот смотрите, говорят:
25 граммов дихромата калия и 10 граммов серебрянки ( алюминиевой пудры) -
я приготовил смесь: 2г меди оксида и чуть меньше 0,5г серебрянки, но смесь имеет нечёрный цвет, а тёмно-серебрянный. Это нормально?
-
А другая соль появиться. Нужно, что-бы все продукты реакции были не растворимы. Наверно можно добавить, р-ры гидроксида бария или кальция
-
а электролизом получить можно (прошлый мой пост)?
-
возьмите ёмкость, в неё опустите 2 электрода. Один из них должен быть графитовый. на нём будет выделяться хлор. Этот электрод подключите положительнопу полюсу источника тока. В роли второга электрода может действовать стальная, медная или др. пластина. Можно так же использовать графит. Этот электрод нужно подключить к отриц. полюсу (это катод). Около него будет выделяться щёлочь.
Почему же? Вроде так можно... Вот например, если нет KCl, но есть K2SO4. реакция такова:
2NaClO3 + K2SO4 = 2KClO3 + Na2SO4
Но электролит вероятно следует прокипятить, так как там может быть гипохлорит натрия (помимо хлората)
-
ну как получилось?
-
1. я считаю, что там такая реакция:
H2O = H(+) + OH(-)
Fe - 2e(-) = Fe(2+) - анод
2H(+) + 2e(-) = H2 - катод
2OH(-) + Fe(2+) = Fe(OH)2
4Fe(OH)2 (суспензия) + O2 (воздух) = 4FeO(OH)↓ + 2H2O
-----------------------------------------------------------------------
6H2O + 4Fe + O2 (воздух)= 4H2 + 4FeO(OH)↓
но можно представить по-другому:
H2O = H(+) + OH(-)
NaCl = Na(+) + Cl(-)
Fe - 2e(-) = Fe(2+) - анод
2H(+) + 2e(-) = H2 - катод
Fe(2+) + 2Cl(-) = FeCl2
Na(+) + OH(-) = NaOH
---------------------------
2H2O + 2NaCl + Fe = H2 + 2NaOH + FeCl2
но NaOH и FeCl2 тутже реагируют и получается тоже самое:
2NaOH + FeCl2 = Fe(OH)2 + 2NaCl
подставляем в уравнение нашей реакции:
2H2O + 2NaCl + Fe = H2 + Fe(OH)2 + 2NaCl
получаем
2H2O + Fe = H2 + Fe(OH)2
затем, гидроксид окисляется.
Т.е. всё тоже самое
2.В статье говорится
И добалвяется:Смешайте 50 г кальцинированной соды и 100 г железного купороса вместе. Смешать надо особо тщательно.+ Внимание! Сода каустическая и сода пищевая вам не подойдут.Но почему? кальцинированная сода - это карбонат натрия, реагирую с сульфатом железа получается карбонат железа и сульфат натрия. Карбонат железа гидролизуется до гидроксида и углекислоты.
Ладно, пищевую нульзя, но а почему нельзя каустическую использовать? Ведь это гидроксид натрия, с ним реакция ещё проще...
-
Вот она: http://pirotek.info/Fire/termit.htm
Вопросы:
1. ДЛя получения гидроксида железа советуют:
Теперь воткните оба провода с выхода выпрямителя в банку с соленой водой (я считаю, что выпрямитель подключен к сети) и оставьте их там на несколько минут. Вскоре один из контактов, погруженный в воду, начнет пузырить сильнее чем другой. Это ПОЛОЖИТЕЛЬНЫЙ(+) провод. Если Вы не сделаете этого теста, то конечный продукт будет противоположен (химически) ржавчине, и будет являться РЖАВОЙ КИСЛОТОЙ. Вам это ненужно (хотя ржавая кислота тоже полезная вещь!).Странно, на аноде вроде-бы в этом случае ничего не выделяется, а он сам переходит в раствор. И вообще, что это за "тест", для чего он нужен? Просто что-бы определить полярность блока питания?
2. Допустим, я перепутал анод и катод, но так как оба электрода одинаковы:
воткните оба провода с выхода выпрямителя в банку с соленой водойПо этому что изменит полярность подключения? И что это "ржавая кислота"?
-
Спасибо за ответы

-
а у меня такой вопрос:
можно ли получить ацетат свинца анодным растворением в уксусе? Думаю, что вначале электролизер будет выделять водород(на катоде), а свинец с анода будет уходить в раствор, но вероятно, когда концентрация ацетата свинца в электролите повысется, то на катоде, помимо водорода, будет выделяться свинец...
Может быть имеет смысл поставить мембрану около анода, что-бы образуемый, в прианодной облости, ацетат свинца меньше "попадал" на катод и реагировал там?
-
Вы хотите узнать как его получить?
1.Для этого нужно приливать уксус к мелу до прекращения выделения газа, полученную жидкость отфильтровать (от гипса, который добавляют в мел, и мусора, если мел из речки). Отфильтрованный раствор выпарить, возможно под тягой или вентиляцией из=за вероятности избытка уксуса
2. Всё тоже самое, но вместо мела побелка. Обычно в извести есть мел, по которому можно определить конец реакции (когда, прекращается выделение газа - реакция закончена).
Я пробовал эти оба способа. 2-ой по-моему лучше, вероятноо из-за более мелких частиц
-
Про мел. Покупалась бордосская смесь. Там 2 пакета, в одном сульфат меди(2), а вдругом известь(наверно). Но, на самом пакете написано: CuSO4 + CaO. (т.е. там негашеная известь. а на обороте этого пакета написано: "возьмите столько-то грамм гашеной извести и растворите..." Т.е. не понятно, там CaO или Ca(OH)2. Но эта известь реагирует с медным купоросом (выпадает осадок), стало быть это не мел
-
а какая температура требуется для этой реакции?
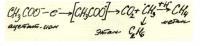
Нитрат ртути и Я
в Синтез соединений
Опубликовано
Хлористым железом платы травят.