-
Постов
92 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Весь контент Alisa-@
-

Чем смыть нитрат ртути 2 с кожи и насколько он опасен?
Alisa-@ опубликовал тема в Токсикологическая химия
Протекла банка с нитратом ртути, попал на палец. Я заметила не сразу. Промыла с мылом, затем кальцинированной содой, потом хлоридом натрия потерла. Еще посоветовали пероксидом водорода промыть. Насколько правильно всё это я не знаю. Как правильно смывать и насколько опасно проникновение в организм?- 22 ответа
-
- нитрат ртути 2
- нитрат ртути ii
- (и ещё 3 )
-
А если результаты спектрального анализа выражены в массовых долях, то как перейти к Abs/0.1 mm? Я впервые сталкиваюсь с этой темой
-
Что означает концентрация Abs/0.1 mm? Подскажите литературу, где подробнее можно узнать
-
Неправильно выразилась. При добавлении хлорида натрия должна была измениться окраска индикатора от желтого в фиолетовую. Но этого не произошло. На титрование должно уйти около 10 мл нитрата ртути. Добавили избыток, окраска не изменилась. установление точной концентрации нитрата ртути по хлориду натрия. Прописано в ПНДФ на определение концентрации хлоридов в воде. ПНДФ сейчас не могу назвать
-
Приготовили раствор нитрата ртути. В методике написано, что раствор нитрата ртути должен быть мутным, но он прозрачный. С хлорид ом натрия в присутствии смешанного индикатора окраска должна измениться от желтого в фиолетовую. Реакции никакой нет. (Предварительно была добавлена азотная кислота до перехода из фиолетового в жёлтый) По методике используют нитрат ртути одноводный. В чем может быть проблема?
-
Правильно сделан расчёт? Объем титранта (трилона Б) = 4,3 мл Концентрация трилона Б = 0,009 Разбавление в 50 раз (2мл до 100) Результат = (2*0,009*4,3*1000*50)/100=38,7
-
Здравствуйте. Нужно осуществить внтрилабораторный контроль методом добавок для нитрит-ионов в природной сточной воде . Пндф 14.1:2:4.3-95. Метод фотометрический. Объем пробы 50 мл, но можно брать с разбавлением до 50 мл. Подскажите, каким образом вводить добавку. Прилагаю расчёт необходимого объёма Ампула содержит 1 мг нитрит ионов ионов. Разбавляем в 1000 раз. 1 мл содержит 0,001 мг нитрит ионов. V добавки =2 мл, т.е. 2 мл содержит 0,002 мг нитрит ионов. 50 мл-0,002 мг 1000 мл - х мг Х= 0,04 мг добавки. Не понятно, когда вводить добавку. Спасибо.
-
Это понятно. Неправильно задала вопрос. Используют ли гидроксид для получения оксида в промышленности? Может, по каким-то причинам этот способ не выгоден. Есть ли литература, описывающая этот способ ?
-
Нашла, что можно выделить церий из смеси других РЗМ. Церий легко окисляется кислородом в процессе сушки смеси гидроксидов РЗМ на воздухе при температуре 120-130 гр. Ц. Ce3+ окисляется до Ce4+. Гидроксиды лантаноидов растворяются в разбавленной азотной или соляной кислоте. А гидроксид церия остаётся в осадке. Можно ли из него получить оксид? И используют ли это в производстве?
-
Один из способов получение металлического церия - восстановление фторидов кальцием. Фториды получают в результате реакции оксидов редкоземельных элементов с HF при ≈ 700 градусов Цельсия. Как получить оксид церия? Можно ли получить его из монацита?
-
Глинка, стр 603,616 формулы также написаны. Ошибку в заряде я видела, вот верно [Zn (OH)4](2-)
-
Понятно!
-
Неорганическая химия в реакциях. Справочник. Р. А. Лидин, В. А. Молочко, Л. Л. Андреева., Дрофа, Москва, 2007 г. С 379 - 380
-
А как верно?
-
Правильно? Уравнения диссоциации полученных гидроксидов по типу кислот Na[Al (OH)4] ⇆ Na+ + H4AlO4- ⇆ Na+ + 4H+ + AlO45- Na2[Zn(OH)4] ⇆ 2 Na+ + H4ZnO42- ⇆ 2 Na+ + 4H+ + ZnO46- Уравнения диссоциации полученных гидроксидов по типу оснований Na[Al (OH)4] ⇆ Na+ + [Al (OH)4]- ⇆ Na+ + Al3+ + 4OH- Na2[Zn(OH)4] ⇆ 2 Na+ + [Zn (OH)4]- ⇆ 2 Na+ + Zn2+ + 4OH-
-
Как составить схему гальванического элемента в атмосферной среде, написать уравнения анодного и катодного процессов и токообразующей реакции. Указать продукт коррозии алюминия?
-
Почему-то в суммарной реакции никто не пишет 2 H+ K(-): 2H2O + 2e = H2↑+ 2OH- восстановление A(+): 2H2O - 4e = O2↑+ 4H+ окисление ------------------------------ 4H2O = 2H2↑ + O2↑ + 4H+ + 2OH- (4H+ + 2OH- = 2 H2O + 2 H+) 4H2O = 2H2↑ + O2↑ + 2 H2O + 2 H+ 2H2O = 2H2↑ + O2↑ + 2 H+
-
могли бы вы помочь в вопросе о скорости хим реакции? могли бы вы помочь в вопросе о скорости хим реакции?
-

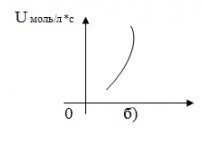
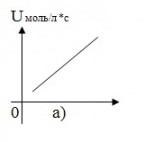
Сделать вывод о зависимости скорости реакции от концентрации
Alisa-@ опубликовал тема в Решение заданий
Сделать вывод о зависимости скорости реакции от концентрации; пояснить, какой линией выражается найденная зависимость; указать, проходит ли график через начало координат и объяснить почему. 1.зависимость линейная 2. ? 3. ? -
Я знаю, что в %