-
Постов
33306 -
Зарегистрирован
-
Победитель дней
1104
Тип контента
Профили
Форумы
События
Сообщения, опубликованные yatcheh
-
-
Fe=As-S-S-As=Fe (+2-1-1-1-1+2)
Валент-наци могут изобразить сетчатый полимер без двойных связей (которые, действительно, смотрятся стрёмно).
Никаких аномалий, довольные граждане расходятся по домам.
-
В 05.09.2024 в 22:39, St2Ra3nn8ik сказал:
Надо же!
Век живи - век учись, а дураком помрёшь...

-
В 05.09.2024 в 19:26, главный колбасист сказал:
А литий на натрий можно заменить? Почему именно литий,он дефицитный.
Ну тяжелее станет аккумулятор. И потенциал у лития выше,кажется.
Гореть будет веселее,наверное. Зато натрия навалом.Есть натрий-серные аккумуляторы, но у них рабочая температура 300С.
А литий заменить он не может. Ну - разная у них химия, тут хоть на пупе вертись. У всех лёгких элементов лица не общее выраженье.
-
В 05.09.2024 в 18:05, BritishPetroleum сказал:
А фосфор хлористый абсолютно бесцветный?
Как водка

-
 1
1
-
-
В 05.09.2024 в 15:37, XuMuK сказал:
Я думал он имел ввиду как раз литий в графите. 🙃
Именно об этом я и толковал. Литий в графите.
В 05.09.2024 в 02:27, XuMuK сказал:Вот так? 😆
Примерно.
Тут важны обстоятельства. Если кусок лития бросить в воду - он не загорится, будет бурно реагировать, но и только. Лучше всего бросать его на мокрую бумагу - тогда он вспыхивает, иногда - со стрельбой. С анодной массой дела хуже обстоят - она реагирует очень быстро, ибо интеркалят моментально разрушается, развивая поверхность контакта, в отличие от компактного лития, который плавится выше 150С, и реагирует только с ограниченной поверхности. Поэтому интеркалят способен взрываться, даже полностью всунутым в воду.
Короче - эффект тут зависит от количества воды, от того, в каком виде в воду попадает этот аккумулятор, какого он размера, насколько разряжен...
-
В 02.09.2024 в 19:49, BritishPetroleum сказал:
Ну это очевидно в случаях когда в среде нет сильного окислителя. А чем вам не нравится серная гадость?
Ну, это уже экзотика. Мы же говорим об карбоновых кислотах. А серная "радость" не нравится тем, что продукт требует выделения и очистки. С PCl3 - слил органический слой с сиропа, и даже перегонять не надо. Все три хлора в дело идут, газов не выделяется никаких, ничего прикапывать-перемешивать-греть-охлаждать не надо - смешал, подождал - профит!
-
В 02.09.2024 в 17:25, BritishPetroleum сказал:
Чего именно? Серы?
Лучше и пятихлористого, и тионила, и, тем более - прочей серной гадости.
-
В 30.08.2024 в 03:58, Алхумук сказал:
Разумеется, нельзя. Кристаллизатор не для нагревания, разве что совсем небольшого.
Лопаются на раз-два.
-
 1
1
-
-
PCl3 лучше во всех отношениях.
-
В 02.09.2024 в 09:23, Электрофил сказал:
Что-то такое и предполагал.
А вот этилендиамин думаю даст соль двухосновную.
Амины легче аммиака окисляются. Разве что с гуанидином соль получится.
-
В 26.08.2024 в 12:38, XuMuK сказал:
И про органику тут вот пишут. С такой цветовой температурой органика не горит. А вот литий горит.
В заряженном аккумуляторе замечательно горит анодная масса - интеркалят лития в графите. Горит не хуже металла, и при контакте с водой воспламеняется.
В разряженном аккумуляторе гореть нечему, кроме органического электролита, но у него весьма высокая температура вспышки, и к тому же это - раствор тетрафторбората (или гексафторфосфата) лития, что тоже не способствует горению.
-
 1
1
-
 1
1
-
-
В 18.08.2024 в 17:58, Wolfy36 сказал:
Неа
Не растворяется
Походу это сульфат свинца все таки, так как есть сульфат ион в нем
Но почему тогда он так активно горел с фосфором
Ну, так намешайте оксида свинца с фосфором - тоже хорошо гореть будет.
Перхлорат, как было отмечено выше, с фосфором должен взрываться, а не гореть.
Походу вас развели как курортника в винном погребке в Ялте

-
или в уксусной.
но в азотной надёжнее.
-
В 18.08.2024 в 10:48, Wolfy36 сказал:
Чудес не бывает. Если он не растворим в воде, значит это не перхлорат. Мохбыть - основной перхлорат, или какой-нить хлорид-перхлорат...
-
В 17.08.2024 в 23:40, BP2 сказал:
Нет ли тут ошибки?
Может и есть. Я не опирался ни на какие источники. Мне так ка-а-этся...

-
В 16.08.2024 в 22:14, Shizuma Eiku сказал:
А мне про влияние рН интересно было бы соображения почитать...
Какие тут рассуждения про pH? Всё просто до банального:
2Na2CO3 + H2O + Cl2 => 2NaHCO3 + NaCl + NaOCl
Поскольку вода исчерпана, далее идёт реакция хлора с гипохлоритом:
NaOCl + Cl2 => NaCl + Cl2O
В сумме
2Na2CO3 + H2O + 2Cl2 => 2NaHCO3 + 2NaCl + Cl2O
В вики не зря упомянут трубчатый реактор с перемешиванием, поскольку жидкой фазы нет.
При чём тут ваше бла-бла-бла про pH? pH чего?
-
В 17.08.2024 в 11:57, Alex Ferrum сказал:
В принципе, возможно. Правда, конфигурация получается невыгодная термодинамически, так что, полимер тут вряд ли получится, будет хелат вида

С гидроксилами в трансоидной конфигурации.
-
 1
1
-
-
В 16.08.2024 в 23:10, Grand1602 сказал:
Ещё вопрос, если применять безводный то большая разнится в весе порошока будет?
122/284 = 0.43
Т.е. безводного надо взять 46.7*0.43 = 20.1 г
-
В 16.08.2024 в 21:54, Shizuma Eiku сказал:
 это весь ответ на замечание, что при рН соды не существует хлорноватистой кислоты или ее ангидрида?
это весь ответ на замечание, что при рН соды не существует хлорноватистой кислоты или ее ангидрида?
Это весь ответ на всю вашу клоунаду.
Бро, успокойся, ты - великий химик, ты всегда прав, а если ты не прав - то смотри пункт первый.

-
В 16.08.2024 в 21:31, Shizuma Eiku сказал:
Не закись хлора производилась промышленно, а она была промежуточным продуктом в производстве гипохлоритов.
Потому что щелочная рН соды не позволит выделиться хлорноватистой кислоте.
Реакция хлора с содой работает не потому что в её ходе выделяется хлорноватистая кислота, а именно потому что в её ходе исчерпывается сода, а хлорноватистая кислота образуется уже из хлора и гипохлорита натрия и гидрокарбоната натрия. Т.е. ту-же реакцию можно провести и без соды.
Реально - клоун!
Бугагашеньки

-
В 16.08.2024 в 21:11, Shizuma Eiku сказал:
Там написано что закись хлора использовалась как промежуточный продукт при получении гипохлоритов и на этом её промышленное использование исчерпывалось.
Какая разница, длЯ чего она использовалась? Она производилась ПРОМЫШЛЕННО! Не надо передёргивать!
В 16.08.2024 в 21:11, Shizuma Eiku сказал:И в некоторых статьях так написано, но это неправда.
... потому что этого не может быть никогда!



Вся рота не в ногу, один унтер в ногу! Если вам что-то кажется - перекреститесь!
В 16.08.2024 в 21:11, Shizuma Eiku сказал:Это не работает т.к. рН соды слишком щелочная чтобы в её присутствии находились свободными кислоты.



Это работает. Не смотря на то, что это вам не нравится. Ну, вот - работает!

Вы с вашими потугами становитесь просто смешны! Ваше ЧСВ не просто зашкаливает - оно переходит всякие границы приличия.
Вы не даже шулер - вы клоун!




-
В 16.08.2024 в 16:26, Роман23 сказал:
Достаточно ли купить лабораторный шкаф в который будет установлен станок
Достаточно вытяжного короба над станком и вентилятор среднего давления на вытяжку. Полноценный шкаф влетит в копеечку, а оно вам надо?
-
 1
1
-
-
В 16.08.2024 в 20:11, Shizuma Eiku сказал:
Несколько лет закись хлора производилась в ограниченных промышленных масштабах
Поздравляю вас соврамши! Хоть и "ограниченные", но - "промышленные" масштабы.
В 16.08.2024 в 20:11, Shizuma Eiku сказал:рН карбоната натрия 11-12 - очевидно что в этих условиях не может существовать ни хлорноватистая кислота, ни ее ангидрид.
Химическая энциклопедия вас устроит как источник?
"Получают Сl2О пропусканием С12, разбавленного N2, над HgO или р-цией С12 с влажным Na2CO3."
В 16.08.2024 в 20:11, Shizuma Eiku сказал:Конкретный пример пожалуйста, а не просто оскорбления в мою сторону.
Я уже дал конкретный пример - закись хлора получают реакцией хлора с содой. Вы ляпнули, что это не работает, и теперь ужом вьётесь, лишь бы не признать свой ляп.
Типичные ужимки шулера

-
В 16.08.2024 в 14:51, Анна Андреевна сказал:
Всем здравствуйте. Если хранить этиленоксид 3 года, с ним произойдут какие-либо изменения? У него ухудшится качество?
В чём "хранить"? В заводском баллоне? За три года с ним ничего не будет. А в другой посуде его и не хранят. Нет, можно, конечно, некоторое время хранить его в дьюаре, но это же не три года.
Бывает, автоклавы используют для этой цели (в том числе - самопальные), но опять же - это для оперативных нужд. Нацедили, в цех отнесли, за неделю использовали.


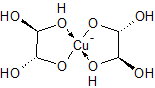
как правильно читать книги
в Книги
Опубликовано
Я знал чувака, который учебники переписывал. Прям - брал, и строчил дословно. Метода такая у него была.