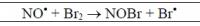komisar_rus
Пользователи-
Постов
18 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Весь контент komisar_rus
-
первая задача: ГЭ состоит из двух стандартных электродов.напишите токообразующие реакции и уравнения электродных процессов, по значению станд потенциалов определить изменение энергии гиббса. Дано Ni2+\Ni Au3+\Au мое решение и вопросы: на аноде - Au-3e=Au3-; на катоде Ni2++2e=Ni; итого: 2Au+3Ni2+=2Au3++3Ni верно? а теперь вопрос dG=-nFE 1)как узнать n? Е=ф_анода-ф_катода или наоборот? Вторая задача: уравнения электродных процессов и суммарной реакции электролиза водного р-ра в-ва. Узнать акие в-ва и сколько выделятся на электродах на даное время, силу тока и т.п. Дано AlCl3, t,I. Вопрос: Как узнать уравнения электродных процессов и суммарную реакцию? Вторую часть я как понял надо делать через Закон Фарадея, но и там проблемы с определением n. UPD В первой задаче ошибка там катод это золото, а анод это никель, но вопрос с n открыт.
-
Ну в курсе три части: ФХ, электрохимия, коррозия. За лит-ру спасибо.
-
МГТУ им. Баумана. Что характерно, первую часть химии этого семестра (кинетика, термодинамика, равновесие) я понимал без особых проблем, а вот с электролитами какие-то проблемы. Может посоветуете литературу? Наш учебник сложноват.
-
Ладно, спасибо за помощь конечно. Просто у меня даже на лекциях не было автопротолиза и не предвидеться, я так понял, что избыток это то, что более чем достаточно для реакции, верно? То есть если на реакцию надо 1 моль, а из концентрации выводим, что присутствуют 2 моль, то 1 моль это избыток. И что он дает заданиях с определением пш? Не понимаю...
-
Но все же, если бы была реакция типа 2A+B=C+h2o то мы бы искали концентрацию в-ва С и из не выражали бы кислотность?
-
Ca(OH)2, коненчо, с купрумом опечатка вышла.
-
ну в этом ошибся, но все же, мое обоснование верно по поводу полного превращения? Просто у меня это одна задача из многих вариантов, а там объемы и концентрации равны. у всех pH 7 что ли...
-
Почему же? Как обосновать?раз их по 0.02 моля, то они полностью превращаются и получается, что Cu(OH)2 выходит из системы как осадок, а вода не диссоциирует?
-
Их обоих по 0.02 моля(n=CV), непонятно что в избытке. Вот я что понял: найдем то, что осталось в избытке, тогда найдем его концентрацию (моль делить на 10 литров), подобрать из таблицы константу диссоциации и найти из уравнения K=[что-то][H+]/[получ конц избытка] концентрацию оинов водорода. Верно?
-
напишите уравнение реакции и вычислите рН конечного раствора, приготовленного смешением 200 мл 0,1М раствора H2SO4 и 100 мл 0,2М раствора Ca(OH)2 с последующим разбавлением до 10 л. Реагенты – сильные электролиты, диссоциирующие полностью. Итак, их сложение дает CaSo4+2H2O, что дальше делать? Как подсчитать конц ионов водорода? Я спрашивал у кое-кого, мне сказали, мол, количество того, что получится в избытке, надо делить на 10 л, и оттуда плясать, верно? А как узнать что в избытке?
-
Нахождение состава раствора NaCl известной плотности.
komisar_rus опубликовал тема в Решение заданий
Такая задача: Рассчитайте молярную концентрацию, молярную концентрацию эквивалента, моляльную и массовую концентрацию, используя значение плотности. Дано ра-р Nacl p(pho)=1050 г\л. Мои вопросы: по таблице концентраций можно узнать массовую долю соли, если "ближайшая" плотность в таблице это 1056 (w=8%)? Если так, то тогда: как искать молярную массу эквивалентов? что такое массовая концентрация? Масса в-ва на массу растворителя что ли? -
-
В задании написано:"С - исходная концентрация вещества", но ведь тут два вещества в начале дано, или в нашем случае ионы "не считаются"?
-
Итак, есть задание по кинетике. В общем-то задание (посчитать константы скорости при температурах и скорость реакции в момент времени) понятно, но вот реакция - нет (см. прикрепленное) Вопрос: что значат эти точки и как это обозначение повлияет на алгоритм решения аналогичных задач с обычнимы реакциями? NO*+Br2=NOBr+Br*
-
Дана реакция CH4+4Cl2 = CCl4+4HCl Температура 6650 К Я рассчитал (возможно неверно) изменение энергии Гиббса, через приращение энтальпии и энтропии, получил ПОЛОЖИТЕЛЬНОЕ ЗНАЧЕНИЕ, сделал ввод, что реакция протекает обратная, однако надо узнать, как на равновесие в реакции влияет повышение\понижение давления, но как я вижу, кол-во вещества газа слева и справа равно 5, как же тогда быть? использовать данные, полученые при вычислении энергии Гиббса? Помогите пожалуйста.