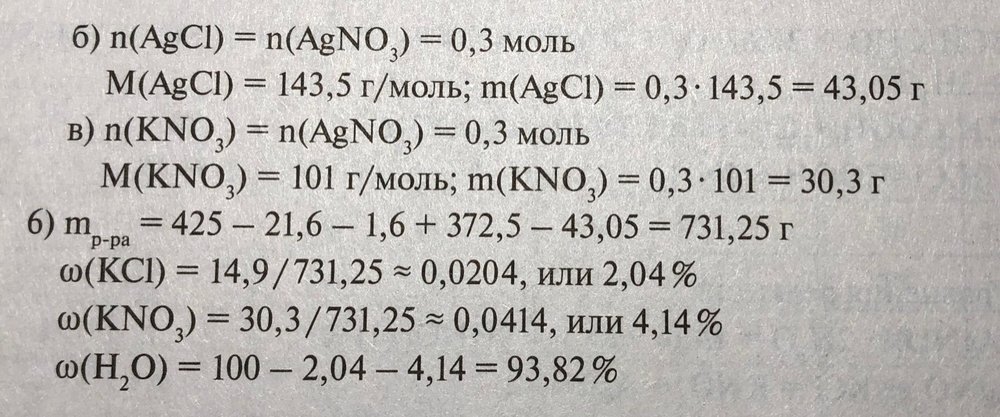Поиск
Показаны результаты для тегов 'электролиз'.
Найдено 125 результатов
-
Здравствуйте! Хотел спросить: подойдёт ли формула на скриншоте для расчёта напряжения в электролизëре?
-
Здравствуйте! Мне нужно придумать, как сделать электролиз эффективнее (чтобы при тех же количествах веществ тратилось меньше энергии). У меня такая идея: сделать в одном электролизëре n пар катод-анод (при этом подводить ко всем ним ток I через один разветляющийся провод и отводить через такой же), то есть n катодов и n анодов, и тогда, как при параллельном подключении проводников, через каждую пару катод-анод должен проходить ток I/n, энергия, затраченная на каждой паре = (I/n)²Rt = I²Rt/n², а энергия, затраченная всем электролизëром = nI²Rt/n² = I²Rt/n. При том, что при одной паре катод-анод тратится энергия I²Rt, то есть сколько пар катод-анод в электролизëре, во столько же раз меньше суммарная затраченная энергия. Я правильно понимаю? Просто у меня нет возможности опытным путём это проверить.
- 8 ответов
-
- электролиз
- электрод
-
(и ещё 2 )
C тегом:
-
Вот интересно 1)влияет ли кол-во вольт и ампер на выход продуктов электролиза? 2)могут ли меняться продукты в зависимости от подаваемого напряжения и силы тока (возможно звучит смешно но я объясню) Раньше у меня не было возможности добыть электролизёр (сейчас кое как собрал дохленький) ну и воспользовался тремя соединенными между собой зарядниками для телефона провёл тогда электролиз р-ра хлорида натрия железными гвоздями ну было явно видно образование зеленого гидроксида железа 2 А сейчас провёл эл-з как раньше вместо гвоздей взял металлическую проволоку диаметром 6мм только зелёного цвета незаметно какая-то бадяга чёрная ещё к магниту липнет при выпаривании неохотно воду отдаёт после выпаривания похож на оксид железа 2 при дальнейшем нагревании какая то вонь идёт легче воздуха (у потолка скапливается) а затем из чёрного порошка переходит в красный скорее всего оксид железа 3 и по прежнему липнет к магниту Из второго эл-за вытекают вопросы 1)Что за вонь прёт 2)Чёрная бадяга это гидроксид железа 2?Если да почему не зелёного цвета как в первый раз?
-
Многие советуют делать электроды из графитовых вставок трамвайных пантографов, которые можно найти вдоль путей. Однако трамваи вымерли как рудимент, и никаких кусков графита не достать. Мне доступен лишь "карандашный графит", но он полный отстой -- быстро разрушается. Какая может быть легальная и дешевая альтернатива "трамвайному графиту"? Ехать в другой город ради того, чтобы шастать там вдоль трамвайных путей без гарантии что-то найти -- занятие такое себе. Спускать деньги на ветер, покупая платину или золото я тоже не хочу. Я планирую получить хлор и перхлорат натрия путем электролиза насыщенного раствора поваренной соли -- электроды не должны быстро разрушаться. P.S. Стоит ли пройтись вдоль обычных ж/д путей в поисках таких вставок, или там их найти маловероятно? Электрички тоже, по идее, от провода запитаны, тоже должен быть там графит
-
Решить задачу в рабочей тетради. При электролизе 400г 30% р-ра гидроксида натрия на катоде выделилось 5,6л (н.у) газа. Найти массовую долю оставшегося в-ва в электролизере и объем газа (н.у.)
- 7 ответов
-
- электролиз
- naoh
-
(и ещё 5 )
C тегом:
-
Чему равно количество использованного электричества (в числах "F"), если при электролизе водного раствора сульфата кобальта (CoSo4) с инертными электродами на катоде выделилось 118 г вещества. Какое это вещество? Что и в каком количестве выделилось на аноде?
-
- электролиз
- электрохимия
-
(и ещё 1 )
C тегом:
-
Здравствуйте! При решении задачи столкнулась с неточностью в ответе. В решении, указанном составителями сборника, в ответе не учитывается концентрация HNO3, хотя при расчёте массы раствора массу азотной кислоты не вычли. То есть в растворе она есть, но её массовую долю не находят. Можете ли объяснить, почему? Или же это просто неточность или опечатка? Заранее благодарю за помощь. Прикрепляю условия задачи и решение:
- 1 ответ
-
- егэ
- егэ по химии
- (и ещё 7 )
-
В книге Томилов АП Смирнов ВА Каган ЕШ электрохимические синтезы органических препаратов Ростов 1981 на стр 86 описан синтез адипонитрила с магнетитовым анодом. Собственно вопрос можно ли магнетитовый заменить на двуокись свинца или ММО-электрод? Или подскажите ещё какой то вариант синтеза из акрилонитрила.
-
- акрилонитрил
- магнетит
-
(и ещё 1 )
C тегом:
-
Хочется получить терморасширенный графит. "Известны способы получения вспененного графита путем его смачивания окислителями (перекисью водорода, бихроматом калия, перманганатом калия или галогенкислородными соединениями формулы МХОn) в сочетании с серной или азотной кислотой...". Но, вроде, электролизом это сделать проще и дешевле. Нашлись видеоролики только на английском. Но, не пойму подробностей процесса из-за проблемами с английским. electrochemical exfoliation H2SO4 Яндекс перевел как "электрохимическое отслаивание H2SO4" ( ) Exfoliation of Graphite by means of Plasma Electrolysis Conscious Energies (Отшелушивание графита посредством электролиза плазмы сознательная энергия) ( )
- 15 ответов
-
- интеркаляция
- графит
- (и ещё 2 )
-
Подскажите сколько кг нужно медного купороса для получения методом электролиза 1л серной кислоты? И какие параметры должны быть у аккумулятора?
-
Некоторые жидкости образуют азеотропные смеси с водой и их нельзя осушить выпариванием. Предлагается для этой цели использовать электролиз с инертными электродами. Если целевая жидкость не разлагается при электролизе, то вода разложится на водород и кислород, целевая жидкость останется. Можно ли таким способом осушить до 100% концентрации серную кислоту; этиловый спирт; глицерин? Какие ещё вещества можно было бы так осушать?
-
Мелкозернистый плотный конструкционный графит марки МПГ-7 высший сорт. Зоготовки блок размером: 220х220х110 мм, 10кг, с небольшими сколами. Видно на фото. Цена: 400 рублей/кг. Бруски размером: 198х150х100 мм, 5,4 кг Цена:500 рублей/кг Есть дополнительная возможность распилить заготовки, для изделия ваших размеров. Физ-механические свойства: Плотность, не менее 1,8 г/cм3 Предел прочности при сжатии, не менее 65 МПа Предел прочности при изгибе, не менее 35 МПа Удельное Электрическое Сопротивление (УЭС), не более 12 мкОм*м Содержание золы, не более 0,25% Возможна доставка по РФ почтой: наложенным платежом. Или транспортными компаниями. Посмотреть графит МПГ можно в Екатеринбурге, район Упи Урфу Втузгородок. Подробности здесь в личке, или комментариях. А лучше по телефону. 8-922-027-89-85
- 8 ответов
-
- графит
- электролиз
- (и ещё 6 )
-
Подскажите, если кто-то знает, какое оборудование необходимо для электролиза? В частности где и какой взять аккумулятор?
-
Здравствуйте, очень нужна помощь. Дан электролиз раствора NaNO2, на выходе были получены NaNO3, NH3 и H2. Кто нибудь может помочь записать эту реакцию, заранее спасибо)
- 10 ответов
-
- электрохимия
- электролиз
-
(и ещё 1 )
C тегом:
-
Всем доброго времени суток! Ребята очень нужна Ваша помощь! Имею луженную медь, как правильно снять олово электролизом? Химией снять получается, травлю в солянке, и как я понимаю, то я получаю хлорид олова, а хотелось бы получить меиалической олово и медь сохранить. Заранее всем благодарен!
-
При электролизе кислородосодержащих кислот с нерастворимым анодом происходит разложение воды. Увеличивается ли при этом концентрация кислоты? Можно ли понизить таким образом содержание воды?
-
хочу попробовать сделать сетку катализатор для каталитической грелки гк-1. там на ней есть платиновое покрытие 0.0017 гр. здесь была тема про извлечение платины из кондеров, но я думаю использовать какоенибудь драгоценное изделие(лом). какое количество платины в ломе может быть? что нужно для растворения,электролиза? если не лень то поподробнее опишите пожалуйста,как для полного профана. кобальто-хромовые катализаторы не предлагать. живу в Узбекистане, так что по возможности предлогайте не очень редкие составы,растворы и т.д. все это для походов,обогрева тела зимой. спасиба заранее.
- 7 ответов
-
- платина
- электролиз
-
(и ещё 2 )
C тегом:
-
Сколько кубических метров 18%-ного раствора поваренной соли (ρ=1,132 г/см3) должно быть подвергнуто электролизу, чтобы получить 1 т 30%-ного раствора соляной кислоты?Сколько кубических метров 18%-ного раствора поваренной соли (ρ=1,132 г/см3) должно быть подвергнуто электролизу, чтобы получить 1 т 30%-ного раствора соляной кислоты?
-
Изобразите схему электролизной системы для получения металлического никеля на стальной (Fe) подложке.Заранее благодарен.
- 2 ответа
-
- схема
- электролиз
-
(и ещё 2 )
C тегом:
-
Провожу электролиз раствора серной кислоты свинцовым анодом и графитовым катодом.Анод покрылся диоксидом как и положено но какая-то непонятная вонь летит не пойму что это.Концентрация кислоты не велика 10% примерно.Получил раствор разбавлением конц кислоты.Кислота грязная загрязнена органикой ну на производстве её использовали для получения хлорпарафинов прочитал на сайте фирмы.Могут ли хлорпарафины при окислении кислородом на аноде давать вонючие соединения?
-
Доброго времени суток, уважаемые химики. Когда-то давно мне здесь писали, что при бездиафрагменном электролизе раствора NaCl может образоваться перхлорат натрия. Я поставил себе целью получить его таким образом. Кто-нибудь использовал этот метод при домашнем получении NaClO4? Какие ток и напряжение оптимальны и безопасны для данной цели? Как потом очищали полученный перхлорат от влаги и прочих хлорных солей? Заранее спасибо
-
Составьте схему процессов, происходящих при электролизе водного раствора KNO3 на медных электродах. Какая масса газа выделится на катоде при пропускании через раствор тока силой 12 А в течение 30 мин?
-

Очистка металлических изделий от ржавчины с помощью электролиза
pupkin027 опубликовал тема в Электрохимия
Применяю электролиз для очистки старинных изделий от ржавчины. В качестве электролита-сода. Всегда использовал в качестве анода нержавейку, но недавно прочитал что при ее использовании в процессе образуется хромат натрия. Что можно использовать как альтернативу? Обычную сталь использовать не хочу т.к. быстро разъедается и загрязняет раствор. И еще, последнее время при чистке латунных изделий они начали покрываться серым металлическим налетом, который трудно счищается. Раньше такого не было. В чем может быть проблема? -
Здравствуйте, В университете задали собрать аккумулятор и мы определились на газовом аккумуляторе Преснякова. Два карбоновых электрода , обмотаны мешочками с активированным углем(абсорбентом ), опущены в 15% раствор NaCl. Суть в том, что при подачи напряжения на электроды выделяется хлор и гидроген, которые впитываются активированным углем. Разность в потенциалах этих двух газов создает напряжение, которые позже можно использовать, как аккумулятор. Я нашел много информации с конкретными числами, но нигде нет расчетов. Здесь более подробно расписано: http://batareyki.105mb.ru/prostoy_akkum.html Формула реакции: 2NaCl + 2H2O -> H2 + Cl2 +2NaOH. Во всех источниках сказано, что заряжать нужно при напряжении 4.5 Вольта, но по моим рассчетам 2.5 Вольта достаточно. Подскажите, как это правильно посчитать? Меня также интересует ток, которым стоит заряжать. Влияет ли это как-то? Как посчитать напряжение и емкость в А*ч после заряда? Насколько это опасно? Насколько я знаю, хлор в виде газа достаточно опасный. Прошу помочь и извинить за ,может быть, глупые вопросы для химиков. Первокурснику, который изучает сенсорные технологии это сложно дается) Буду рад любому совету!
- 16 ответов
-
- газовый аккумулятор
- электролиз
-
(и ещё 3 )
C тегом: