
Даврон
-
Постов
91 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные Даврон
-
-
Первый раствор: рН1=1 V1=1л
Второй раствор: рН2=х V2=1л
Объединим) первую раствор со вторым и получаем третий раствор: pH3=7 V3=2л
Найдите рН 2-го раствора (х)
Я сделал вот так но сам себе не уверен.
((рН1*V1)+( рН2*V2)) / (V1+V2)=рН3 (есть ли такая формула?)
(1*1 + 1*х) / (1+1) = 7
х=13
Всё правильно?
-
Спасибо вам большое!
-
Сколько молекулы воды может окружать одну молекулы Н2О с помощью водородной связи? (Я признаю что, мне была трудно перевести вопрос. Пишите если не понятно, я думаю что нибудь по другому.)
-
Там плохо с этим, в соединениях с галогенами принимают другой радиус. Сильное оттягивание электронной плотности, другие взаимодействия
Вы можете подробнее объяснить того, чего как происходит оттягивание плотности облака (электронной) , и других взаимодействии. Вероятно, может эти вопросы мне попадает в поступающих экзаменах. Заранее Спасибо!
-
Внимание, вопрос: откуда взята величина 0.5, когда обычно берут 0.3?
Не знаю откуда. ( Может быть это всё чушь)
Вы хотели сказать о том , что водород ков. радиусом 0,5 не существует? То есть водород имеет единая величина (0,3). Могу ли я рассчитывать на вас?
И ещё, можно ли вот так уточнить ков. радиус?: 0,74/2=0,37 в место 0,3
-
Всем привет! (Без меня не соскучились?) Была такая задача:
Ковалентные радиусы брома и водорода соответственно сравна 0,85 А и 0,5 А. Найдите расстоянию между ядрами двух брома (то есть в молекуле Br2 ) и водород бромида (HBr).
А теперь мой вопрос: Если ковалентный радиус водорода сравна 0,5 А то у нас получается, что расстояние двумя ядрами водорода будет 1 А. Но мы знаем что это не так. То есть должно быть 0,74 А. По каким причинам водород имеет разные ковалентные радиусы?
Заранее спасибо!
-
Это чистая условность, но принято считать, что если стрелка вверх, то +0,5, стрелка вниз -0,5
Кстати значения магнитных квантовых чисел для квантовых ячеек, тоже принято размещать упорядоченно:
-2; -1; 0; +1; +2
Поэтому для электрона в последней ячейке я бы написал следующий набор чисел: n=3; l=2; m=+2; s= +0,5
Но слова "последний электрон" можно понять и так, что это последний электрон пришедший при заполнении подуровня.
Таким последним является второй электрон во второй ячейке
Для него набор квантовых чисел такой: n=3; l=2; m= -1; s = -0,5
Спасибо вам!
Значить стрелка вверх прибывает первым и получает число +0,5. а стрелка вниз прибывает последним.
Я не очень понимаю русского языка. Хотел бы ещё раз спросить: куда делся 5,2 гр Zn на теме "электролиз"? Вы не могли бы подсказать с простыми словами. Заранее спасибо!
-
Найдите квантовое число для последнего электрона 3d7
n=3; l=2; m=-1; s=?
Я бы сокращал первые две пары и сказал бы +1.5 (остальные три ячейки). Мне когда - то так научили. Но сейчас я думаю есть и другой вариант в место этого.
Помогите найти спиновую квант (либо +0,5, либо -0,5).
-
На аноде идет окисление (растворение) цинка:
Zn - 2e = Zn2+
А вот на катоде сразу 2 реакции
Восстановление ионов цинка
Zn2+ + 2e = Zn
и восстановление воды:
2H2O + 2e = H2 + 2OH-
Раствор подщелачивается (если не содержал избыток кислоты)
И в осадок начинает уходить гидроксид цинка.
Суммарно этот процесс можно записать так:
2H2O + 2e + Zn2+ = H2 + Zn(OH)2
Мораль сей басни такова:
поскольку количество сульфат-ионов в растворе при этом не меняется, то и количество сульфата цинка остается неизменным!
Избыток цинка растворенный с анода будет уходить в осадок.
А массовая доля сульфата цинка возрастает, поскольку в ходе электролиза расходуется вода и уменьшается масса раствора.
Дальше просто: цинка перешло в осадок по реакции 3: 31,2-5,2=26 г или 0,4 моль
Значит воды истратилось 0,8 моль (14,4 г), масса раствора стала равной 85,6 г,
Массовая доля 20/85,6 = 0,233 = 23,3%
Спасибо вам. Но мне тут непонятно что - то. Потеряет ли анод 31,2 гр Zn ?
Масса катода увеличивает на 5,2 гр (ну как сказать) благодаря цинка входящий в состав соль? Соль потеряет 5,2 гр цинка и вместе его берут обратно Zn у анода? Подскажите пожалуйста тут всё правильно? Я просто так думал.
-
Ну, не знаю. У меня получилось вот такое решение...
1) Из того, что на гидрирование 1 л смеси непредельных уходит 1,8 л H2, однозначно следует, что в смеси содержатся CnH2n (алкен) и CmH2m-2 (алкин или алкадиен, что для решения данной задачи не принципиально).
Уравнения гидрирования не привожу, так всем понятно: если вступило x (л) алкена, на его гидрирование ушло столько же водорода, т.е. x (л). На гидрирование (1-x) л "алкина" потребуется вдвое больше водорода, т.е. 2(1-x), а всего водорода потребовалось 1,8, откуда из линейного уравнения x=0,2 л. (объём алкена в смеси), т.е. объём "алкина" 1-0,2=0,8 (л).
Далее - банальный подбор. В "алкине" не может быть более 2-ух углеродных атомов, т.к. при сжигании C3 образуется 3*0,8=2,4 (л) CO2, что уже противоречит условию. Сл-но в смеси было 0,8 л C2H2 и 0,2 л CnH2n. Т.к. при его сжигании образовалось 2,2-1,6=0,6 (л) CO2 , то отсюда n=0,6/0,2=3, т.е. в смеси был пропен.
Отсюда Mсм = x(C2H2)*M(C2H2) + x(C3H6)*M(C3H6) = 0,8*26 + 0,2*42 = 29,2, т.е. DHe = 29,2/4 = 7,3, как и в ответе.
С уважением.
Спасибо вам. Ваш метод понятнее и подробнее.
Не так немного: Обозначим исходную смесь так: СхНу
Переходим к молям (объемы пропорциональны молям)
При гидрировании 1 моль смеси присоединяется 1,8 моль Н2 или 3,6 моль Н
При сгорании 1 моль смеси образуется 2,2 моль CO2, значит и получаемый
1 моль алканов будет иметь 2,2 моль углерода в 1 моль
Смесь алканов имеет формулу алканов СхН2х+2
Подставляя х=2,2, получаем, что в этой смеси алканов водорода 6,4 моль
Значит в 1 моль СхНу водорода было 6,4-3,6= 2,8 моль
И средняя формула исходной смеси С2,2H2,8
Средняя молярная масса такой смеси 29,2 г/моль;
Плотность по гелию DHe = 7,3
И вам тоже спасибо. Ваш метод не только простой но и хитрый! Я буду переписать всех троих.
-
Сделали электролиз 100 гр 20 %- го раствора ZnSO4 с помощью электродов сделанный из цинка. Когда остановили процесс масса анода уменьшилась на 31,2 гр, а масса катода увеличилась на 5,2 гр. Найдите % концентрацию ZnSO4 в образовавшем растворе.
Объясните пожалуйста, как влияет электроды к реакцию, если они одинаковые ну вот так:
электрод соль
Zn ZnSO4
-
Углеродиков там (2.2/22.4) моля 0,098*12= 1,176
Водородиков там (2.2*2/22 4+2-2*1.8/22.4) моля в итоге вышло 2,036
(12*углеродики+водородики) масса 1 литра смеси 1,176+2,036=3,212*22,4=72/4=18
Надеюсь я не ошибся в втором красном строке. У нас ответ не получается. Пожалуйста обратите ещё раз внимание на это. А)7,3 Б)9,7 С)19,4 Д)14,6
-
Для того чтобы получит алканы из двух ненасыщенных углеводородов (1 л смесь) требуется 1,8 л водород. При сгорание того же смеси образуется 2,2 л СО2 . Найдите сравнительную плотность начальной смеси по гелию.
Всем привет! Давно не общались, пожалуйста помогите решить!
-
yatcheh, Спасибо вам. Первый вариант сработал! -
-
Теперь я понял почему столько грамматических ошибок, человек из Узбекистана.
Да, здесь всем трудно со мной работать, но не стоит меня недооценивать.
-
Если образовавшая вещества F является 3,4-диметил пентадиен -1,3, найдите массовая соотношения вещества А и B
-
При гидролизе фрагмента нуклеиновой кислоты массой 12 мг образовалась 12,24 мг смесь нуклеотидов. Если она состоит из 81 нуклеотидов вычислите его молекулярная масса (Далтон).
Далтон эта абсолютная масса что ли?
-
Спасибо вам большое M_GM. Используя эту уравнению H(C6H10O5)nOH + (n-1)H2O + nC6H12O6 я решил другую задачу похожий на этом! В неё нет проблемы с условием. Я всё понял! Простите за таких странности. Я пока не могу связаться с учителям или со друзьями. Поэтому я обращаюсь здесь. Берегите себя, я вам ещё нуждаюсь.
-
При полном гидролизе олигосахарида ((С6Н10О5)n )массой 71,28 гр образовалась только глюкоза. Потом в этом реакции : С6Н12О6 → С3H7COOH + 2CO2+ 2H2 выделился 1,6 моль газ. Найдите n ?
х=0,4*180= 72гр 1,6
С6Н12О6 → С3H7COOH + 2CO2+ 2H2
1 4
71,28 - 72= 0.72 гр воды/18= 0,04моль
(С6Н10О5)n + nH2O = nС6Н12О6
0,4/0,04=10 но этого делал ничего не понимая. Я просто хотел получить ответ. Даже не знаю правильно ли я делал? Мне нужна ваша помочь! Объясните пожалуйста!
-
M_GM, Спасибо вам большое!!!
-
Вероятно опять проблемы с условием задачи, или с ответами на нее.
Так как я всё правильно сделал?
-
Электролизная уравнения раствора СnH2n+1COOK
-
Для полного нейтрализации олеума формулой Н2SO4*1,5SO3 израсходовано 20% раствор едкого натра. К образованному раствору добавили олеум H2SO4*4SO3 массой 118,3 гр и получили олеум с тем же составом, как и начальный. Найдите массу 20% - го раствора (NaOH) который был израсходован. А)200 Б)100 С)150 Д)75
118,3 х=5,09
H2SO4*4SO3+ Н2О = 2Н2SO4*3SO3
0.2х y= 0,063х + 0,8х = 0,863х
H2SO4*1.5SO3 + 5NaOH = 2.5Na2SO4 + 3.5Н2О Н2О вода р-р NaOH
200 63
5,09/0,863х=5,8 гр раствор NaOH
Я думал что так нужна решать. Но как видите ответ совсем не совпадает???
Прошу помочь.

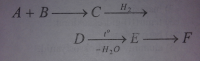
рН раствора
в Решение заданий
Опубликовано
Спасибо я всё понял!