Несколько задачек по теме:
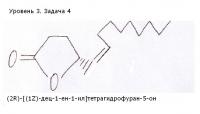
1) Феромон японского жука джапонилур ( как вам название) представляет собой (2R)-[(1Z)-дец-1-ен-1-ил]тетрагидрофуран-5-он. Напишите его структурную формулу.
примерно так:
извините, что корявенько
2) несложная, но забавная:
Теория типов
В середине прошлого века в органической химии господствовала теория типов, согласно которой превращения органических соединений описывались подобно реакциям простейших неорганических веществ – H2, HCl , H2O , NH3. Так, образование водорода из хлороводорода (тип HCl ) и натрия и его реакцию с хлором (образование HCl ) в соответствии с требованиями теории типов можно записать следующим образом:
Углеводороды относили к типу водорода, т.к. они могли быть получены подобно водороду из алкилхлоридов (тип RCl ) и в реакциях с хлором образовывали HCl .
1. В соответствии с теорией типов для этана можно написать две типические формулы. Напишите уравнения получения этана и его реакции с хлором в формулах теории типов.
2. Одна из «типических формул» этана позволяет предположить возможность второго (гипотетического) направления реакции этана с хлором, при котором HCl выделяться не будет. Напишите уравнения такого гипотетического превращения этана.
3) Моя любимая (хотя, думаю, почти все ее решали):
Ядерный синтез на Солнце
Источником солнечной энергии служит следующая последовательность реакций ядерного синтеза:
1 H + 1H -> 2 H + b+ + n;
2 H + 1H -> 3 He + g;
3 He + 3He -> 4 He + 21H,
где b+ – позитрон (антиэлектрон), n – нейтрино, g – гамма-излучение. Напишите суммарное уравнение процесса «горения» водорода на Солнце. Рассчитайте, какая масса (в а.е.м.) теряется при образовании одного ядра атома гелия в этом процессе. Используя формулу Эйнштейна E = mc2, найдите, сколько энергии выделяется в данном процессе ядерного синтеза из 1.000 г водорода. Во сколько раз эта энергия больше, чем энергия, выделяющаяся при сгорании 1.000 г водорода в атмосфере кислорода? При расчетах используйте следующие данные: m(1H) = 1.00727, m(b+ ) = 0.0005486, m(4He) = 4.00273 (массы выражены в а.е.м.), теплота образования жидкой воды 286 кДж/моль.
4) Вещество z представляет собой мелко-кристаллический порошок с металлическим блеском. Навеску его массой 2,8 г разделили на две равные части. Первую часть растворили в избытке концентрированной азотной кислоты при нагревании и упарили раствор до удаления следов HNO 3 . Вторую половину растворили при нагревании в избытке раствора едкого натра. Получившиеся в обоих случаях растворы вызывают посинение подкисленного раствора иодида калия с крахмалом.
К каждому из растворов добавили избыток подкисленного раствора иодида калия с крахмалом и оттитровали 1 М раствором тиосульфата натрия до исчезновения синей окраски. Для первого раствора потребовалось 66 мл тиосульфата, для второго 11 мл.
Определите состав вещества z и напишите уравнения упомянутых реакций.
HClO , HClO 2 , HClO 3 , HClO 4 :
1) Как и почему изменяется сила кислот в этом ряду?
2) Какое соединение, KClO или KClO 3 , является более сильным окислителем? Подтвердите Ваш вывод, используя реакцию с одним и тем же восстановителем.
3) Используя в качестве единственного источника хлора К Cl , предложите схему синтеза Cl О2. Напишите уравнения реакций, укажите условия их проведения.