
Химический смех
-
Постов
280 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные Химический смех
-
-
18 часов назад, yatcheh сказал:
Вас "C" смутила? Это не концентрация, константа интегрирования. Она равна 1/x0.
А формулы одинаковы, просто я обозначил С = x и С0 = x0
Концентрация x0 (С0) нам неизвестна, но она и не нужна для вычислений.
Извините, что-то все-равно не доходит до меня эта задача. Почему мы можем пренебречь начальной конц-й и принять ее за нуль? Ведь тогда получится деление 1 на нуль и условно мы должны вычесть из (1/текущая конц-я) бесконечно большое число. Даже если просто отбросить (1/С0) и посчитать, то получится 981 миллион, что очень далеко от ответа. К слову, ответ k = 2,42 × 10^7 л/(моль × с).
-
3 часа назад, yatcheh сказал:
dx/dt = -k*x^2
dx/x^2 = -k*dt
1/x = С + k*t
Величина C у нас равна 1/x0, но она нам и не нужна, её можно принять за нуль.
Строим график в координатах 1/x (обратная концентрация) - t (время в секундах), определяем тангенс угла наклона прямой. Это и будет константа скорости.
Тоже самое можно сделать аналитически, взяв несколько пар значений из таблицы.
Не понимаю немного. Формула для второго порядка kt=(1/C)-(1/C0)
-
2 часа назад, yatcheh сказал:
А причём тут "моменты времени", если вам даны только скорости при разных давлениях?
w = k*A^x*B^y
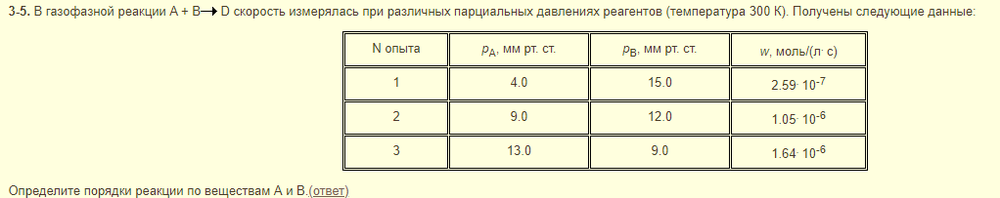
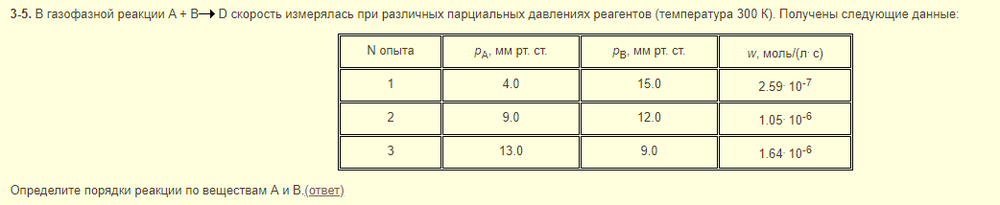
Надо по трём точкам найти сумму x+y. Для этого логарифмируем и решаем систему уравнений:
ln(w1/w2)=x*ln(A1/A2) + y*ln(B1/B2)
ln(w1/w3)=x*ln(A1/A3) + y*ln(B1/B3)
Все гениальное - просто) Спасибо Вам.
-
Как найти константу скорости через массу продукта? Подскажите формулы, пожалуйста
-
Как найти константу скорости, если неизвестна начальная концентрация? Подскажу, что реакция второго порядка по ответу.
-
-
21 час назад, yatcheh сказал:
Согласно уравнению Аррениуса
k = A*exp(-E/RT)
k1/k2 = A1/A2*exp((E2 - E1)/(R*283)) = 10
k1/k2 = A1/A2*exp((E2 - E1)/(R*313)) = 0.1
Делим первое на второе
exp((E2 - E1)/(R*283) - (E2 - E1)/(R*313)) = 100
(E2 - E1)*(1/(R*283) - 1/(R*313) )= ln(100)
E2 - E1 = ln(100)/((1/(R*283) - 1/(R*313) ) = 112867 Дж
Если, конечно, я нигде не накосячил в выкладках

А я правильно решил?
Правильно)
-
 1
1
-
-
Уже решила, извините

-
Вещество разлагается двумя параллельными путями с константами скорости k1 и k2. Какова разность энергий активации этих двух реакций, если при 10oC k1/k2 = 10, а при 40oC k1/k2 = 0.1?
-
18 часов назад, yatcheh сказал:
У ТС его энтальпия есть. А в растворе он на момент реакции, или нет - уже не важно (важно, но - не очень, в том смысле, что если дана энтальпия твёрдой соли, а он в растворе - это даст ошибку в расчётах, но вы сами говорите, что он только в растворе существует). Главное, что сода - твёрдая, а образующийся сульфит - в растворе. Отсюда и экзоэффект проистекает.
Что такое ТС?
17 часов назад, yatcheh сказал:А-а-а! Так эта каша по всему форуму размазана. Теплота растворения солей изрядно, бывает, зависит от концентрации, так что -866 - это почти ни о чём.
Если речь о технологических делах, тут нужны технологические справочники, а не академические вычисления В данном случае - теплота растворения SO2 в растворе сульфита заданной концентрации. Тем более, что раствор "бисульфита" может вовсе не содержать анионов HSO3-.
18 часов назад, Paul_S сказал:>У ТС его энтальпия есть.
Поинтересуйтесь, каким левым способом она его нашла. Ни в каких справочниках его нет. Я уже несколько месяцев слежу за потугами ТС обсчитать эту реакцию.
> Главное, что сода - твёрдая, а образующийся сульфит - в растворе.
С чего Вы это взяли? Все в растворе. Поэтому логично считать энтальпию этой ионной реакции через соотв. константы кислот.
Мне научрук те же самые значения потом отправил. Не знаю, где он их нашел. Вероятно, что в литературе. Это я про т/д характеристики гидросульфита натрия.
-
2 часа назад, Nemo_78 сказал:
Ну вот Вам и объяснение низкая растворимость гептагидрата сульфита натрия в воде при температурах повыше комнатной, что также находит своё отражение и в литературе (см. ссылку).
Все-равно не понимаю( Почему реакция по расчетам эндо, а идет с выделением тепла?
-
2 часа назад, yatcheh сказал:
Шо за манера - темнить, у вас что - подписка о неразглашении?

Покажите реакцию и расчёты.
2NaHSO3(ж)+Na2CO3(ж) = 2Na2SO3(ж)+CO2(г)+H2O(ж) (3.1)
Исходные данные для реакции представлены в таблице 1.
Таблица 1. Стандартные термодинамические величины для реакции (3.1)
2NaHSO3(ж)
Na2CO3(ж)
2Na2SO3(ж)
CO2(г)
H2O(ж)
ΔH(298), кДж/моль
-866
-1129
-1090
-393,51
-285,84
ΔS(298), Дж/моль*К
199
136
146
213,6
69,96
ΔН=2*(-1090)+(-393,51)+(-285,84)-2*(-866)-(-1129)=1,65 (кДж/моль)
Так как ΔН х.р. > 0, то Q х.р. < 0, реакция эндотермическая.
Цитата из учебника: За счет тепла, выделяющегося при нейтрализации гидросульфита натрия, раствор нагревается. Его охлаждают до температуры 311-313 К, так как при несоблюдении этого условия сульфит натрия выпадает в осадок.
-
Может ли эндотермическая реакция проходить с увеличением температуры смеси? По теории реакция идет с нагреванием смеси, но по расчетам она у меня получается эндотермическая.
-
2 часа назад, M_GM сказал:
Реакция будет протекать самопроизвольно, такие реакции обычно экзотермичны, значит температура раствора возрастет.
Более точный ответ требует расчета с учетом энтальпий растворения веществ и энтальпии хим. реакции.
А в чем вообще состоит суть вопроса? Я просто не совсем понимаю, что от меня хотят. Имеется в виду, что берут не два раствора, а два сухих вещества и смешивают их в воде?
2 часа назад, M_GM сказал:Реакция будет протекать самопроизвольно, такие реакции обычно экзотермичны, значит температура раствора возрастет.
Более точный ответ требует расчета с учетом энтальпий растворения веществ и энтальпии хим. реакции.
Почему может быть такое, что реакция идет по теории с выделением тепла, а по расчетам у меня получается эндотермическая реакция?
-
-
-
2 часа назад, aversun сказал:
-
Что содержится в отработанном воздухе после кристаллизатора? Кристаллизация насыщенного р-ра Na2SO3 с выпадением кристаллов Na2SO3
Насыщенный раствор сульфита натрия охлаждают во вращающемся трубчатом кристаллизаторе 5 воздухом - летом до 18-20 °C (20-25 °C), зимой до 10-15 °C. При этом из него выпадают кристаллы семиводного сульфита.
-
Какую формулу использовать при расчете порядка реакции в этой задаче? Я использовала ту, которая на фото, но у меня ничего путного не вышло.
-
18 часов назад, M_GM сказал:
Ход расчетов допустимый, но грубое округление искажает результат
Ты потом от своих 6,2 вычитаешь 3,38*10^(-4), т.е. 0,000338
Это должно было подсказать, что ln 500 надо брать с такой же точностью, т.е. до 6-го знака после запятой
Попробуем рассчитать, используя более точное значение ln500 = 6,214608
3,38*10^(-4)=6,214608-lnx
lnx=6,214608-0,000338=6,214270
x=499,831
Поняла. Спасибо. Учту на будущее

-
Решенная задача по химии. Объясните простым языком, пожалуйста. В частности, непонятна последняя строчка
-
16 часов назад, M_GM сказал:
Во-первых, беда с математикой
Нетрудно видеть, что ln 500/x = 3.38*10^(-5)*10 = 3.38*10^(-4)
откуда 500/х = EXP(0,000338) = 1,00033806;
откуда х = 500/1,00033806 = 499,831 (мм.рт.ст.) ;
Во-вторых, надо понимать что вы посчитали
- Вы посчитали парциальное давление исходного вещества N2O5(г), которое естественно уменьшается, т.к. это вещество расходуется. Но вам надо найти общее давление газовой смеси, в составе которой уже появились продукты реакции. Считаем:
dp(N2O5) = 500-499,831= 0,169 (мм.рт.ст.)
Учитывая, что давление пропорционально количеству вещества, а у N2O5 и продуктов реакции оно относится как 2:5 (см. ур-ние реакции), то:
p(NO2(г) + O2(г)) = (0,169/2)*5 = 0,423 (мм.рт.ст.)
и общее давление газовой смеси будет равно : Р = 499,831+ 0,423 =~ 500,3 (мм.рт.ст.)
- что и требовалось доказать

Я просто считала так:
3,38*10^(-5)=(1/10)*(ln 500/x)
3,38*10^(-4)=6,2-lnx
lnx=6,199662
x=492,6
Так неправильно считать, получается?
-
3 часа назад, M_GM сказал:
k=(1/t)*(ln P0/P)
3.38*10^(-5)=(1/10)*(ln 500/x)
x=492,6 мм.рт.ст.
В ответе 500,3 мм.рт.ст.
-
21.05.2020 в 17:27, Мигрень сказал:
нет, ответа пока нет
Если вы решите задачу или вам помогут с решением, то можете написать мне об этом, пожалуйста?) Я сама сейчас тренируюсь в решении таких задач и хотелось бы понять, правильное мое решение или нет




Тепловой баланс. Как найти температуру продуктов?
в Решение заданий
Опубликовано
1000 кг метана, поступающего в печь при температуре 20оС, сгорает в воздухе, содержащем 21%об.О2 и 79%об.N2. Избыток воздуха составляет 50% от стехиометрии. В результате расчета материального и теплового балансов определить температуру продуктов сгорания.
Я МБ составила. Мне кажется либо тут автотермичный процесс без дополнительного подвода или отвода тепла (но тогда почему не написали об этом в условии в отличие от других задач?), либо надо решать по формуле T=Q/V*C. Но что-то у меня какой-то бред по ней получается.
Как вы думаете, как надо найти Т в этой задаче?