
Carryn
-
Постов
232 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные Carryn
-
-
Все равно не понимаю, почему мы заменяем [Kt+] на С-[H+]. Вот расписала гидролиз по первой ступени Pb+ + H2o=PbOH+H+
-
2 минуты назад, M_GM сказал:
Всегда, когда идет гидролиз средней соли
Когда идет гидролиз кислой соли KHS, HS(-) + HOH = H2S + OH(-)
то берется Кд не по последней ступени, а по той, которая соответствует диссоциации образовавшейся при гидролизе частице (здесь - молекулы H2S), т.е. берется Кд(1) для H2S
Напиши уравнение гидролиза по катиону, и всё станет понятно.
Спасибо. Просто нашла в литературе, что эта формула используется только когда сильная соль и слабое основание, а не в общем случае средних солей
-
-
-
57 минут назад, M_GM сказал:
А что тут может быть? Естественно HCl в этой реакции уже не нужен, он отработал своё в первой реакции.
Поэтому: 2Сr(NO3)3 +H2 = 2Сr(NO3)2 + 2HNO3
Зеленая окраска, соли хрома(3) должна была смениться на голубую, характерную для солей хрома(2). Но как я уже писал:
Плохо, что при этом для реакции вы брали нитрат хрома (нитрат-ионы сами легко восстанавливаются) правильнее было проводить опыт с CrCl3.
Потому, скорее всего опыт прошел не удачно и изменения окраски вы не увидели.
- "h2 с ноликом" - я старался набирать не с ноликом, а со звездочкой H2*. Так обычно показывают молекулы в возбужденном состоянии
Спасибо большое!!! С ноликом атомарный водород обозначали при подготовке у олимпиадам. Могу дать ссылку(
скажите, пожалуйста, по неорганической химии какой самый качественный учебник к экзамену?
-
16.11.2020 в 14:41, M_GM сказал:
Сверху органический растворитель. Реакцию пишу cr(no3)3+hcl +zn=zn(no3)2+crcl2
+h2(не уравнено).Окислитель хром, восстановитель? Предположила, что водород из реакции цинка с соляной?
По той схеме что вы написали восстановитель цинк - он у вас окисляется.
На деле считается, что восстановителем является "водород в момент выделения" - молекулы водорода только-только образовавшиеся при реакции цинка с кислотой, обладающие повышенной энергией и активностью (H2* ).
Поэтому вашу схему лучше разбить на два уравнения - реакция цинка с кислотой и восстановление соли хрома водородом. Плохо, что при этом для реакции вы брали нитрат хрома (нитрат-ионы сами легко восстанавливаются) правильнее было проводить опыт с CrCl3.
2)k2cr2o7 (2 мл)+hcl (2 капли)+bacl2 пойдёт реакция? У меня пожелтение, одногруппники пишут у себя отсутствие реакции( - дихромат не дает осадка с хлоридом бария в отличие от хромата.
3)k2cr2o7 сильно разбавить водой. - не знаю, чего добивались этим разбавлением, возможно переходом дихромата в хромат Но это обычно происходит при добавлении к дихромату КОН. Может вы при наблюдении перепутали пробирки 2 и 3?
4)почему реакция k2cr2o7+hcl(2M) при комнатной температуре не пошла, а при легком нагревании вполне успешно осуществилась? А это секрет, что многие реакции заметно идут лишь при нагревании?
И снова мучаюсь с этой реакцией. Скажите, пожалуйста, реакцию cr(no3)3+Hcl+zn Вы посоветовали разбить на две реакции
Zn+Hcl=zncl2+h2(с нулем)
Как я поняла, полученный водород пойдёт На восстановление cr(no3)3, но вот реакцию я составить не могу(. Нашла где-то в литературе, что будет реакция cr(no3)3+Hcl+h2 с ноликом? А что в продуктах?
-
2 часа назад, aversun сказал:
В обоих случая выпал гидроксид железа (II и III).
Что бы железо III проявило свои амфотерные свойства надо очень концентрированный раствор щелочи, процентов на 50.
Гидроксид железа II амфотерных свойств не проявляет, но что бы его перевести в гидроксо-комплкс, надо раствор щелочи подобный концентрации, хотя я не помню, описано ли это где нибудь. Но если судить по гидроксиду магния, должно получится, при подборе соответствующей методики.
Спасибо большое!
-
Я окончательно запуталась((( Помогите, пожалуйста, разобраться. Делали опыт: соли железа 2 с разбавленной и концентрированной щелочью, и соли железа 3 с разбавленной и концентрированной щелочью. Во всех случаях что-то вываливалось в осадок( Вопрос только в том, ЧТО вываливалось. Я полагала, видимо ошибочно, что и железо 2 и железо 3 с разбавленной щелочью даст гидроксид, а с концентрированной - комплекс. А что на самом деле там происходит?
-
1 час назад, M_GM сказал:
K2[Al(OH)5(H2O)] - вот они пентагидроксо-
Спасибо, что поправили! Я тоже заблудилась в этих названиях, бо ни в школе, ни в вузе нас этому не учат(
2 минуты назад, Nemo_78 сказал:Нет, Вы не ошиблись, в том, что сейчас как-раз-таки и ошиблись. Ибо множительная приставка "пента-" относится к гидроксильному лиганду, а не к водице, как у Вас.
О чем, в прочем, Вас уже и уведомили...
Да, знаю. Спасибо!
-
20 минут назад, odnikolirna_veselka сказал:
Здесь на украинском написано, могу прислать перевод
вариант 4 1. Назовите комплексное соединение [CoBr (NH3) 5] SO4, определите и запишите: - степень окисления комплексообразователя; - координационное число комплексообразователя; - заряд комплексного иона; - заряд лиганда; - тип комплексного соединения: а-катионный, б-анионный, в-нейтральный; - уравнение диссоциации комплексного соединения по ионогенных связью и сумму его коэффициентов; - уравнение полной диссоциации комплексного иона и сумму его коэффициентов; - выражение константы диссоциации комплексного иона. 2. Напишите формулу калий аквапентагидроксоалюминату (iii) и вычислите его мольную массу (с точностью до целых).Первый называется сульфат пентаамминбромокобальта. (III) . Остальное можно найти в учебниках.
-
 1
1
-
-
-
18 минут назад, M_GM сказал:
То есть соль железа 2 даст гидроксид независимо от концентрации щёлочи, а соль железа 3 с разбавленной щелочью даст гидроксид, а с концентрированной щелочью часть гидроксид, а часть комплекс? Так?
-
19 минут назад, M_GM сказал:
Гидроксид железа(2) практически не обладает амфотерными свойствами
и не растворяется в избытке щелочиИ соль железа 2 и соль железа 3 будет с концентрированной щелочью давать комплекс?
-
Спасибо!
-
Подскажите, пожалуйста, а реакция kmno4+H2O+c6h12o6 в продуктах получится c6h12o7 или все же со2 и Н2О? Спасибо!
-
Доброго времени суток!
Подскажите, пожалуйста, в реакции feso4 и концентрированной щелочи и fecl3+ концентрированная щелочь будет комплекс по типу na2(fe(oh)4) и na3(fe(oh)6)?
И ещё вопрос: в реакции feso4+na2co3+h2o будет Гидроксид железа 2 в продуктах?
спасибо!
-
Спасибо! А в последней реакции kmno4+naoh+c6h12o6 в продуктах будет k2mno4+na2mno4+co2+h2o или k2mno4+C6h11o7na+mno2+h2o?
И посмотрите реакцию с ортованадием, пожалуйста.
-
Спасибо!
-
Не поняла по поводу первого вопроса. Если разбить на 2 реакции (мне надо где-то записать соляную), то будет zn+Hcl=zncl2+h2 и cr(no3)3+h2=? Так?
-
Спасибо за ответы. По поводу 4 вопроса не все так просто. Велено обосновывать через нернста.
-
Доброго времени суток!
опять опыты( Проверьте, пожалуйста, мои реакции. Опыт по смешиванию равных объемов перманганата с разбавленной серной, разбавленным гидроксидом и водой. В каждую пробирку кристаллики глюкозы. Зачем они нужны в этой реакции?
Kmno4+h2so4+c6h12o6->co2+k2so4+mnso4+h2o
kmno4+h2o+c6h13o6->c6h12o7+mno2+koh (у меня коричневый р-р)
Kmno4+Naoh+c6h12o6->mno2+c6h11o7na+koh +h2o (у меня светло-коричневый р-р).
Все реакции не уравнены. Посмотрите, пожалуйста, чушь написала или имеет право на существование.
и опыт с ортованадатом натрия, несколькими каплями соляной и кристаллами цинка
Na3VO4+hcl+zn->vo(cl2)+NaCl+zncl2+h2o
Это правильно? У меня вывалился какой-то жёлтый осадок...
спасибо!
-
Доброго времени суток! Прошу помощи. Вопросов много(
1)Делала опыт, к раствору 1 мл cr(no3)3 добавлялся 1 мл hcl (2M), а затем несколько гранул цинка. Сверху органический растворитель. Реакцию пишу cr(no3)3+hcl +zn=zn(no3)2+crcl2+h2 (не уравнено). И на этом этапе я понимаю, что ничего не понимаю. Окислитель хром, восстановитель? Предположила, что водород из реакции цинка с соляной? В общем запуталась((( Подскажите, пожалуйста.
2)k2cr2o7 (2 мл)+hcl (2 капли)+bacl2 пойдёт реакция? У меня пожелтение, одногруппники пишут у себя отсутствие реакции( У меня руки не из того места?
3)k2cr2o7 сильно разбавить водой. Продукты KHCr2O7+KOH?
4)почему реакция k2cr2o7+hcl(2M) при комнатной температуре не пошла, а при легком нагревании вполне успешно осуществилась?
Спасибо!
-
Спасибо!
-
Объясните мне, пожалуйста это) у меня контрольная совсем и скоро, а я не могу разобраться с теорией. Точнее я считаю, а у меня адовы цифры получаются
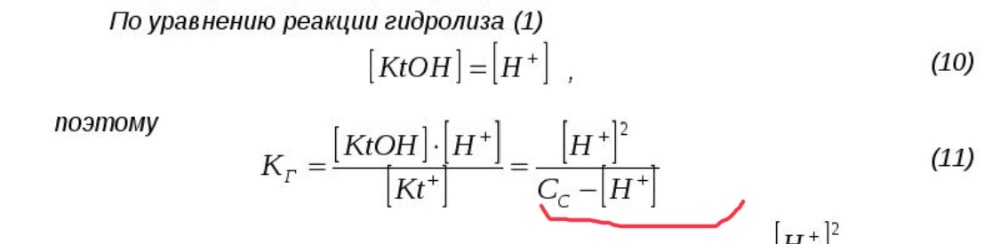


Вопрос теоретический по гидролизу
в Решение заданий
Опубликовано · Изменено пользователем Carryn
Зачем, зачем я пошла учить химию..
спасибо большое!