-
Постов
108 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Весь контент Farhad
-
N-бензилпропан-2-имин - по ИЮПАК
- 2 ответа
-
- 1
-

-
-
Благодарю! Вы очень сильно мне помогли!
-
Теперь я всё понял. Я просто неправильно Вас понял. Протон отщепило основание, оно же его впоследствии и отдало, так?
-
С третьим всё ясно. Насчёт второго: O2N-CH2- атакует CH3-O-(-O-)C=CH-CH2+ и получается CH3-O-C(=O)=CH(+)-CH2-CH2-O2N, а откуда берётся ещё протон? Или я не совсем понимаю.. Насчёт третьей стадии. В какой литературе можно откопать её? В Травне нет, Реутов мне тоже ничего не дал
-
Небольшое уточнение по второму заданию. Почему первая стадия не идёт как конденсация? Откуда третья стадия? И по возможности разъяснить механизм третьей задачки
-
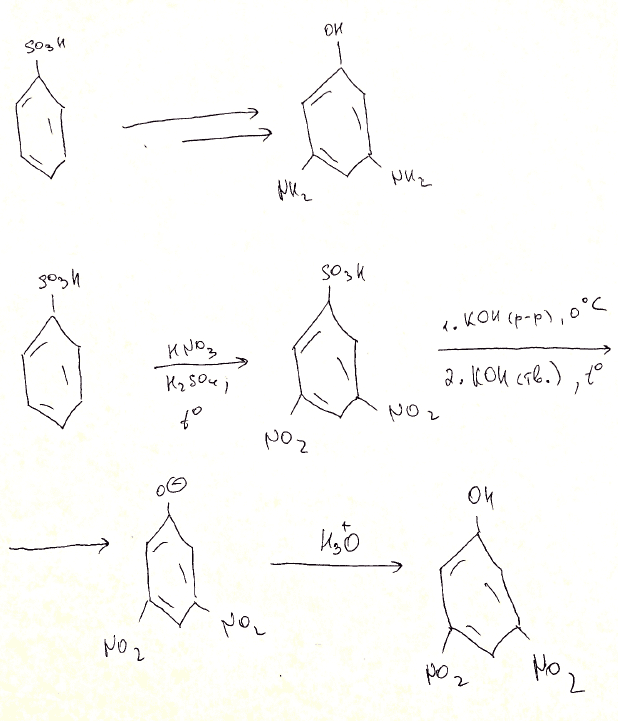
1. Из EtOH и i-PrOH (изопропанол) получить 3-амино-3-метилбутанол-2 2. Из MeNO2 и метилакрилата получить пирролидон-2 3. Завершить цепочку (картинка в приложении)
-
У нас одноименные ионы сульфата уже в марганце есть, они будут мешать определению
-
Нужно определить. То бишь, у вас есть смесь солей и задача определить выделенные соответствующими способами, при отсутствии влияния других солей при определении. Гравиметрическая форма бария BaSO4, да, но чтобы получить эту гравиметрическую форму, нужно сделать так, чтобы её получить. К примеру, MnSO4, BaCl2, ZnCl2, CH3COOH. Ну, вроде как все вещества растворимые и спокойно перейдут в раствор при растворении водой. Дальше нужно думать, как потихоньку избавляться от всего, что у нас есть, разделяя чистые вещества, дабы в дальнейшим определить их титриметрически (Mn, скорее всего комплексонометрическое с ЭДТА, ну или ещё как-нибудь) и гравиметрически (для Ba в форме сульфата). Для этого нужно отделить оба определяемых вещества, но при этом в максимальной чистой форме, без уксусной и без хлорида цинка.
-
Дана СМЕСЬ: CH3COONa, ZnCl2, MnSO4, BaCl Нужно гравиметрически определить барий, а титриметрически марганец, но учитывать, что дана смесь
-
Напишите уравнение кислотно-основного равновесия для ацетата натрия в метиловом спирте. Рассчитайте рН 0,0100 М раствора, приняв коэффициент активности за 1. (Для CH3COОН в CH3ОH Kа = 2,0·10-10, для CH3ОH KSH = 2,0·10-17)
-
да, но сначала их как-нибудь разделить и предположить где-что, а там можно и под качественные реакции)
-
Используя качественные реакции на ионы переходных элементов, определите какой раствор содержится в каждой из пробирок: VCl3, K2MnO4, NiSO4
-
Как можно разделить CdSO4 и Fe2(SO4)3. Изначально хотел добавить железных опилок, но как-то не очень, учитывая, что они стоят рядом по потенциалам.
-
Смесь Zn, Ag и Hg перевести любым возможными способами полностью в раствор; разделить и доказать присутствие каждого элемента; выделить каждый элемент в виде простого вещества. Напишите уравнения всех реакций и укажите условия их проведения.
-
Ну так сказать то легко. А Вы попробуйте. Ждать-то сколько придётся... P.S. Проверено на личном опыте
-
Теперь всё понятно, спасибо! Извиняюсь за тупые вопросы ))
-
Разве соляная кислота не способствует разрушение всех трёх этих комплексов? AgCl, CuCl2, ZnCl2 образовались, теперь приливаем к раствору щелочь и тут крайне не совсем приятная ситуация: AgCl + NaOH = Ag2O(осадок) + ..... CuCl2 + NaOH = Cu(OH)2(осадок) + .... ZnCl2 + NaOH = Na2[Zn(OH)4] + .... тут либо опять связывание в комплекс при избытке NaOH, либо при недостатке выпадение Zn(OH)2. Пусть будет избыток, чтобы Cu(OH)2 и Ag2O можно было разделить, ибо комплексные соединения сами по себе в осадок не выпадают, но имеют свойство перекрашивать растворы в красочные цвета. Теперь стоит задача разделения Ag2O и Cu(OH)2, не забывая, что в растворе есть Na2[Zn(OH)4]. Вот этот момент мне не особо ясен, почему именно горячий раствор смеси хлоридов?