MoreFeeling
Пользователи-
Постов
48 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Весь контент MoreFeeling
-
Спасибо, туплю немного, другой тоже третичный)
-
Спасибо, так вроде же тот фрагмент, где N-Me- это 1-метил-1,2,3,6-тетрагидропиридин, который хоть и слабое основание, но в присутствии минеральных кислот устойчив и протонируется. Почему по нему реакция не пойдет?
-
Здравствуйте, как тут определиться, по какому положению пойдет реакция и почему?
-
Доброго времени суток, подскажите, пожалуйста, насчет катализаторов BF3 и BF3*O(C2H5)2. В чем преимущество последнего кроме как в том, что в инертном растворителе эфират удобнее хранить? Трифторид-газ, но он дешевле. Почему в одних синтезах используют BF3, а в других BF3*O(C2H5)2.?
-
-
Спасибо, а если как-нибудь попроще,чисто на бумаге?
-
-
-
-
Спасибо, а как по-Вашему, что происходит с левым кольцом? Какое превращение к такому приводит?
-
-
Спасибо, а как примерно реакция будет выглядеть и с каким реагентом? Беда в том, что только гидроксильная группа при 5 атоме останется незатронутой. Как добиться такой избирательности?
-
Очень стало интересно, с чем же всё-таки можно связать эту необычную реакционную способность... Пока поиски успеха не принесли, к сожалению.
-
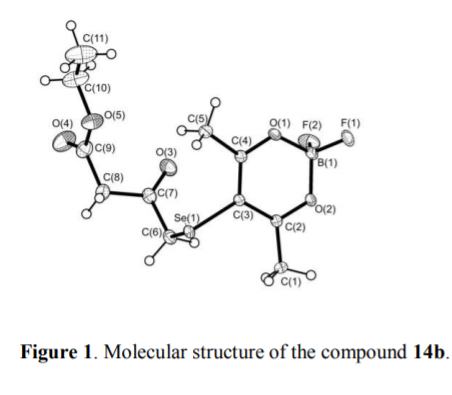
Судя по выдержке из основной статьи, РСА проводился для ацетоуксусного эфира, а ЯМР для ацетилацетона и ацетоуксусного эфира. Сути не меняет, оба соединения дают нестандартный продукт "Selenylchloride 2 reacts with acetyl acetone and with acetoacetic ester in a different way as compared to sulfur-containing analogue: the reaction proceeds by the terminal methyl group with the formation of the compounds 14 (Scheme 6). The structure of compounds 14a and 14b was defined by 1H NMR spectroscopy. Additionally, the structure of 14b was unambiguously determined by X-ray crystallographic analysis (Figure 1)" В статье также есть таблица с параметрами кристаллической структуры.
-
Да, всё крайне странно, тем не менее с ЯМР спорить сложно. Как говорится, это не фантазия, а факт.
-
Тема модная:)
-
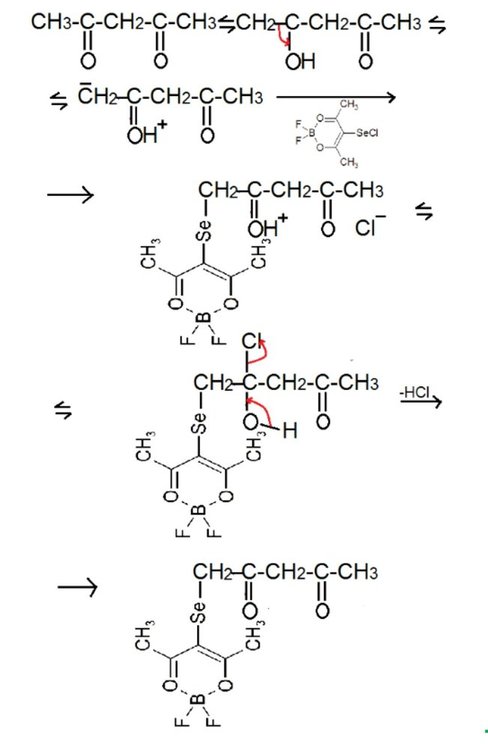
Доброго времени суток, возник такой вопрос: имеется два соединения сульфенилхлорид и селенилхлорид ацетилацетоната дифторида бора. Они реагируют с енольными формами ацетилацетона. Возникает вопрос, почему селенилхлорид реагирует по метильной группе( на картинке) а сульфенилхлорид по метиленовой? Может быть, будут какие-нибудь перегруппировки или же разная устойчивость?Как я понимаю, в случае сульфенилхлорида будет другая форма енола взаимодействовать. И насколько правильно изображен механизм, подскажите, пожалуйста? Второй енол типа CH3-C(OH)=CH-C(O)-CH3
-
-
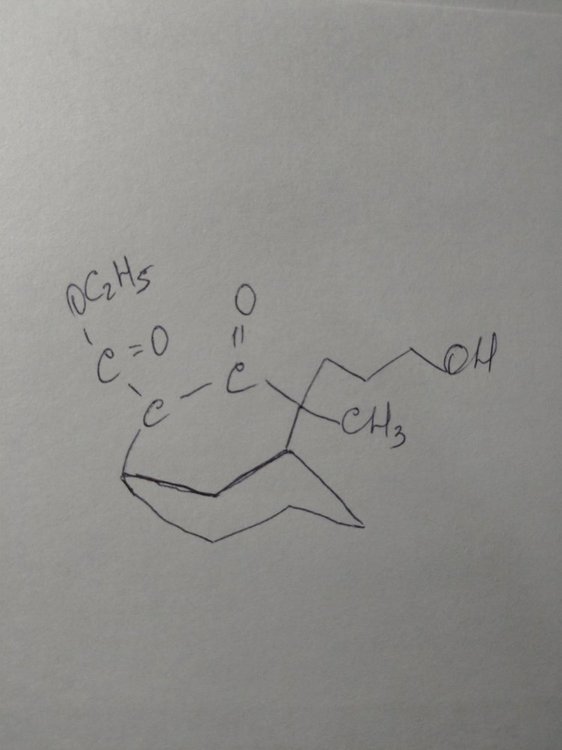
Спасибо, а как называется соединение, где есть двойная связь с циклом и кето-группа?
-