
NelloN06
-
Постов
107 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные NelloN06
-
-
16 часов назад, St2Ra3nn8ik сказал:
Поищите на https://www.twirpx.com/ Там вроде есть.
Там нету,искал
-
1 час назад, NelloN06 сказал:
У кого есть электронная версия книги Щербина,Матусевич "Органическая химия"?
Очень нужна,если у вас есть можете отправить пожалуйста
-
У кого есть электронная версия книги Щербина,Матусевич "Органическая химия"?
-
Можете помочь с данными реакциями
CaCl2+NH3=
Mn(NO3)2+NH3=
K2CO3+NH3=
MgSO4+NH3=
Al(NO3)3+NH3=
ZnSO4+NH3=
HNO3+NH3=
И можете пожалуйста осадки и газы тоже указать
-
Только что, Paul_S сказал:
(ΔH3-ΔH4)*3
Почему на 3 умножаем?
-
21 минуту назад, NelloN06 сказал:
Можете помочь
-
-
Только что, aversun сказал:
FeBr3 + Ag2SO4 => Fe2(SO4)3 + AgCl
Вы имели в виду AgBr?
-
Можете помочь с первой реакцией ,остальное сам сделаю
-
-
12 часов назад, M_GM сказал:
Это удивительно, как ты столько насчитал
10*3=30
8*4=32 или не так?
-
Только что, chemister2010 сказал:
Видимо в расчетах. У меня получилось:
3H2S + 8HNO3 = 3H2SO4 + 8NO + 4H2O
Там же в правой части 30H,а в левой 32H
-
2 часа назад, M_GM сказал:
Это конечно неверно. Никаких ионов водорода добавлять нельзя,
хотя бы потому, что Fe(OH)2 их не потерпит
К тому же в схеме реакции Fe(OH)2 + NO2 --> Fe(NO3)3 + NO + H2O;
нет слева источников ионов водорода, нет слева кислоты.
По алгоритму:
1) Ионная схема: Fe(OH)2 + NO2 --> Fe(3+) + 3NO3(-) + NO + H2O; тут только один сильный электролит
2) Полуреакции - меняют степени окисления железо и азот
Для железа: Fe(OH)2 - е(-) --> Fe(3+) + 2OH(-)
гидроксид-ионы частицы, которые могут образовываться в изначально нейтральной средеС азотом придется писать две полуреакции, поскольку он превращается и в NO, и в NO3(-)
NO2 --> NO
В кислой среде были протоны, они связывали кислород(-2) в воду.
В нейтральной среде кислород связывается водой по схеме O(-2) + H2O = 2OH(-):
NO2 + H2O + 2е(-) --> NO + 2OH(-)
NO2 --> NO3(-) здесь наоборот, слева не хватает кислорода. Откуда взять?
Среда нейтральная, значит опять только из воды,
которая может отдать кислород по схеме: H2O = O(-2) + 2H(+):
Получаем такую полуреакцию:
NO2 + H2O -е(-) --> NO3(-) + 2H(+)
3) ЗАПИСЫВАЕМ ВСЕ ПОЛУРЕАКЦИИ ВМЕСТЕ И ДУМАЕМ что с этим богатством делать:
Fe(OH)2 + NO2 --> Fe(NO3(3) + NO + H2O;
Fe(OH)2 - е(-) --> Fe(3+) + 2OH(-)
NO2 + H2O -е(-) --> NO3(-) + 2H(+)
NO2 + H2O + 2е(-) --> NO + 2OH(-)
Учитывая, что на один ион железа должно получаться три нитрат-иона, я для второй полуреакции поставлю коэф-т 3, и посчитаю общее число отданых электронов:
Fe(OH)2 + NO2 --> Fe(NO3(3) + NO + H2O;
Fe(OH)2 - е(-) --> Fe(3+) + 2OH(-) | 1
NO2 + H2O -е(-) --> NO3(-) + 2H(+) | 3 - 4е(-)
NO2 + H2O + 2е(-) --> NO + 2OH(-)
Тогда для баланса число отданных = числу принятых для треьей полуреакции надо поставить коэф-т 2
Fe(OH)2 + NO2 --> Fe(NO3(3) + NO + H2O;
Fe(OH)2 - е(-) = Fe(3+) + 2OH(-) | 1 - восст-ль
NO2 + H2O -е(-) = NO3(-) + 2H(+) | 3 - 4е(-) - восст-ль
NO2 + H2O + 2е(-) = NO + 2OH(-) | 2 + 4е(-) - окислитель
4) Суммарное ионное - складываем левые и правые части с учетом коэф-тов:
Fe(OH)2 + 3NO2 + 3H2O -е(-) - 3е(-) + 2NO2 + 2H2O + 4е(-) =
= Fe(3+) + 3NO3(-) + 2NO + 4OH(-) + 2OH(-) + 6H(+)Находим подобные сокращаем электроны, учитываем, что OH(-) + H(+) дают воду:
Fe(OH)2 + 5NO2 + 5H2O = Fe(3+) + 3NO3(-) + 2NO + 6H2O
Видим, что можно еще сократить по 5H2O в слева и справа:
Fe(OH)2 + 5NO2 = Fe(3+) + 3NO3(-) + 2NO + H2O
- и получаем сокращенное ионное уравнение!

5) - пишем молекулярное:
Fe(OH)2 + 5NO2 = Fe(NO3)3 + 2NO + H2O;
Fe(OH)2 - е(-) = Fe(3+) + 2OH(-) | 1 - восст-ль
NO2 + H2O -е(-) = NO3(-) + 2H(+) | 3 - 4е(-) - восст-ль
NO2 + H2O + 2е(-) = NO + 2OH(-) | 2 + 4е(-) - окислитель
-------------------------------------------------------------------------------------
Fe(OH)2 + 5NO2 = Fe(3+) + 3NO3(-) + 2NO + H2O
6) окончательно проверяем баланс.

Можешь сказать где у меня ошибка.
H2S+H(+)+NO3(-)=2H(+)+SO4(2-)+NO+H2O
1)H2S+4H2O-8e=SO4(2-)+10H(+) *3
2)NO3(-)+4H(+)+3e=NO+2H2O *8
И в конце выходит такое уравнение
3H2S+8HNO3+2H(+)=3H2SO4+8NO+4H20
То есть два атома водорода лишние,а так ответ правильный.Где я допустил ошибку??
-
15 минут назад, M_GM сказал:
Это конечно неверно. Никаких ионов водорода добавлять нельзя,
хотя бы потому, что Fe(OH)2 их не потерпит
К тому же в схеме реакции Fe(OH)2 + NO2 --> Fe(NO3)3 + NO + H2O;
нет слева источников ионов водорода, нет слева кислоты.
По алгоритму:
1) Ионная схема: Fe(OH)2 + NO2 --> Fe(3+) + 3NO3(-) + NO + H2O; тут только один сильный электролит
2) Полуреакции - меняют степени окисления железо и азот
Для железа: Fe(OH)2 - е(-) --> Fe(3+) + 2OH(-)
гидроксид-ионы частицы, которые могут образовываться в изначально нейтральной средеС азотом придется писать две полуреакции, поскольку он превращается и в NO, и в NO3(-)
NO2 --> NO
В кислой среде были протоны, они связывали кислород(-2) в воду.
В нейтральной среде кислород связывается водой по схеме O(-2) + H2O = 2OH(-):
NO2 + H2O + 2е(-) --> NO + 2OH(-)
NO2 --> NO3(-) здесь наоборот, слева не хватает кислорода. Откуда взять?
Среда нейтральная, значит опять только из воды,
которая может отдать кислород по схеме: H2O = O(-2) + 2H(+):
Получаем такую полуреакцию:
NO2 + H2O -е(-) --> NO3(-) + 2H(+)
3) ЗАПИСЫВАЕМ ВСЕ ПОЛУРЕАКЦИИ ВМЕСТЕ И ДУМАЕМ что с этим богатством делать:
Fe(OH)2 + NO2 --> Fe(NO3(3) + NO + H2O;
Fe(OH)2 - е(-) --> Fe(3+) + 2OH(-)
NO2 + H2O -е(-) --> NO3(-) + 2H(+)
NO2 + H2O + 2е(-) --> NO + 2OH(-)
Учитывая, что на один ион железа должно получаться три нитрат-иона, я для второй полуреакции поставлю коэф-т 3, и посчитаю общее число отданых электронов:
Fe(OH)2 + NO2 --> Fe(NO3(3) + NO + H2O;
Fe(OH)2 - е(-) --> Fe(3+) + 2OH(-) | 1
NO2 + H2O -е(-) --> NO3(-) + 2H(+) | 3 - 4е(-)
NO2 + H2O + 2е(-) --> NO + 2OH(-)
Тогда для баланса число отданных = числу принятых для треьей полуреакции надо поставить коэф-т 2
Fe(OH)2 + NO2 --> Fe(NO3(3) + NO + H2O;
Fe(OH)2 - е(-) = Fe(3+) + 2OH(-) | 1 - восст-ль
NO2 + H2O -е(-) = NO3(-) + 2H(+) | 3 - 4е(-) - восст-ль
NO2 + H2O + 2е(-) = NO + 2OH(-) | 2 + 4е(-) - окислитель
4) Суммарное ионное - складываем левые и правые части с учетом коэф-тов:
Fe(OH)2 + 3NO2 + 3H2O -е(-) - 3е(-) + 2NO2 + 2H2O + 4е(-) =
= Fe(3+) + 3NO3(-) + 2NO + 4OH(-) + 2OH(-) + 6H(+)Находим подобные сокращаем электроны, учитываем, что OH(-) + H(+) дают воду:
Fe(OH)2 + 5NO2 + 5H2O = Fe(3+) + 3NO3(-) + 2NO + 6H2O
Видим, что можно еще сократить по 5H2O в слева и справа:
Fe(OH)2 + 5NO2 = Fe(3+) + 3NO3(-) + 2NO + H2O
- и получаем сокращенное ионное уравнение!

5) - пишем молекулярное:
Fe(OH)2 + 5NO2 = Fe(NO3)3 + 2NO + H2O;
Fe(OH)2 - е(-) = Fe(3+) + 2OH(-) | 1 - восст-ль
NO2 + H2O -е(-) = NO3(-) + 2H(+) | 3 - 4е(-) - восст-ль
NO2 + H2O + 2е(-) = NO + 2OH(-) | 2 + 4е(-) - окислитель
-------------------------------------------------------------------------------------
Fe(OH)2 + 5NO2 = Fe(3+) + 3NO3(-) + 2NO + H2O
6) окончательно проверяем баланс.

Огромное тебе спасибо, не знаю чтобы я без тебя делал
-
Только что, M_GM сказал:
Вам даны схемы реакций протекающих в растворе. Вещества указаны, поэтому добавлять в левую часть вы можете только молекулы воды
Схема NaOCl + KI + H2SO4--> I2 + NaCl + K2SO4 + H2O
Алгоритм следующий:
1) Записываете все вещества с учетом их электролитической диссоциации (черновик)
(сильные электролиты - в виде ионов, слабые, осадки, газы - в виде молекул)
Na(+) + OCl(-) + K(+)+ I(-) + 2H(+) + SO4(2-)--> I2 + Na(+) +Cl(-) + 2K(+) + SO4(2-) + H2O
И вы видите в левой части ионы H(+) - ничего придумывать не надо, в левой части должны быть по мере необходимости только H(+) или вода
2) Пишем уравнения полуреакций.
Ищите элементы, которые меняют степень окисления и выписываете ионы или молекулы их содержащие:
OCl(-) --> Cl(-)
Надо превратить эту запись в уравнение полуреакции, прежде всего уравнять атомы,
хлор уравнен, надо уравнять кислород. Кислород(-2) в этой реакции переходит в воду H2O
для этого и нужны два иона H(+):
OCl(-) + 2H(+) --> Cl(-) + H2O
Атомы уравнены, надо уравнять заряды - считаем суммарный заряд ионов слева: 1+ и справа 1-
Заряды уравниваем электронами, добавляя их в левую часть:
OCl(-) + 2H(+) + 2е(-) --> Cl(-) + H2O - все, первая полуреакция составлена.
Меняется ст. окисления йода:
I(-) --> I2
Здесь только йод, уравниваем его атомы:
2I(-) --> I2 - слева 2-, справа 0, чтобы уравнять заряды надо отнять 2 электрона:
2I(-) - 2е(-) --> I2
Все две полуреакции составлены, они должны быть записаны рядом
NaOCl + KI + H2SO4--> I2 + NaCl + K2SO4 + H2O
OCl(-) + 2H(+) + 2е(-) = Cl(-) + H2O
2I(-) - 2е(-) = I2
3) Следующий этап - определяем коэф-ты электронного баланса, чтобы число отданных электронов было равно числу принятых. Но здесь они и так равны, значит коэф=ты электронного баланса 1:1 :
NaOCl + KI + H2SO4--> I2 + NaCl + K2SO4 + H2O
OCl(-) + 2H(+) + 2е(-)= Cl(-) + H2O | 1
2I(-) - 2е(-) = I2 | 1
ЕГЭ еще требует указать окислитель - восстановитель.
Окислитель принимает электроны, восстановитель отдает - подписываем:
NaOCl + KI + H2SO4--> I2 + NaCl + K2SO4 + H2O
OCl(-) + 2H(+) + 2е(-)= Cl(-) + H2O | 1; окислитель
2I(-) - 2е(-) = I2 | 1; вост-ль
4) Получаем ионное уравнение
Подводим черту, складываем полуреакции, умножая их на коэф-ты баланса (здесь умножать легко
 )
)
NaOCl + KI + H2SO4--> I2 + NaCl + K2SO4 + H2O
OCl(-) + 2H(+) + 2е(-)= Cl(-) + H2O | 1; окислитель
2I(-) - 2е(-) = I2 | 1; вост-ль
------------------------------------------
OCl(-) + 2I(-) + 2H(+) = Cl(-) + I2 + H2O - электроны при этом сокращаются,
иногда можно сократить еще какие-нибудь частицы,
одинаковые и в правой и в левой части. Но тут сразу получили краткое ионное уравнение.5) Предпоследний этап - по ионному уравнению расставляем коэффициенты в молекулярном:
OCl(-) + 2I(-) + 2H(+) = Cl(-) + I2 + H2O
NaOCl + 2KI + H2SO4--> NaCl + I2 + K2SO4 + H2O
При этом у нас оставались не задействанными ионы 2K(+) и SO4(2-) - объединяем их в K2SO4
6) Последний этап: еще раз проверяем, все ли уравнено и вместо --> пишем знак равенства:
На чистовике это должно смотреться так:
NaOCl + 2KI + H2SO4 = NaCl + I2 + K2SO4 + H2O
OCl(-) + 2H(+) + 2е(-)= Cl(-) + H2O | 1; окислитель
2I(-) - 2е(-) = I2 | 1; вост-ль
------------------------------------------
OCl(-) + 2I(-) + 2H(+) = Cl(-) + I2 + H2O
Уф-ф!
 (легче 10 сделать, чем 1 объяснить)
(легче 10 сделать, чем 1 объяснить)
Спасибо большое?
-
-
Только что, M_GM сказал:
Тут нету химии))
Спасибо, у меня тоже такой ответ получился
Ты поднял мою уверенность
Только что, M_GM сказал:показывай, как решал, что так получилось
Не могу показать ,файл превышает размер
-
-
14 минут назад, M_GM сказал:
Так покажи как ты решал, и можно будет сказать, есть ли ошибки и где.
У меня, признаюсь, получился третий ответ
Я понял свою ошибку.Я в конце написал 0,272=66,6-111х/153,6-219х и сделал ошибку
Только что, NelloN06 сказал:Я понял свою ошибку.Я в конце написал 0,272=66,6-111х/153,6-219х и сделал ошибку
То есть я делил массу соли на массу раствора.Ваще не могу понять эти кристаллогидраты
-
-
Оксид кальция, полученный при прокаливании 60 г карбоната кальция, растворен в строго необходимом ко личестве 36,5% -ной соляной кислоты. Полученный раствор охлажден до 0°С. При этом выпал шестиводный гидрат соли. Насыщенный раствор при указанной температуре содержит 27,2% кристаллогидрата. Вычислите массу выпавших кристаллов.
У меня вышло 105.69г и я уверен в своем решений ,но с ответом не сходится( Не могли бы вы сказать какой здесь ответ
-
Ааа, то есть нам дали моль соляной кислоты чтобы мы потом в дальнейшем посмотрели который из них будет в недостатоке?
Только что, M_GM сказал:Как нашел?
Я правильно сказал?
-
Только что, NelloN06 сказал:
-
Только что, M_GM сказал:
Физика, 6 класс.
Физика в 7 классе начинается))


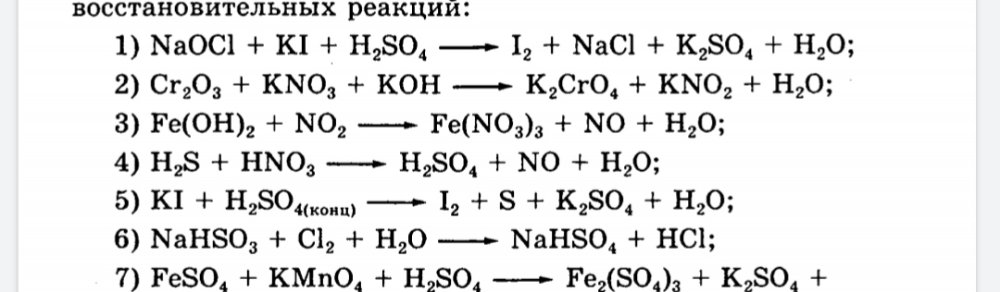

Логарифм числа
в Решение заданий
Опубликовано
Есть число 9,483*10^-7
Как найти его логарифм?