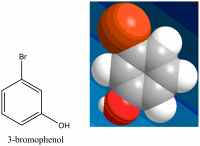
-
Постов
128 -
Зарегистрирован
-
Посещение
Весь контент Pitman
-
Судя по стоимости самого вещества доступен этот метод будет только состоятельным челам. А про технологию надумки есть, все манипуляции под наркозом, один бронх и половину легкого используем для естесвенного дыхания, другую половину через зонд подходящего размера омываем специальной жидкостью применяя капилярныетрубки ну или чет из имеющегося арсенала.
-
А еще интересно, слышал об таких соединениях из фторорганики (кровезаменители) и ведение иследований в области жидкостей для дыхания. Какие продвижения в этой области имеются на сегодняшний день? Меня интересует возможность применения этой жидкости для промывки легких от инородных частиц и профилактики силикоза и подобных заболеваний. Сам работаю в пыльной среде под землей и эта проблемма затрагивает меня лично.
-
Кто может привести примеры какие гормоны отвечают за те или иные реакции организма (смех, страх, сон, депрессия, повышение температуры, понижение температуры, и т. д.)
-
Да это я знаю, а дальнейшие превращения? Или может через промежуточные какие ни буть соединения.
-
Возможны ли реакции ДМСО (диметилсульфоксид) с образованием его перекисей? По типу циклической триперекиси ацетона.
-
:D Химия и технология бризантных взрывчатых веществ. 1981. Орлова Е.Ю Самораспространяющийся высокотемпературный синтез оксидов.
-
Спасибо за помощь. От серной кислоты сульфироваться не будет? Из всего я понял что смесь сначала надо промыть большим количеством воды, затем прокипятить с крепким раствором щелочи, отделив от щелочей взболтать с концентрированной серной кислотой не нагревая. Снова промыть водой и сушить выделенный толуол. Если что то забыл или не правильно поправьте.
-
Существует ли качественная реакция на толуол. Как его определить и извлечь из этого растворителя. Растворитель 646: толуол 50%, этанол 15%, бутилацетат (или амилацетат) 10%, бутанол 10%, этилцеллозольв 8%, ацетон 7%
-
Продаются в Москве. А) Стекло для перегонки: 1. Колба круглодонная термостойкая 1л, шлиф 29/32 2. Насадка Вюрца 29/32*14*14 3. Термометр от 0 до 350°С со шлифом 14 (для насадки Вюрца) 4. Капилляр на шлифе (14) для подачи воздуха и облегчения кипения при перегонке с вакуумом. 5. Прямой холодильник Либиха, длина 40см, шлифы 14 и 14 6. Холодильник обратный, шлифы стандартные - 29/32 и 14-й 7. Аллонж вакуумный, шлифы 14 и 14. Сам аллонж соединен с промывателем для откачиваемого газа, чтобы в случае агрессивности паров не повреждался вакуумный шланг.. 8. Аллонж простой, муфта 14-ая, керн 29/32.. 9. Колба-приёмник, 250мл, шлиф 14-й. 10. Насос водоструйный стеклянный, 3штуки (они без дефектов, просто запасные). Б) Другое стекло: 1. Колбы конические, объем 0.5л, 5 штук 2. Колба коническая 1л 3. стакан на 500мл, 2шт. 4. Цилиндры мерные: 250мл - 2шт, 100мл - 2шт. 5. Воронка делительная 250мл. 6. Воронка коническая стеклянная, диам. 6см, 2шт. 7. Воронка Бюхнера с резиновой обоймой диам.9см 8. Колба Бунзена 0.5л, горло под имеющуюся воронку Бюхнера. 9. 2 колбочки на 100мл со шлифом 29/32 В) Вспомогательная часть + мелочь: 1. Штативы, 2 штуки, оба старые, имеется ржавчина, но привести их в потребный вид при желании можно быстро. К штативам прилагается по 1-ой лапке с креплением (один штатив держит колбу, другой поддерживает холодильник). 2. Электроплитка одноконфорочная, регулируется нагрев, на максимуме выдаёт не меньше 400° (новая вообще до красна жарила).. 3. Ареометры для определения плотности азотной кислоты, 4 штуки (интервалы,г/мл: 1.300-1.360, 1.360-1.420, 1.420-1.480 и 1.480-1.540), плюс цилиндр на 50мл, в котором удобно юзать эти ареометры. 4. Чаша фарфоровая на 0.5л для выпаривания/кристаллизации водных р-ров солей, круглодонная, юзал редко, иногда бывает нужна.. 5. Термометры 5а) 0-50°С, цена деления 0.2°, шлиф 14 5б) 50-100°С, цена деления 0.2°, шлиф 14 5в) 100-150°С, цена деления 0.2°, шлиф 14 5г) 150-200°С, цена деления 0.2°, шлиф 14 5д) 50-100°С, цена деления 0.1°, без шлифа 7. Есть пара магнитных мешалок, ни разу не было нужды ими пользоваться 8. Стеклянные палочки 5штук, длина от 14 до 20см.. 9. Универсальная индикаторная бумага, 1упак. 10. Фильтровальная бумага "синяя лента", 1упак.. Старенькая, немецкая, но лучшая из всех, с которыми доводилось работать.. Все вопросы по ценам и уточнениям списка - в асю .
-
Была бы полезная функция автоматического расчета названия созданного соединения и отображения по номенклатуре. А также брутто формул, 3D молекул, атомного веса ну и всякой нужной химику информации.
-
Если реакция довольно интересная и доступная, то можно и на практике. Вообще я собираю рецепты получения веществ в домашних условиях из доступных ингредиентов. Стараюсь на практике это подтвердить. Кстати раз зацепили фотосинтез, какими лампами лучше пользоватся (накаливания, дуговыми ртутными, люминисцентными, криптоновыми), про волну 555 нм правда, только эта или спектр более широк. Вообще интересует влияние ионизирующего излучения на вещества и их соединения. Каков процент превращения кислорода в озон при облучении УФ (с условием охлаждения кислорода)?
-
dqin именно 555 откуда такая инфра? Про реакцию хлора и водорода очень интересно, но это известно из учебников по химии. Учитывая более углубленное изучение предмета, здешней аудитории я посмел предположить что информации будет куда больше и интересней. Но видимо я ошибся, сдешние научные деятели скупы на информацию, либо что самое страшное они просто проходили науку химию . Приходится все самому делать. Хех. :(
-
Ув. экспериментаторы в каких реакциях УФ (ультрафиолетовый свет) может ускорить, процесс? А в каких, например это обязательное условие, присуцтвие УФ. Например, УФ вызывает выпадение окиси серебра из его нитрата. Как вообще действует УФ на органические и не органические соединения. Каково влияние его на предельные и не предельные углеводороды, на амиды и амины, на альдегиды и кетоны и т. д. Спасибо.
-
Мента боятся, ВВ не мутить. На одном форуме по тематике ВВ, там дядька из ФСБ есть и почти все это знают, однако не заморачиваются. Вы химики не переоценивайте свою роль, кому надо тот и так узнает какие в-ва и как надо смешать, чтоб получилась выбухивка. Saaw парень конечно провокатор и ко мне на страничку личных данных заглядывал. Никто ни кого не принуждает давать ту инфру которую просят менты провокаторы и пиротехники любители. Вас же не просят изготовить и продать запрещенные препараты и соединения. Информация сама по себе законна, но реализация этой информации на деле это уже уголовка.
-
Ю. В. Карякин, И.И. Ангелов «Чистые химические вещества», М., 1974 Получение серебра (стр.330) Из сплавов, содержащих Ag, Cu, Pb, Sn, As, Zn и др. Метод основан на растворении сплава в HNO3 с последующим осаждением AgCl и восстановлением соли до металла. 3Ag+ 4HNO3 = 3AgNO3 + NO↑ + 2H2O Сплав растворяют в 13-16% HNO3, раствор разбавляют водой и выдерживают, при этом осаждаются Au, SnO2, Sb2O3 и др. После отстаивания смесь фильтруют через двойной или тройной фильтр в большой стакан и осаждают AgCl соляной кислотой (пл.1,12) (не NaCl !), взятой в небольшом избытке. Жидкость с осадком нагревают, при этом посторонние металлы растворяются в образовавшейся царской водке (при использовании NaCl в осадке вместе с AgCl могут быть PbCl2, BiOCl, SbOCl). Осевшую соль AgCl отфильтровывают и повторно кипятят с 10% HCl (ч.д.а.). Затем осадок промывают горячей водой декантацией до исчезновения кислой реакции и до отрицательной реакции на Cu+2 промывных вод [K4[Fe(CN)6] не должен давать красно-бурого осадка]. Далее AgCl восстанавливают Zn или формальдегидом: 2AgCl + Zn = 2Ag↓ + ZnCl2 2AgCl + HCHO + 3NaOH = 2Ag↓ + 2NaCl + HCOONa + 2H2O Размешивают 500 г влажного AgCl в 500 мл горячей воды. Полученную жидкую кашицу переносят в фарфоровый стакан, снабженный механической мешалкой, приливают (под тягой) раствор 300 г NaOH в 750 мл воды и при 35 – 400С вводят при непрерывном перемешивании 250 г 40% формальдегида. Смесь перемешивают 2-3 ч, добавляют еще 200 мл формальдегида и постепенно в течение 2 ч повышают температуру до 55-700С. Выпавший осадок серебра отсасывают на воронке Бюхнера, промывают 1 л горячей дистилированой воды, затем 500 мл 2%-ной H2SO4, 500 мл 2%-ного NH4OH и, наконец, горячей дистилированой водой до удаления Clˉ. Промытый металл сушат при 40-500С. Выход 100%.
-
Можно и нужно. 1. Перекрывает доступ кислорода. 2. Охлаждает пары горючки до температуры ниже температуры самовосплменения бензина. Другой вопрос как пользоватся таким огнетушителем. Если направить струю углекислоты на горящее ведро с бензином, если не загаснет сразу то может произойти выплескивание жидкости с последующим увеличением очага загорания. Отсюда и последствия.
-
d35945 Получение водорода действием щелочи на алюминий. Водород, получаемый данным методом, обладает высокой чистотой. Листовой алюминий или проволоку нарезают небольшими кусочками и помещают в аппарат Киппа, в который заливают 10–15-процентный раствор щелочи. Можно воспользоваться амальгамированным алюминием (при воздействии на алюминий раствора хлорида ртути), который легко вступает в реакцию не только со щелочью, но и нпосредственно с водой. Реакцию удобнее проводить в колбе Вюрца, приливая к алюминию по каплям воду из капельной воронки. Если же реакцию проводить в аппарате Киппа, то алюминий постепенно расходуется, так как амальгамированный алюминий вступает в реакцию с парами воды. Вобще расчитывай по этой формуле приблизительное количество компонентов. Используй емкость покрепче чем аппарат Киппа, желательно из нержавеющей стали. 2Аl + 2NaOH + 6Н2О = 2Na[Al(OH)4] + ЗН2 А вас химики хреновы совета просят а не дискусировать-пиздеть, зубов боятся в рот не давать. У чела своя голова есть на плечах, и в школе он учился, наверняка знает о горючести и взрывоопасности водорода. А вы!!! Ты шо, та это стремно, та побереги стекла, тьфу блин маразм.
-
Из батареек можно выделить так 1. Активную массу измельчаешь, идешь за город разжигаешь костер и прокаливаешь порошок в какой-то емкости, хлориды аммония достаточно летучи, они испаряются. Попутно можно выжечь графит при легком продувании воздуха через раскаленный сабж (порошок становится из черного, темно коричневого цвета). 2. Растворяешь полученный порошок в серной кислоте, желательно конечно до полного растворения (нагревание ускорит реакцию). Если же есть мусор, то фильтруешь раствор (он должен быть розового цвета). 3. Осадить MnSO4щелочью. 4. Отфильтровать Mn(OH)2, сушишь и прокаливаешь на газовой горелке. Вот и все у тебя сравнительно чистый MnO. Способ рабочий сам так делал. Не используй соляную кислоту выделяется хлор и его оксиды (ЯДОВИТО!!!)
-
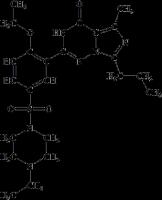
2-[2-Ethoxy-5-(4-ethyl-piperazine-1-sulfonyl)-phenyl]-5-methyl-7-propyl-3H-imidazo[5,1-f][1,2,4]triazin-4-one синтез из веществ смотри выше. Дома нереально это получить, эсли конечно ты не суперголовастый химик миллионер. Лучше купи таблетки Levitra скушай одну штуку и иди к своей подружке стояк смачный обезбечен. P. S. Родителей подружки не должно быть дома!!!
-
Хранить жидкие и твердые эфиры азотной кислоты в чистом виде, без стабилизации и флегматизации не рекомендуется. В связи с низкой устойчивостью соединений. Взрывчатые свойства сравни сам. Нитроглицерин: Расширение в бомбе Трауцля, мл - 550 Скорость детонации, м/с жидкого нитроглицерина - 1100-2000 при испытании в стальной трубке диам. 25мм - 8000-8500 Обьем газообразных продуктов взрыва, л/кг - 716 Теплота взрыва, кДж/кг - 6163 Этиленгликольдинитрат:Расширение в бомбе Трауцля, мл - 650 Скорость детонации, м/с жидкого этиленгликольдинитрата - 1100-2000 при испытании в стальной трубке диам. 25мм - 8300 Обьем газообразных продуктов взрыва, л/кг - 737 Теплота взрыва, кДж/кг - 6606 Этиленгликольдинитрат имеет нулевой кислородный баланс и по значению потенциальной энергии превосходит нитроглицерин примерно на 7%. Источник: Е. Ю. Орлова "Химия и технология бризантных взрывчатых веществ". -Л "Химия" 1981г.
-
Собственно это один из правильных ответов. При тушении горящих веществ температура горения которых превышает 20000С не только металлов но и кремния например, происходит термолиз воды в результате вода преврвщается из тушашего соединения в окислитель. Попутно выделяется водород образуя взрывоопасные смеси с воздухом. Еще металлы нельзя тушить углекислотой и галоген соединениями типа тетрахлорметан и т. д.
-
Точнее ЕС50 (концентрация ингибирующая 50% ферментов) концентрация препарата приводящего к 50% подавлению действия фермента. Например в анестезии это концентрация препарата в плазме крови которая ингибирует 50% ферментов и вызывает сон у 50% пациентов. Вроде Я так понимаю. Вобще через поисковик много всякого барахла, а определение ЕС50 нету.
-
Почитал немного про кавитацию и вот что подумал: а может ли использоватся эта кавитация для инициирования детонации жидких взрывчатых веществ? Вот рисунок приблизительно показывающий ход мыслей. Можно использовать пьезоэллементы для создания кавитации в ЖВВ и их детонации.