
As1d
-
Постов
204 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные As1d
-
-
Есть идеи по способу покрытия им стального куска?
-
Да, нужно сделать покрытие, скорее всего попробуем покрыть небольшой кусок стали. Тефлон действительно хорош, но, как Вы и сказали - хрен им что покроешь.
-
Добрый день, химики! Подскажите пожалуйста недорогой полимер, способный выдерживать горячие(около 100С) растворы щелочей(точнее сульфида натрия, стабилизированного крепкой щелочью). Сам с подбором "пластиков" столкнулся впервые, пока смотрю в сторону полиформальдегида, хотя не уверен, держит ли он горячую крепкую щелочь. Я довольно слаб в вопресе высокомолекулярных соединений, поэтому прошу Вашей помощи, заранее спасибо!
-
А чем распространенные тигли не устраивают? НЕметаллические. Чем не угождает обычный фарфоровый глазированный тигель? Или корундовый? Я сплавлял в фарфоровом тигле оксид свинца с содой, оксидом кремния и добавкой оксида меди ради интереса(зеленое стекло, кстати, получал). Расчетная температура плавления = 730, я сплавлял и выдерживал час при 830. Потом открыл печку(830С было), достал щипцами тигель и вылил стекло на стальную пластину. Тигель в норме, правда но он уже был прокален однажды и ко дну прилип тонкий слой стекла.
А если будете впервые прокаливать, то остановите нагрев на 200 и 400 градусах минут на 10-15, чтобы ваш тигель не треснул.
-
Ух, спасибо, пойду искать!
-
Сабж. Ищу литературу по электролитическому получению металлов, по процессу электролиза, по тонкостям сего процесса. Интересуют в основном растворы, водные и неводные. Кстати, есть у кого опыт по электролизу в неводных средах? ДМСО, ДМФА и др. Если есть такие, в личку, пожалуйста.
-
Все правильно, я хотел бы просто больше узнать о возможностях, максимальном количестве способов восстановления карбоксильной группы. Просто помню, что это сложно - восстановить карбоксильную группу в метиленовую, но знаю, что можно. Если есть еще какие-нибудь возможные варианты, даже варианты промежуточных стадий - прошу привести, вы мне очень поможете.
-
Схема это хорошо, но мне не понятно, какие реактивы при этом используются, механизмы и т.д. Распишите пожалуйста подробно, для чайников. А если знаете где об этом толково написано, так я и сам прочитаю, дайте только ссылочку.
-
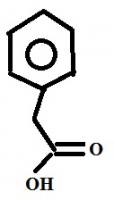
Уважаемые химики, подскажите, возможно ли восстановление карбоксильной группы в метильную в ароматическом соединении?(карбоксильная группа изолирована от бензольного кольца) например в таком соединении:
-
Доброе время суток, ищу литературу по производству соды методом Сольве, заранее благодарен всем откликнувшимся.
p.s. статьи по типу википедии не предлагать.
-
чтобы нитрат аммония не взорвался его надо разбавить. песком, например, солью, и т.д.
Чтобы нитрат аммония из хоз. мага взорвался дома, нужно сильно постараться.
-
Представьте себе стеклянную кастрюлю с плотно притертой, шлифованной крышкой. В кастрюле стоит пароварка(на которой манты делают или котлеты раогревают). На дне кастрюли - серная кислота, что жаждой мучается, а на
пароварке стоит различная посуда с осушаемыми веществами. Серка тянет влагу из воздуха, забирая тем самым пары воды над осушаемым веществом, равновесие нарушается, вода не возвращается обратно в ваше в-во.
-
Ю. В. Карякин, И. И. Ангелов - Чистые химические вещества. Посмотрите там, книга в свободном виде в сети
-
-
/Offtop
Отключи FriendlyFire :cc:
-
Всем спасибо за ответы!
-
Видимо, придеться признать правоту препода :bh:
-
Да в моем вопросе ничего особо серьезного, просто препод по физ. химии действует мне на нервы своими гениальными шуточками, а в последнем тесте я был несогласен с тем, что вода обязательно гомогенна и решил доказать, что среди песка, молока и жемчуга можно тоже выбрать то, что может быть гомогенным. Кстати, почему молоко не является гомогенной системой? Обезжиренное к примеру.
-
Это возможно в невесомости на орбитальной станции.
Второе противоречит первому. Это уже будет не жемчуг.
Блин, да как так? А что скажете насчет воды? Обычная вода содержит в себе растворенные газы, и мы называем ее водой, но стоит воду прокипятить и газы улетучатся, но это все равно будет вода. Почему же жемчуг становится нежемчугом?
Собствено вся попаболь заключается в вопросе по физ. химии, где требовалось выбрать гомогенную систему из песка, молока, воды и жемчуга. Понятно, что идеальная вода может быть гомогенной, но она так же может быть и гетеро. Еще вопрос: если чистейший песок поместить в идеальный вакуум, его можно будет рассмотреть как гомогенную систему?
-
Я читал, что жемчуг, как гетерогенная система, содержит в кристалической решетке карбоната воду, которая и делает систему гетерогенной. Так же я слышал, что в специальных лабораториях есть возможность вырастить идеальный кристалл, без деффектов. Собственно вопрос: учитывая вышесказанное, можно ли вырастить жемчуг, хоть мельчайшую крупицу, так, чтобы систему можно было считать гомогенной? Это не вопрос целесообразности, вопрос возможности и принципа, так спрошу еще раз, возможно ли?
-
Gall, согласен, однако я помню, как все стало просто, когда мы в 11м классе прошли этот кратенький курс квантовой, ой, а на 1м курсе то какая лафа была)
-
Активность определяется (не)заполненностью внешней оболочки. Валентность - количество электронов, необходимых для ее полного заполнения (или опустошения). В зависимости от того, что легче - дополнить оболочку или опустошить, элемент более склонен быть окислителем или восстановителем соответственно.
В первом приближении стоит учитывать еще и радиус атома, иначе: Be и Сa к примеру, должны иметь весьма и весьма схожие свойства.
Что касается заполнения оболочек - выучите правило Кличковского, или банальную квантовую механику, я предпочитаю второй вариант.
n - Главное квантовое число, = номеру периода, характерезует энергию(соответственно n>=1 всегда) и номер уровня валентных орбиталей(все орбитали, которые ниже по энергии чем n заполнены полностью).
l - Орбитальное кв. ч. Принимает значения от 0 до n-1, характеризует вид электронного облака: l=0, - S; l=1, - P; l=2 - D; l=3 - F; l=4 - G; и так далее.
Ml -Магнитное кв. ч. Принимает все значения от -l до l через еденицу.(К примеру l=2, Ml принимает значения -2, -1, 0, 1, 2) Характеризует расположение орбитале в пространстве.
Ms -Спиновое кв. ч. Принимает два значения: +1/2 и -1/2. Характеризует "правостороннее или левостороннее вращение" электрона вокруг собственной оси.
Система(атом) стремится к минимуму энергии, что обуславливает ее устойчивость.
На одной орбирали максимум два электрона, поличество орбиталей в подуровне = 2l+1 или количеству значений Ml
Энергия атомной орбитали = n+l, а электроны заполняют орбитали с максимальным значением спинового числа, и сначала заполняют подуровни с минимальной энергией.
Добавим принцип Паули - на одной атомной орбитали не могут находится два электрона с одинаковым набором всех квантовых чисел.
Отметим, что атом устойчивей, если его валентный подуровень заполнен полностью или на половину, а устойчивый потомучто таким образом достигается минимум энергии.
Примеры:
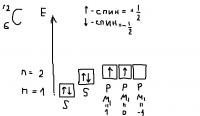
С - углерод, n=2; l=0,1; 6 электронов. Значит, что с n=1 оболочка полностью заполнена, l=0, значит S орбиталь причем одна(2*0+1) Заполнение идет сл. образом: nlnum, где num - кол-во электронов.
1S2 - n=1, l=0, num=2, так как на 1 орбитали макс. 2 электрона с противоположными спинами, а орбиталь заполнена полнотсью. Больше на n=1 подуровне орбиталей нет.(l=0)
n=2, l=0,1 = S и P орбитали. Причем если S(l=0, 2l+1=1) всего одна, то количество P орбиталей целых 3. (l=1, 2l+1 = 3) На одну орбиталь поместится 2 электрона, а на 3 орбитали - 6 электронов, тогда заполняем. 2S2 2P2 . И поместилось бы шесть, да только электронов не хватило. Поэтому на двух P орбиталях по 1 электрону, т.к. орбитали заполняются сначала с максимальным спином, то есть на двух орбиталях по 1 электрону со спинами +1/2.
Sc : 4 период, 21 электрон. n=4, l=0,1,2,3 - означает, что на уровне=4 возможны S, P, D и F орбитали.
Орбитали с n<4 полностью заполнены, кроме 3D орбитали. Почему? Очень просто: посчитаем энергию 3D орбитали = n+l(n=3,D орбиталь значит l=2) = 3+2 = 5. Посчитаем энергию 4P орбитали = 4+1=5! Тоже пять. Если энергия двух орбиталей совпадает, то сначало будет заполнятся орбиталь с наименьшим n, то есть 3D. Таким образом после орбитали 4S(энергия = 4+0 = 4) будет заполнятся 3D, и только после нее 4P. - Заполняем.
1S22S22P63S23P64S23D1(помним, что P орбиталей всегда три, и все три в сумме умещают 6 электронов) Нетрудно догадаться, что D орбиталей аж целых 5, и поместятся на них 10 электронов, но у нас кончились электроны для заполнения, поэтому на одной D орбитали всего один электрон. Вы спросите, а как же F орбиталь? Есть же значение l=3! F орбиталь присутствует, только на ней электронов нет, как присутствует и 4P и 4D орбиталь, просто мы их не пишем, ведь на них сейчас нет электронов.
Кстати, если электронов нехватает, чтобы заполнить полностью D орбитали, но хотябы один электрон заполнил D, то эти D орбитали так же являются валентными(c F та же история). То есть у скандия максимальная валентность будет складываться из суммы электронов на 4S и 3D орбиталях и составит 2+1 = 3.
Cr n=4 l=0,1,2,3 24 электрона
нижние оболочки как и у Sc:
1S22S22P63S23P6 в сумме потрачено 18 электронов на их заполнение, осталось 6 электронов. Заполняем валентный уровень n=4.
4S2(дальше, как мы уже знаем, идет 3D) 3D4. И тут происходит нечто. Как я уже говорил, атом стремится к минимуму энергии, а достичь этого можно, если бы был еще один электрон на 3D орбитали. Тогда на 3D орбитали было бы 5 электронов, а это как-раз половина. Поэтому в атоме хрома один электрон с 4S орбитали переходит на 3D орбиталь. Окончательно орбитали хрома выглядят так:
1S22S22P63S23P64S13D5
Максимальная валентность хрома = 1+5 = 6
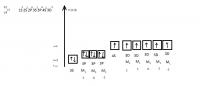
Такие вот хитрые атомы. У F элементов есть еще некоторые тонкости, но обычно для школы и начала первого курса хватает S-D элементов.
Вот еще картинки заполнения рассмотренных атомов.
-
На моих двадцать третьего, если только до ваших 7 утра
 , в 8 по вашему времени у меня начнется экзамен, поэтому мне остается только еще раз вас поблагодарить!
, в 8 по вашему времени у меня начнется экзамен, поэтому мне остается только еще раз вас поблагодарить! -
Но быть может - всё проще, и автор, ничтоже сумняшеся, имеет в виду именно банально-формальную реакцию Вюрца с образованием того продукта, который Вы изначально нарисовали.

Да уж, кто его пойми! Спасибо за объяснения! Если вы еще не собираетесь спать, я задам еще парочку вопросов

Предложите механизм жидкофазного окисления метил(нео-пентил)метана при 150 ºС кислородом воздуха.
CH3-CH2-CH2-C(CH3)3 он, правильно? я не знаю эту тему, но могу предположить, что катализируя процесс каким-нибудь волшебством, мы оторвем гомолитически водородик от одного из вторичных атомов, который очень удачно встретится с молекулой кислорода, образует ОН радикал. Который позже зацепится за радикал алкана. Люблю предлагать механизмы на форуме, здесь за неправильные ответы не ругают


Подбор термостойкого полимера
в Полимеры
Опубликовано
Посмотрел свойства в интернете, вроде подходит. А у него еще какие-нибудь названия есть? Потому что как реактив он не числится, думал в русхиме глянуть а там нет такого.