
KRAB-XIMIK
-
Постов
4567 -
Зарегистрирован
-
Посещение
-
Победитель дней
3
Тип контента
Профили
Форумы
События
Сообщения, опубликованные KRAB-XIMIK
-
-
Из бензола можно получить гексахлорциклогексан с помощью силы хлора и света
-
А может просто добавить кислоты?
-
-
В принтере скоро закончатся краски. Каттридж можно, конечно, заправить, всё для этого есть. Но вот принтеру от этого не легче: он, наверное, запрограммирован так, что он не следит за уровнем чернил(ну как бы следит, но одновременно и нет). Понимаете, если в каттридже закончится краска, то принтер скажет, что там краски нет, а если его заправить, то принтер всё равно скажет, что краски нет и не будет печатать. Как можно сделать так, чтобы принтеру казалось, что каттридж полный?
-
 1
1
-
-
-
3-метилбутен-1
2,3-диметилбутен-1
-
-
V(HI)=VM*w(HI)*Vр-ра*pр-ра/M(HI)
-
Где Вы такое нашли? Скажите номер элемента
-
Не в пэйнте же:o
А Вы эти формулы изображали при помощи какой-то программы?
-
CH3-CH=C(C2H5)-CH(CH3)-CH2-CH(CH3)-CH2-CH3
Я старался
-
1) добавьте растворимую соль серебра. Выпадет белый осадок - сульфат, жёлтоватый - фосфат, ничего - нитрат.
2) К сожалению, фосфат и карбонат серебра жёлтого цвета. Сначала добавляем какую-нибудь сильную кислоту. Где выделится газ - там карбонат калия. Затем к двум оставшимся склянкам добавляем растворимую соль серебра - где жёлтый осадок, там фосфат натрия.
3) Снова серебро. Теперь белый осадок - хлорид калия.
4) И ещё раз серебро.
-
NO+KClO+KOH->KNO3+KCl+H2O
N+2-3e=N+5|2|
Cl++2e=Cl-|3|
2NO+3KClO+2KOH=2KNO3+3KCl+H2O
-
диэтилбутиламин - (C2H5)2(C3H7)N
Вы рисуете быстрее, чем я пишу :(
-
втор-бутилцианид - CH3-CH2-CH(CN)-CH3
-
Выплывает в осадок?согласен, только правильно ли ее осадком называть? :D она наверху должна плавать.

-
Ну вот, говорил же, что не уверен...Определенно не то. Я бы назвал так 3-метил-4-фенил-2-хлорбутан
2,6-дибромциклогексанон
1,2,4-тригидроксибензол
гексанон
-
NH4NO3+H2O=NH3+H2O+HNO3
[NH4NO3]=[HNO3]=10-pH
m(NH4NO3)=V*[NH4NO3]*M(NH4NO3)
-
V=m/ρ
Массовая доля глюкозы у Вас дана - 40%
-
Используя постоянство массовой доли сульфата калия, находите, сколько граммов содержится в 400 г раствора, насыщенного при 80 С:
21,4/(100+21,4)=х/400
Пусть выпало у моль сульфата калия, тогда масса оставшегося сульфата равна (х-M(K2SO4)*y) г
Масса раствора равна 400-M(K2SO4)*y
Используем постоянство массовой доли сульфата при 20 градусах:
11,1/(100+11,1)=(х-M(K2SO4)*y)/(400-M(K2SO4)*y)
Вот и всё. Находите у, а затем и массу осадка
Можно даже заменить M(K2SO4)*y на m(осадка) и не находить у
-
Качественный состав: бутен-2 и 2-метилпропен
-
(3-хлорпропил)бензол
1-бром-3-нитро-4-хлорбензол
2,5-дибромциклогексанон
3-метилциклогексанол
бензол-1,24-триол
5-гидроксипентанон-2
4-гидрокси-5-фторпентановая кислота
Я не очень уверен
-
что такое Кв и Ка?
-
В последнем проще написать +NaOH1) С2Н4 + HСl --> C2H5Cl
2) C2H5Cl + H2O --> C2H5OH + HCl
3) C2H5OH + CuO --> C2H4O (или CH3-CHO) + H2O + Cu
4) C2H4O + Ag2O --> C2H4O2 (или CH3-COOH) + 2Ag
5) CH3-COOH + Na2CO3 --> CH3-COONa + CO2 + H2O
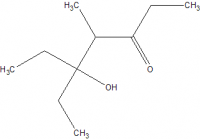
превращения органика
в Решение заданий
Опубликовано