
docanton
-
Постов
145 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные docanton
-
-
рассчитайте навеску технического нитрита натрия, содержащего 90% NaNO2, необходимую для приготовления 250 мл 0,05 н раствора для перманганатометрического определения
рассчитайте навеску технического нитрита натрия, содержащего 90% NaNO2, необходимую для приготовления 250 мл 0,05 н раствора для перманганатометрического определения
Я так решил, но не уверен
Расчёт навески
В основе перманганатометрического определения натрия нитрита лежит ОВР:
2KMnO4 + 8H2SO4 + 10NaNO2 = 10NO2 + 8H2O + 2MnSO4 + 5Na2SO4 + K2SO4.
Для приготовления 0,05 н раствора натрия нитрита объёмом 250 мл понадобилось бы:
C = m / М • V р-ра
m = C • M • Vр-ра = 0,05 моль/л • 68,996 г/моль • 0,25 л = 0,86245 г (при 100% содержании вещества в навеске вещества). Следовательно, 10% - это примеси. Находим массу примесей:
0,86245 г – 100%
Х г – 10% Х = 10% • 0,86245 г / 100% = 0,086245 г
Масса чистого препарата: 0,86245 г – 0,086245 г = 0,776205 г
-
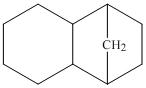
Напишите структурную формулу 1,7-диэтилбицикло[4,1,1]октана.
И название углеводорода, прикреплён к сообщению
-
Вроде как уравнялось
4MnO2 + 6KBiO3 + 12H2SO4 = 4HMnO4 + 3Bi2(SO4)3 + 3K2SO4 + 10H2O
-
Вот и я о том же. Не может диоксид марганца втупать в реакцию. Такое задание
-
Какие продукты реакции получаться?
MnO2 + KBiO3 + H2SO4 =
-
K2MnO4 + H2S + H2O =
Спецы, помогите, мне думается, что K2MnO4 вообще не может вступать в реакцию, а образуется только в результате реакции.
Не могу по нескольким вариантам уравнений расставить коэффициенты. Может быть эта реакция вообще не существует?
-
Начал было решать задачу, но ответ не получается и даже не стал ответ вписывать. Помогите дорешить
Задача
Сделайте заключение о качестве таблеток нитроксолина, если при спектрофотометрическом определении точную массу порошка растертых таблеток, равную 0,3975 г, поместили в мерную колбу вместимостью 250 мл, прибавили 20 мл воды, перемешали, довели 0,2 моль/л раствором натра едкого до метки и профильтровали. 2 мл фильтрата развели до 250 мл 0,2 моль/л раствором натра едкого. Оптическая плотность полученного раствора (Dх), измеренная при 450 нм в кювете с толщиной слоя 10 мм составила 0,405. Оптическая плотность раствора рабочего стандартного образца (Dо), содержащего 0,000003 г нитроксолина в 1 мл составила 0,395. Средняя масса одной таблетки 0,195.Согласно требованиям НД содержание нитроксолина в одной таблетке должно быть от 0,04625 до 0,05375 г.
Неужели никто не сможет до конца решить?
-
Вес 20 капель раствора нитроглицерина по нестандартному каплемеру 0,25 г.
Сколько капель нужно отпустить, если в рецепте выписано 0,7 мл; 20 капель?
Спасибо
-
Где можно скачать архив журнала "вопросы биологической медицинской и фармацевтической химии"? Ссылку можете показать?
-
Провести кислотный гидролиз стрептоцида в присутствии кислоты серной средней крепкости.
-
Начал было решать задачу, но ответ не получается и даже не стал ответ вписывать. Помогите дорешить
Задача
Сделайте заключение о качестве таблеток нитроксолина, если при спектрофотометрическом определении точную массу порошка растертых таблеток, равную 0,3975 г, поместили в мерную колбу вместимостью 250 мл, прибавили 20 мл воды, перемешали, довели 0,2 моль/л раствором натра едкого до метки и профильтровали. 2 мл фильтрата развели до 250 мл 0,2 моль/л раствором натра едкого. Оптическая плотность полученного раствора (Dх), измеренная при 450 нм в кювете с толщиной слоя 10 мм составила 0,405. Оптическая плотность раствора рабочего стандартного образца (Dо), содержащего 0,000003 г нитроксолина в 1 мл составила 0,395. Средняя масса одной таблетки 0,195.Согласно требованиям НД содержание нитроксолина в одной таблетке должно быть от 0,04625 до 0,05375 г.
Концентрация нитроксолина в исходном растворе:
Cисх = а / V = 0,3975 г/ 250 мл = 0,00159 г/мл
Концентрация раствора нитроксолина, приготовленного из исходного раствора и подвергнутого далее с целью определения оптической плотности:
С = Сисх • Vисх / V =0,00159 г/мл • 2 мл / 250 мл = 0,00001772 г/мл = 1,772 • 10-5 г/мл
В растворе с прозрачным растворителем свет поглощается растворённым веществом. Для таких растворов справедлив закон Бугера-Ламберта-Бера:
I = I0 • exp (-K•C•l)
I – интенсивность прошедшего света;
I0 – интенсивность падающего света;
K – коэффициент поглощения. Не зависит от концентрации, но зависит от длины волны и температуры;
l-толщина слоя в кювете (дм);
В данном случае в качестве прозрачного растворителя выступает смесь натрия гидроксида и воды, а свет поглощается растворённым веществом – нитроксолином.
После преобразования уравнения закона Бугера-Ламберта-Бера получаем:
Ln(I0/I) = K•C•l = D
D-оптическая плотность;
K=Е- удельный показатели поглощения
D=E•C•L
Выразим величину Е из этого уравнения:
Е = D / (C•L)
Соответственно, из данных по исследованию стандартного образца:
Е = 0,395 / (1,772•10-5 • 1) • 100 = 222,912
Концентрация нитроксолина в растворе, приготовленном из стандартного образца и подвергнутого далее исследованию с целью определения оптической плотности:
Сиссл = Dиссл / (Е • l) =0,405 / (222,912 • 1 дм) = 1,82 • 10-3 г/ 100 мл =
= 1,82•10-5 г/мл
Концентрация нитроксолина в растворе, приготовленном из исследуемого образца:
С = Сисл * Vиссл / Vстанд = 1,82•10-5 г/мл • 250 / 5 = 9,1•10-5 г/мл
Используем формулу
А1 - оптическая плотность испытуемого раствора;
А0 - оптическая плотность раствора стандартного образца;
С0 - концентрация раствора стандартного образца, г/мл;
b – разведение;
q - средняя масса таблетки, г;
а - навеска, г.
Содержание вещества в одной таблетке в граммах (х), считая на сред-нюю массу таблетки:
Х = A1 * C0 * b * q / А0 * а
Данная формула применима при использовании стандартного образца.
Х = 0,405 • 0,000003 г/мл • 9,1•10-5 г/мл • 0,195 г / 0,395 • 0,3975 г =
=
-
При таких расчётах получается
0,12 = Х в квадрате / 0,55 в квадрате
Итого 0,19 моль/л А должен быть ответ 0,11 моль/л
-
А что здесь считать за Х
-
Там непонятно, как формула с Х составляется
-
Определите равновесные концентрации водорода в реакции
2HJ = H2 + J2
Если исходная концентрация HJ = 0,55 моль/л, а константа равновесия равна 0,12.
Помгите
-
спасибо Вам, Ефим
-
Не могли бы Вы помочь написать реакции синтеза из диэтилового эфира малоновой кислоты янтарную кислоту и аллилуксусную кислоту
-
Спасибо за помощь
-
Допишите уравнение реакции
K2S2O8 + K2SO3 + H2O = KHSO4 +
Разбавление водой
в Решение заданий
Опубликовано
Какое количество воды очищенной необходимо добавить к 2 кг кальция
хлорида, чтобы получился 50% раствор. Рассчитайте массу и объем полученного концентрата.