
anddor
-
Постов
232 -
Зарегистрирован
-
Посещение
-
Победитель дней
1
Тип контента
Профили
Форумы
События
Сообщения, опубликованные anddor
-
-
14.09.2023 в 14:51, HE KOT сказал:
Приветствую. А что посоветуете для людей, которые пока что не встречался с этой темой?

Для начала можно это:
Л.А. Казицына, Н.Б. Куплетская. Применение УФ-, ИК-, ЯМР- и масс-спектроскопии в органической химии.
-
-
-
12.09.2023 в 02:27, Дмитрий А сказал:
Недавно я заполучил немного сульфата свинца и теперь думаю как можно перевести его в раствор. Первое что мне пришло в голову - растворение в конц. растворе Na2SO4/K2SO4. Возможно ли это?
Щёлочью можно в гидроксокомплекс перевести.
-
11.09.2023 в 19:15, BritishPetroleum сказал:
Реакция идёт, когда энергия Гиббса реакции меньше нуля. Вот и смотрите, какой у неё будет знак во всех этих случаях.
-
11.09.2023 в 18:57, Олег1977 сказал:
Здравствуйте! У меня такой вопрос. Я во время стирки вещей, точнее во время последнего полоскания добавляю в воду немного спиртового уксуса, чтобы смягчить вещи и лучше выполоскать средство для стирки. Подскажите, пожалуйста, после того, как вещи высохнут, что происходит с частичками уксуса, оставшимися на одежде? Уксус улетучивается или так и остаётся на вещах?
Откройте бутылку с уксусом и понюхайте. Сразу получите ответ на свой вопрос.
-
01.09.2023 в 14:53, Razor8 сказал:
по альдегиду, если кто еще за темой следит- изыскания, медь, серебро, катализаторы это все очень интересно, но в коммерческом плане пока лидирует окисление хромпиком в кислой среде. выхода 60-70% все быстро и удобно.
куда деть оксид хрома зеленый не ясно.
кстати, а почему кислый раствор зеленый? там же оксид должен стать сульфатом?
Образуются разные аква- и сульфатокомплексы типа [Cr(H2O)4SO4]+. Они и придают раствору зелёный цвет.
-
 1
1
-
-
19.08.2023 в 21:58, Zenith сказал:
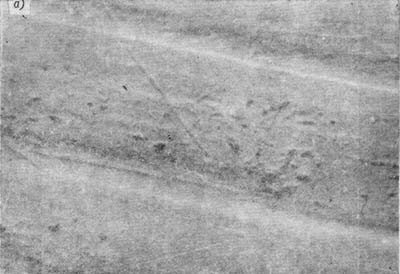
В микроскоп посмотрите металлографический.
При прокатке/вытяжке на поверхности будут характерные полосы.
-
 1
1
-
-
23.08.2023 в 02:50, Romix сказал:
Не только они, ну и многие другие, есть что-нибудь селективнее??
Сульфид натрия даёт с гидроксокомплексом цинка белый осадок сульфида цинка. Гидроксокомплекс алюминия с сульфидом не реагирует.
-
21.08.2023 в 04:04, Romix сказал:
Спирту добавь. Сульфат кальция очень неохотно выпадает из раствора, особенно если растворы разбавленные. В присутствии спирта осадок образуется намного быстрее.
-
22.08.2023 в 11:49, Елена199031 сказал:
Здравствуйте! Подскажите пожалуйста. Наушник блютуз постирался при 60 градусах 45 мин. Может ли что-то вредное или ядовитое, аллергенное попасть на постиранные вещи. Спасибо заранее
Не может. Используйте спокойно и забудьте об этом случае.
-
 1
1
-
-
29.07.2023 в 17:25, birg77out сказал:
ИИ
Спектрофотометр дал следующие результаты цветности: 0,912; 0,815; 0,622
Для анализа сходимости чисел и определения промаха в данном случае можно использовать метод среднего значения и стандартного отклонения.
Метод среднего значения:
Найдите среднее значение, сложив все числа и разделив их на их количество:
среднее = (0.912 + 0.815 + 0.622) / 3
Вычислите разницу каждого числа относительно этого среднего значения:
разница1 = 0.912 - среднее разница2 = 0.815 - среднее разница3 = 0.622 - среднее
Рассчитайте сумму квадратов разниц:
сумма квадратов разниц = разница1^2 + разница2^2 + разница3^2
Нормализуйте сумму квадратов разниц, разделив ее на количество чисел:
нормализованная сумма квадратов разниц = сумма квадратов разниц / 3
Вычислите среднеквадратичное отклонение (стандартное отклонение):
стандартное отклонение = корень из (нормализованная сумма квадратов разниц)
Теперь мы можем провести сравнение чисел:
Если какое-либо число существенно отличается от среднего значения (больше или меньше его на несколько стандартных отклонений), то это число можно считать промахом.
Если все числа примерно равны друг другу и находятся на расстоянии менее одного стандартного отклонения от среднего значения, то можно считать, что они сходятся.
Далее выведу результаты вычислений...
Спектрофотометр дал следующие результаты цветности: 0,912; 0,815; 0,622
Вычислим среднее значение цветности:
среднее = (0.912 + 0.815 + 0.622) / 3 = 0.783
Вычислим разницу каждого числа относительно среднего значения:
разница1 = 0.912 - 0.783 = 0.129 разница2 = 0.815 - 0.783 = 0.032 разница3 = 0.622 - 0.783 = -0.161
Рассчитаем сумму квадратов разниц:
сумма квадратов разниц = (0.129)^2 + (0.032)^2 + (-0.161)^2 = 0.036
Нормализуем сумму квадратов разниц, разделив ее на количество чисел:
нормализованная сумма квадратов разниц = 0.036 / 3 = 0.012
Вычислим стандартное отклонение:
стандартное отклонение = √(0.012) ≈ 0.1096
Теперь проанализируем сходимость чисел и определим промах:
Все числа находятся на расстоянии менее одного стандартного отклонения от среднего значения (0.912, 0.815 и 0.622), поэтому можно считать их сходящимися.
Нет числа, которое существенно отличается от среднего значения, поэтому нет промаха.
Таким образом, числа 0.912, 0.815 и 0.622 сходятся и не содержат промаха.
Хуйня какая-то.
У ИИ явные проблемы с математикой. 0.912 и 0.622 отличаются от среднего на величину, бОльшую, чем стандартное отклонение.
На самом деле для выявления промаха надо использовать Q-критерий.
-
09.08.2023 в 12:42, Александра98 сказал:
Метод Кейдаля
Вы даже название метода правильно написать не можете. Очевидно, методику анализа Вы не читали. Начните с этого.
-
 1
1
-
-
09.08.2023 в 07:06, ЕленаАвдеева сказал:
Почитайте внимательнее методику. Глюкозу там используют не только для титрования, но и как раствор калибровочный, вместо пробы.
Так калибровочный раствор, как и пробу, из бюретки надо добавлять по каплям! Это Вы прочитайте внимательно методику: Принцип метода заключается в том, что щелочной раствор железосинеродистого калия (установленной концентрации) оттитровывают испытуемым раствором, содержащим сахар, в присутствии метиленовой сини в качестве индикатора.
-
08.08.2023 в 13:11, ЕленаАвдеева сказал:
Почему раствор не становится голубым? Смешиваю глюкозу, 10% гидроксид натрия и железосинеродистый калий, кипячу в течение 1 минуты (по методике), добавляю метиленовый голубой. Что я делаю не так?
Так глюкозу по каплям из бюретки добавлять надо до обесцвечивания МС, а Вы её сразу бухнули в избытке. Вот индикатор и не синеет, поскольку глюкозой восстанавливается.
-
06.08.2023 в 16:28, shah82 сказал:
вольфрам там может быть, но студенистый осадок это скорее всего кремнекислота
"эхо войны" только если лемурийцев с протоайнами, хреновина эта где-то на полметра под землей лежит
Неразорвавшиеся снаряды времён ВОВ и на большей глубине находят.
В осадочных отложениях природного железа металлического быть не может. Разве что метеорит. Так что Ваш образец явно рукотворный.
-
-
04.08.2023 в 02:47, shah82 сказал:
добыт в речных отложениях, встречается там в виде линз до 1 м и толщиной 25 см
плотность ок 3
черта рыжая или он царапает фарфор, он неоднородный очень, мне показалось в начале, что там куски гвоздей попадаются, но техногенным он быть не может... скорее всего
магнитится хорошо, после дробления можно разделить на магнитную и немагнитную фракции, хотя визуально они мало отличимы
спайность кмк в таком случае вообще неприменимое понятие,
немагнитная фракция содержит тяжелый серо-стальной шлих, возможна платина или МПГ
кремнекислота окрашенная гематитом разве будет вымываться при кислотной обработке? и да - сам гематит из неё не вытравится?
зы. фотки не получаются, камера сдохла
С плотностью 3 это даже на гематит не тянет, не говоря уж о МПГ. Скорее всего какой-нибудь бурый железняк или железистый кварцит.
А может таки и шлак от какого-нибудь древнего железоплавильного производства. Больно уж маленькие линзы.
Где нашли образец территориально?
-
29.07.2023 в 17:29, birg77out сказал:
ИИ
Цвет шарика в стеклянных электродах
Цвет шарика в стеклянных электродах, таких как те, что используются в лампах накаливания, обычно имеет функциональное значение.
Синий цвет шарика
Синий цвет обусловлен присутствием ионов меди. Ионы меди в процессе окисления придают синий цвет, в результате активного сопротивления окислению и сильной связи с кислородом.
Прозрачный шарик в стеклянных электродах
Электроды с прозрачным шариком обычно не содержат добавок и служат для передачи электричества без всякого влияния на цвет излучения.
Применение различных цветов шариков
Оптический эффект. Различные цвета создают интересный оптический эффект при пропускании света. Синие шарики, например, могут создавать ощущение более "холодного" света.
Защита от ультрафиолета. Некоторые окрашенные материалы могут загораживать или поглощать определенные длины волн, такие как ультрафиолетовые лучи, что может быть полезно для защиты от ультрафиолета.
Функциональное использование. В некоторых случаях, цвет может служить для подсветки определенных областей или для обозначения определенного типа лампы.
Вывод
В ядре дело, что цвет шарика в стеклянных электродах существенно зависит от его использования и компонентов внутри него. Он может меняться в зависимости от выбранного вида использования и желаемого эффекта.
Цвет шариков в стеклянных электродах в химической лаборатории
В химической лаборатории стеклянные электроды используются в различных экспериментах и приборах, включая вольтметры и амперметры. Здесь цвет шарика в электроде также имеет значение.
Синий цвет шарика
В электролитических экспериментах, синий цвет шарика может использоваться для обозначения катода, т.е. электрода, к которому подключен отрицательный заряд. Обычно катод окрашивается в синий цвет для обозначения, что здесь происходит восстановление вещества.
Прозрачный шарик в электродах
Прозрачные шарики на электродах обычно используются для обозначения анода, или электрода, к которому подключена положительная заряд. Здесь происходит процесс окисления вещества.
Различные цвета шариков
Основная цель использования различных цветов шариков в химической лаборатории - это упростить идентификацию и использование электродов, а также помочь в изучении различных химических процессов.
Вывод
Цвет шарика в электроде является важными индикатором в различных химических экспериментах. Он помогает идентифицировать, какой электрод является катодом, а какой - анодом, а также дает понять, какие процессы происходят на каждом из них. В конечном счете, это делает процесс обучения и экспериментирования намного проще и понятнее.
Какие, нахуй, ионы меди?!
Какие, в пизду, катоды?!
Достал ты своим ЖПТ!
Синим шарик делают в современных стеклянных электродах для того, чтоб он заметнее был. Так меньше вероятность раскокать его о дно стаканчика.
-
01.08.2023 в 13:57, shah82 сказал:
странного вида шлакоподобный минерал, предположительно продукт естественного (хотя не факт) обжига пирита, содержит много металлического железа,
если растворять в 35% серной кислоте с добавкой азотки, при нагревании - выделяется водород и образуется много сульфата железа
но если полученный после первого протравливания (травил до прекращения выделения газа) остаток снова залить той же смесью, то газ таки немного выделяется (уже не водород), и в растворе образуется мелкодисперсное красно-коричневое вещество, отфильтровал через синюю ленту, в соляной и азотной по отдельности - не растворяется,
в царской водке при нагревании медленно растворяется, сначала чернеет с поверхности
при прибавлении к взвеси гидрохлорида гидразина - тоже чернеет
попытка сплавить с содой (думал вдруг там платиноиды какие вымылись из минерала) привела к получению опять таки чёрных прочных кусочков, но металла там нет, плавил кислородно-пропановой горелкой
результат плавки залил царской водкой (отмыв от соды разумеется), растворяется вяло, после частичного испарения кислот остался желтый студенистый остаток, который плохо растворяется в воде (лежит как сопля на дне, и за час кипячения с водой может процентов на 20 разошелся
зы. нормальная аналитика недоступна сейчас, но вдрук у кого какие мысли будут
А фото "минерала" выложить слабо? Здесь экстрасенсов нет.
Как установили, что выделяется именно водород?
Фарфоровые тигли стойки к действию серняги и азотки, так что кремнекислота однозначно из "минерала".
-
05.09.2022 в 18:18, Romix сказал:
Да в яицах действительно многo Серы которую они легко отдают серебру из соединений при контакте.
Даже с маинеза настаящего столовое серебро чернеет...В купе едут мама с дочкой и едят вареные яйца.
— А яйца, доченька, никогда на серебро не клади — серебро от яиц чернеет, — наставляет дочку мама.
"Век живи — век учись, — подумал ехавший на верхней полке поручик Ржевский и переложил серебряный портсигар из кармана брюк в нагрудный карман.
-
07.07.2023 в 09:13, SeaDoo сказал:
Собственно из изумрудно-зеленого стал сине-фиолетовым, в течении 2х дней (в хим. стакане 25мл)... Что произошло?
Зелёный [Cr(H2O)4Cl2]+, который вы получили при растворении в воде зелёного же [Cr(H2O)4Cl2]Cl*2H2O, при стоянии в растворе переходит в сине-фиолетовый [Cr(H2O)6]3+. Гидратная изомерия.
-
 1
1
-
 1
1
-
 1
1
-
-
30.06.2023 в 15:51, Малюгин Фёдор сказал:
Здравствуйте, хотел бы попросить помощи в вопросе об основности.
Так, раз HF - слабая кислота, то F-- сильное основание. В группе сила оснований галогенид - ионов падает. Это объясняется тем, что радиус атомов галогенов увеличивается , но при этом перекрывание связи обеспечивается в большей мере лишь 1s1 электроном водорода, т.е. важна плотность заряда, распределенного на внешнем уровне: у фтора она максимальна, следовательно, связь будет наиболее крепкой, далее плотность электронного облака снижается , тогда и снижается энергия связи ?
В водном растворе фторид-ион - слабое основание. Его pKb составляет 10.2. То есть константа основности фторид-ина примерно на 7 порядков меньше константы кислотности плавиковой кислоты и примерно на столько же меньше константы основности, например, карбонат-иона.
-
 1
1
-
-
27.06.2023 в 17:33, Romix сказал:
Я делаю так, в Фейсбуке когда присылаешь фотку кому то она сжимается до требований форума Химиков.
Скачиваешь с чата и заливаешь сюда.Раньше в Paint проге резал их.
Аааа, не заметил, у вас мало комментов на форуме, не получится вам через фейсбук.
Я через вотсап сжимаю так же. Сжалось до 203 кб. ХЗ как оставшиеся лишними три кб убрать. Форум живёт до сих пор в прошлом веке?
Вопрос с подвохом. Будет ли серная кислота реагировать с хлоридами меди? CuCl2 , CuCl
в Неорганическая химия
Опубликовано
Хлоридный комплекс меди(I) бесцветный. Жёлтый цвет может придавать примесь комплекса меди(II).