Поиск
Показаны результаты для тегов 'расчет'.
Найдено 10 результатов
-
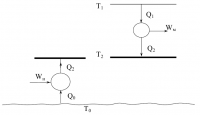
Помогите, пожалуйста! (Если что-то не понятно по условиям, то смело спрашивайте=)) Q2 = 100 кДж, Т0 = 298 К, Т1 = 800 К, Т2 = 370 К, Кн = 0,4, Км = 0,5 Рассматривается два случая подвода теплоты Q2 потребителю при температуре Т2 . В первом случае Q2 подводится путем передачи теплоты от окружающей среды (Т0) с помощью теплового насоса. Во втором случае теплота подводится от топливной энергоустановки с температурой Т1 (см. рис.). Для теплового насоса коэффициент преобразования ϕ работы Wн в теплоту Q2 = ϕ*Wн, передаваемую потребителю при температуре Т2, равен ϕ = Кн*ϕТ, (0
-
Дано: адиабатическая система двух термостатов, соединенных между собой, переходит из состояния 1 (Ср, М1, Т10, М2, Т20) в стационарное состояние 2 (Ср, М1, М2, Т1 = Т2 = Т*). Рассчитать потери эксергии при переходе системы из состояния 1 в состояние 2. Для расчетов использовать уравнения баласнов энтропии и энтальпии. Все приведенные выше в обоих скобках величины даны. Плиз, помогите посчитать потери эксергии, ну или просто скажите, как это считать)
-
- эксергия
- потери эксергии
-
(и ещё 2 )
C тегом:
-
Дано: адиабатическая система двух термостатов, соединенных между собой, переходит из состояния 1 (Ср, М1, Т10, М2, Т20) в стационарное состояние 2 (Ср, М1, М2, Т1 = Т2 = Т*). Рассчитать потери эксергии при переходе системы из состояния 1 в состояние 2. Для расчетов использовать уравнения баласнов энтропии и энтальпии. Все приведенные выше в обоих скобках величины даны. Плиз, помогите посчитать потери эксергии, ну или просто скажите, как это считать)
-
- эксергия
- потери эксергии
-
(и ещё 1 )
C тегом:
-
Сама я в физ химии не очень от слова совсем, но мне нужно разобраться со следующей задачей: у меня идет реакция первого порядка, идет в изотермических, изобарных условиях, для нее известны для нескольких температур протекания реакции – константы скорости реакции (при 40С k=0,00267 ч-1, при 60С k=0,0058 ч-1, при 80С k=0,0384 ч-1). Каким образом на основании этих данных рассчитать энергию Гиббса, при этом, желательно, так, чтоб уравнения были не безумно заумными? Пока что то, на что натыкалась- жуткая теория, не имеющая к практике никакого отношения(
-
Доброго времени суток Посмотрите пожалуйтса туда ли я двигаюсь вообще правильно хоть что-то или нет (сам напутал и вас наверное запутаю спрашивайте пожалуйста если что не понятно) Необходимо расчитать сколько выделится тепла и какая будет конечная температура раствора в стандартных условиях 1 атм температура 298 К и при давлении 200 атм и температуре 353 К Есть водный однонормальный раствор солей NH4NO3+NaNO2 при взаимодействии солей в водном растворе происходит екзотермическая реакция, бурно проходить реакция начинает при температуре 60-80 0С (самоинециируэться) вобще реально реакция будет происходить в трубе на глубине 4000 тисячи метров и мне надо узнать на сколько прогреется растовр например обемом 20 или 500 л и тд по факту берется 1 моль нитрата амония 1 моль нитрита натрия и 4 моля воды NH4NO3+NaNO2=NaNo3+2H2O+N2 ↑ Ентальпия образования ΔН0298 NH4NO3 -365,7 кДж/моль ( для твердого вещества ) NaNO2 - 359 кДж/моль ( для твердого вещества ) NaNo3 -466,7 кДж/моль ( для твердого вещества ) H2O -258,8 кДж/моль ( для жидкости ) N2 0 кДж/моль ΔH = ∑(nΔH)продукты - ∑(nΔH)реагенты Тоесть ΔH = (-466,7+(2*-285,8)+0)-(-365,7+(-359))=313,6 кДж/моль Ктото мне говорил что для того чтобы узнать тампературу необходимо ентальпию образования разделить на ентропию образования ( но помоему это равноесная температура так опредиляеться ) А вот что делать далть с етим незнаю что где брать куда и как Для давления 200 атм и температуры 353 К насколько я понимаю необходимо пременить уравнения Ван дер Ваальса или Ван дер Ваальса если да то какое из них
- 2 ответа
-
- термохимия
- расчет
-
(и ещё 2 )
C тегом:
-
25 мл HCl реагирует с 20 мл 0.15н NaOH. Определите массу хлороводорода, содержащуюся в 200 мл исследуемого раствора. Сделайте расчет: а) через нормальность А.Р. по правилу пропорциональности б) через титр по определяемому компоненту- Т(NaOH/HCl)
-
Некоторое кол-во органического в-ва, содержащего N и О, сожгли в 26,88л кислорода н.у.Образов. 9г воды и смесь газов, которую пропустили через избыток р-на Ba(OH)2, в раз-те выпало 275,8 г осадка и осталось 10,08л газовой смеси с плотностью 1,31г/л. Формула в ва - ?? В принципе все понятно, но я не могу "разделить" в расчетах непрореагировавший кислород и азот, которые с гидроксид. не взаимодействуют. Помогите пожалуйста!
- 1 ответ
-
- задача;
- формула органического веществ
-
(и ещё 1 )
C тегом:
-
Помогите пожалуйста решить: Расчитать нормальность концентрированной серной кислоты, содержащей 65,5% H2SO4 (p=1,56 г/мл).
-
Бертолетова соль при нагревании разлагается на кислород и хлорид калия. Вычислить количественный состав бертолетовой соли и вывести ее формулу, если при разложении 1,02 г соли получено 0,62 г KCl. Подскажите пожалуйста как решить это?
- 1 ответ
-
- соль реакция
- расчет
-
(и ещё 1 )
C тегом: