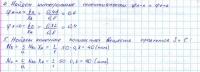neutron
Пользователи-
Постов
105 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Весь контент neutron
-
Спасибо большое, я все поняла. Молярную массу соли ртути надо было взять вдвое меньше, потому что в расчётах используется молекулярная масса эквивалентов. Но что получится в результате этой реакции: Hg(NO3)2 + CS(NH2)2 = ?
-
Помогите с задачей!! что-то пошло не так... (точка эквивалентности по графику = 9мл) задача и решение на фото спасибо за ответы
-
Саму задачу и ее решение Вы можете видеть внизу на фото. Смущает последнее действие, а именно, количество вещества получившихся продуктов S и C - по 40 моль. Наверное, количества получившихся веществ в реакции должно быть равно количеству вещества исходного реагента, у меня так не получается. Может такое быть? Как решить по-другому, чтобы было правильно? Может ошибка где - то в предыдущих действиях? Спасибо за внимание к моему вопросу и Вашим ответам!
-
а как Вы определили то, что тут две ОН-группы? И на ИК - спектре С=О группа определяется в области 1600см^-1?
-
проанализировав оба спектра, я нашел, что молекулярная масса вещества = 76, Молекула имеет ОН-группу, С-Н в sp3 и С=С (возможно) начал составлять брутто-формулу соединения:из 76 вычел 17(мол.масса группы ОН) = 59. т.к. масса углерода = 12, то максимальное число атомов углерода в молекуле 4. 4 * 12 = 48.для того чтобы найти массу водорода : 59 - 48 = 11, таким образом, брутто-формула имеет следующий вид: С4Н12О. Но такого соединения, по-моему, не существует. где я ошибся?
-
Интересует один из способов синтеза циклогексанона. Реакция окисления циклогексанола хроматом калия в кислой среде в присутствии уксусной кислоты: C6H12О + K2CrO4 + CH3COOH + H2SO4 = С6Н10О + K2SO4 + H2O + .... 1. Почему реакцию нужно проводить в кислой среде? И как среда вообще влияет на реакцию? 2. Есть ли какие-то побочные реакции? образование адипиновой кислоты? 3. Что будет, если заменить хромат калия на бихромат калия? 4. В методике указано, что нужно растворить хромат калия в уксусной кислоте при нагревании, а затем раствор охладить до 15°С. С какой целью это делают? 5. Также в методике указано, что раствор циклогексанола сначала надо смешать с толуолом и только потом добавлять при перемешивании в реакционную колбу. Для чего это делают? 6. После смешения всех реагентов температура реакционной смеси не должна превышать 60°С. Это связано с побочными реакциями? Большое спасибо за ответы.
-
Дали тест по органике. Я сомневаюсь в ответах. Кружком обведены ответы, которые, по - моему, правильные. Проверьте, пожалуйста. Спасибо. Тема: Азотсодержащие соединения. Посмотрите, пожалуйста. Очень нужно. Хотя бы частично
-
Спасибо. Все исправлю
-
В смысле? Я просто спросил, так решать или нет.
-
-
Получается так:2М*100мл/(V+100мл)=0.02М V=9900мл=9.9л. В ответах 0.97. Это я неправильно считаю?
-
Задача по теме комплексообразование. Помогите. Нашел концентрации ионов хлора и дальше не знаю, как решать. Решение на фото. Спасибо
-
в любом случае. В кислой среде будет окисляться до бензойной кислоты, а в нейтральной до бензальдегида? или реакция совсем не идет?
-
Методика: В трехгорлую колбу емкостью 150 мл, снабженную воздушным холодильником, капельной воронкой и термометром, помещают 19,9 мл ацетона и 9,92 мл бензальдегида. К смеси из капельной воронки прибавляют 2,5 мл. 10%-го водного раствора гидроксида натрия при постоянном перемешивании и охлаждении. Температура смеси 25-31°С. После прибавления всей щелочи смесь перемешивают 2 часа при температуре 20°С. Прибавляют разбавленную хлороводородную кислоту до кислой реакции.Два образовавшихся слоя разделяют на делительной воронке. Нижний водный слой экстрагируют толуолом. Толуольный раствор прибавляют к верхнему органическому слою. Органическую вытяжку промывают водой и сушат прокаленным MgSO4. Отгоняют толуол простой перегонкой с колбой Вюрца в интервале 260-262°С. Во время проведения синтеза у меня возникли вопросы: 1.Для чего прибавляют NaOH и почему при этом соблюдают определенную температуру и условия? 2.Почему перемешивать нужно при определенной температуре? 3.Зачем подкисляют среду? 4.Какие побочные реакции могут еще идти? 5.Можно ли оставлять бензалиденацетон в открытой склянке? СПАСИБО!!!
-
1. как действуют на бензиловый спирт такие окислители, как перманганат калия и азотная кислота? 2. при помощи каких реакций можно доказать наличие альдегидной группы в бензальдегиде? (реактив Толленса и гидроксид меди???) 3. почему приходится очищать бензальдегид от бензилового спирта не смотря на то, что окислитель взят в избытке? Уравнение реакции: 3C6H5-CH2-OH + K2Cr2O7 = 3C6H5CHO + 2KOH + Cr2O3 + H2O спасибо!
-
Какое вещество в недостатке? 3C6H5-CH2-OH + K2Cr2O7 = 3C6H5CHO + 2KOH + 2Cr2O3 + H2O
-
Укажите температуру плавления п-иодбензойной кислоты
-
-
И как же найти концентрацию сульфид ионов? Через константу равновесия никак, т.к. нет [HS-], и вряд ли [s2-]=[H+]=10^-2......
-
Помогите с задачами. В первой задаче получается неправильный ответ. А вторую, не знаю, как решить, подтолкните к решению. Спасибо!
-
-
ну да, спасибо
-
Спасибо, всё получилось. Только не понятно, как вы определили, что образуется раствор соли с концентрацией 0,1 моль/л?