-
Постов
764 -
Зарегистрирован
-
Посещение
-
Победитель дней
2
Тип контента
Профили
Форумы
События
Весь контент llinks
-
В сети полно рецептов - костлявую рыбу (типа карп, лещ, язь) нужно исколоть раствором лимонной кислоты, и оставить на сутки в холодильнике. Мол кости растворятся, и всё прекрасно, жарьте парьте на здоровье Экспериментировать мне что-то не хочется, какое будет мнение теоретиков? Или может кто-нибудь на практике пробовал?
-
Штука зелени - как раз стоимость похорон
-
Можно зеленым сделать Чтобы убрать пятно, надо вытащить хром, что не представляется возможным. Можно весь стол бихроматом выкрасить, хотя бы одноцветный будет
-
Всё же спасибо за ответы. / еще сульфат марганца 2+, но зеленой окраски почему-то с роданидом нет. / кстати, при работе с действительно опасными веществами противогаз нужен, на тягу рассчитывать нельзя - потому как электрик Уася...
-
Материал стола? Пластик, дерево?
-
Как говорим мы "обжегшись на молоке дуешь на воду" Только из-за того что в растворе присутствует роданид железа 3+, в качестве красящего агента, работать под тягой, в противогазе и перчатках
-
Вот я и спрашиваю, мало ли, какая-нибудь окислительно-восстановительная реакция, с Fe 2+ 3+, или подобная, и ага... На всякий случай.
-
Вроде да, роданиды не опасны, напрягла вот такая инфа >>> "В воде родан хорошо растворим, но быстро разлагается по уравнению: 3 (SCN)2 + 4 Н2O = 5 HCNS + Н2SO4 + HCN." Говорят цианистый калий на вкус приятный кисловато-сладкий?
-
В литературе есть данные, что роданистый водород в растворе распадается на серную и синильную. Вопрос: В растворе сульфатов и роданидов, слегка подкисленном, есть вероятность что образуется циановодород? Насколько велика опасность "дохимичиться"?
-
Очевидно автор задавая конкретный вопрос по ПР должен был указать конкретно какой именно силикат серебра его интересует, и, может быть, тогда...
-
В контексте о минералах, силикаты-минералы все нерастворимы, поскольку растворимый силикат, тем более редкого элемента, фактически не встречается. О минералах пост был.
-
Есть много разных дрожжевых грибков, соответственно разные брожения, возможно есть и дрожжи более продуктивно выделяющие винную кислоту. В любом случае винная кислота получается дрожжами из сахара или глюкозы, а виноград или другой материал как витамины для дрожжей, только на одном сахаре жизнь невозможна.
-
Возможно есть такой минерал, надо смотреть энциклопедию минералов. Если силикат безводный, то растворимость ничтожно мала.
-
Схватывание цемента - это рост кристаллогидратов, игольчатые кристаллы растут и тесно переплетаются. Реакция гидратации начинается с окислов, СаО и т.д присоединяют воду. Здесь же ничего не присоединяется, при обычных условиях смесь гидроокисей так и останется смесью, реакции между ними не произойдет, в сухой смеси то уж точно. Если же смесь замешать водой, то получившаяся каша очень долго останется кашей, схватывания не будет.
-
Для ускорения процесса растворения добавить в серную поваренной соли или еще и селитры, тогда быстрей растворится, особенно при нагревании А там дальше смотреть, что получилось.
-
Значит увеличу концентрацию солей по максимуму.
-
Бело-коричневые кристаллы, сульфаты - коричневый цвет наверное железо. Fe 2+ окислился до Fe 3+, образовалась основная соль Fe(OH)SO4, которая закристаллизовалась в двойную соль типа Fe(OH)SO4·(Fe,Zn)SO4·nH20. Если кристаллы косые призмы, то скорей всего так и есть. Но, в кислом растворе основная соль врядли бы образовалась, тогда могут выпасть железные квасцы, кристаллы октаэдры. По облику кристаллов (сингония) можно судить о химическом составе, ведь кристаллы крупные?
-
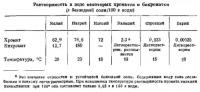
Я исходил из других данных, см. таблицу: (но, при любых данных, концентрация в разы превышает растворимое кол-во. Другие данные, см. таблицу: ( может он 'думает', в какой форме выпадать?
-
Требуется получить CaCrO4, в наличии есть CaCl2 и K2CrO4. Хромат кальция малорастворим, поэтому по обменной реакции при смешении насыщенных р-ов CaCrO4 должен бы выпасть в осадок - но этого не произошло, раствор прозрачный желтого цвета. Есть сообщения что в промышленности хромат кальция получают обменом CaCl2 и Na2CrO4. В данном случае нет разницы между калием и натрием. Почему хромат кальция не выпадает?
-
Карбамид в водном растворе постепенно переходит в карбонат аммония, делайте выводы.
-
За ответ спасибо, думаю... Воздуха нет в смеси, и выделения газа нет. Плотность стехиометрических веществ заметно меньше конечного продукта реакции. Масса постепенно твердеет из почти жидкого состояния, и именно по причине уменьшения объема становится пористой - значит если проводить в вакууме, то поры всё равно будут, безвоздушные, что ничего не меняет. Но запомню конечно, мало ли... PS: вакуумный насос можно сделать из ручного автомобильного - перевернуть сальник, и тд.- для опыта, с небольшим обьемом, сойдет наверное. В похожих случаях применяют и вибрацию, бетон например лучше схватывается.
-
Нужно создать постоянное давление на зону реакции, провести эксперимент. Сколько-нибудь серьезное оборудование приобретать нет смысла, потому-что не факт что эксперимент удастся. Суть - фосфатный материал, густая кашеобразная смесь, твердеет со значительным уменьшением объема, получается пористая масса, а желаемый конечный материал нужен монолитом. Можно предположить, что под постоянным давлением получится значительно более монолитная масса. Вопрос : Может быть есть какие-то простые технические приемы? Экспериментальный объем смеси небольшой, с пробку пластиковой бутыли. Может быть кто сталкивался с подобными проблемами?