
Dmitriy1990
-
Постов
592 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные Dmitriy1990
-
-
Всем доброго времени суток. Возник такой вопрос: можно ли избирательно восстановить кеталь непредельного кетона водородом, сохранив при этом двойную связь? Я встречал информацию только про тиокетали. Также не совсем понятно, что за превращения идут дальше (цепочки 7, 8), если после восстановления у нас остался алкен. До этого я прописал альдольную и кротоновую конденсации с получением соответствующих непредельных кетонов или альдегидов. Помогите, пожалуйста.
-
4 часа назад, Paul_K сказал:
Видимо, ожидается циклизация с образованием ТГФ.
1 час назад, yatcheh сказал:Я так скажу. Была у меня мысль получить 4-пирролидинилбутанол-1 реакцией 4-хлорбутанола-1 с пирролидином. Хрен там. Только тетрагидрофуран и получился.
Гидроксил - это не только нуклеофил, но и основание. SN2-реакция - довольно медленный процесс, а вот депротонирование гидроксила - очень быстрый. А последующая за этим циклизация - весьма энтропийно выгодный процесс. Внутримолекулярная SN2-реакция всегда выиграет у межмолекулярной по скорости. Поэтому при обработке 4-хлорбутанола-1 щёлочью получится тетрагидрофуран.
Большое спасибо за ответы.
-
Всем доброго времени суток. Возник вопрос со следующей реакцией Cl-(CH2)3-CH2-OH+NaOH. Я предполагаю стандартную реакцию SN2. Настораживает тот факт, что реакция дана в теме "Простые эфиры". Получение соответствующих простых эфиров из b-галогенспиртов хорошо описано в литературе. Однако информации по циклизации спиртов вроде предложенного я не нашел. Какая же реакция в итоге пойдет? Помогите, пожалуйста.
-
11 минуту назад, yatcheh сказал:
Почему не выдержит? Ничего ему не будет. Прокрасится, конечно, но не развалится, и не загорится.
Вот хлористый сульфурил на полиэтилен скверно действует, или олеум 60%-й.
Я просто знаю, что во всех практикумах не рекомендуют хранить 90% азотную кислоту в таре с полимерными пробками. А про действие на бумагу ничего не нашел. Понятно, что азотная кислота в такой концентрации ее разъест. Вопрос лишь в том, насколько бурно идет взаимодействие.
10 минут назад, Митя сказал:Фторопласт-4 можно отличить от полиэтилена по плавлению последнего. Не знаю, как себя ведут при нагревании другие фторопласты. Да и на ощупь они разные, фторопласт прям жирный.
Нет, пробка и заглушка на ощупь нежирные.
-
2 минуты назад, yatcheh сказал:
Жаль, что полиэтилен. Дымящей азотной кислоты, я считаю, он не выдержит(. Чтобы новую тему зря не создавать, не знаете, обычная бумага (газета) и полиэтилен, как к дымящей азотной кислоте относятся (воспламеняются или нет)?
-
49 минут назад, Ruslan_Sharipov сказал:
Толуол растворяет полиэтилен в горячем виде. А в холодном вроде бы нет.
Возможно и так. Изначально была надежда, что фторопласт).
-
2 часа назад, Леша гальваник сказал:
Походу, полиэтилен.
Вы про упаковку? В схожей бутылке хранится толуол, а он полиэтилен неплохо растворяет. Следовательно, и пробка с заглушкой пришли бы в негодность. Однако уже несколько лет бутылка стоит, и ничего.
-
-
-
1 час назад, yatcheh сказал:
В хорошо герметизированной упаковке - почему бы и нет? Только это должна быть действительно герметичная упаковка, а не пенициллинка с резиновой пробкой.
P.S. Кстати, что касается мути - возможно это примесь спирта гадит. Теоретически он должен сольват давать с хлоридом кальция, как и вода, но практически бывает такая коллоидная хрень.
При чём после перегонки в погоне того спирта - фиг целых хрен десятых, но муть визуально напрягает.
Большое спасибо за помощь. Спирта после обработки серной кислотой и хлоридом кальция действительно должно быть мало. В любом случае, практика покажет, годен полученный реактив для Гриньяра или негоден.
-
3 минуты назад, yatcheh сказал:
Вот и я думаю также. Разве что пытаться сделать реактив Гриньяра из бромэтана такого качества. Скажите, пожалуйста, возможно ли хранение бромэтана с диэтиловым эфиром на складе без холодильника (примерная температура 25 градусов по Цельсию)?
-
23 минуты назад, yatcheh сказал:
Вряд ли это сульфат кальция. В таких случаях помогает замена осушителя на свежий. Что там происходит - хз, это чистое колдунство

Повлиять может на запуск реакции, это всегда - рулетка, если реакция пойдёт, на выход не должно существенно повлиять.
Вот и я не могу понять, что происходит. Уже трижды пытался осушить хлористым кальцием (менял осушитель с каждой попыткой) - ничего не меняется. Надеюсь, если реакция Гриньяра с таким бромэтаном с ходу не пойдет, йод поможет. Что бы вы еще посоветовали сделать для уборки мути из реактива? Перегонка нерентабельна в связи с малым количеством продукта (13 граммов).
-
Всем доброго времени суток. Возникла такая проблема: после синтеза бромэтан, несмотря на осушку серной кислотой и хлористым кальцием, остался мутным. Возможно, муть обусловлена не влажностью, а сульфатом кальция? После обработки серной кислотой продукт был промыт раствором NaHCO3, затем дистиллированной водой. В данный момент осушивается в потенциальной таре для хранения хлористым кальцием. С момента начала осушки хлористым кальцием прошло около 2 часов? Если в дальнейшем бромэтан не станет кристально чистым, возможно ли его использование для приготовления этилмагнийбромида (реактив Гриньяра). Если эта муть обусловлена сульфатом кальция, то может ли он помешать данной реакции. Помогите, пожалуйста.
-
27 минут назад, Аль де Баран сказал:
Растворы получить нельзя, но суспензию или порошок первичных алкилмагнийгалогенидов в среде УВ-растворителей (даже в керосине!) при температуре 80-100°С получить можно. По реакционной способности они практически не отличаются от обычных реактивов Гриньяра. В книге Ольдекопа и Майера "Введение в элементоорганическую химию" этому вопросу уделяется полстранички (см. стр. 45)
Спасибо большое, почитаю.
-
3 минуты назад, yatcheh сказал:
Проблема, видимо - в самой реакции с магнием. В присутствии эфира или триэтиламина реакция идёт и в бензоле, и в лигроине. А без комплексообразователя поверхность дезактивируется нерастворимым хлоридом магния. По этой причине, кстати - диоксан для гриньяров негоден, в нём хлорид магния даёт совершенно нерастворимый сольват.
Я с гриньярами не работал, а теория этого дела довольно мутная.
Понял, спасибо большое.
-
8 минут назад, yatcheh сказал:
Самому бы разобраться... В одних букварях одно пишут, в других - другое.
То есть точных данных, объясняющих выбор растворителя в реакции Гриньяра, все ещё нет? Подскажите, пожалуйста, как можно всё-таки по-научному обосновать непригодность бензола для данной реакции? Хотел как-то обосновать через равновесие Шленка, но дельного ничего на ум не приходит.
-
1 час назад, yatcheh сказал:
Правильно. Дело не в растворимости, а в равновесии Шленка.
Спасибо большое за ответ. Можете, пожалуйста, объяснить, почему все-таки равновесие Шленка:
2R-MgHal<--->MgR2+MgX2
смещено влево в простых эфирах? Кроме того, нашел информацию, что в углеводородах реактивы Гриньяра получали. Помогите, пожалуйста, разобраться.
-
Всем доброго времени суток. Подскажите, пожалуйста, можно ли получить реактив Гриньяра в среде бензола или других углеводородов? Я считаю, что нет, так как в таких растворителях магнийорганическое соединение ничем не стабилизировано ( с простыми эфирами за счет НЭП кислорода образуются стабильные эфираты). Также я считал, что ввиду высокой полярности связи в магнийорганических соединениях, эти соединения должны быть плохо растворимы в бензоле, но, судя по лабораторным методикам, растворимость данных соединений в бензоле приемлемая. Правильны ли мои рассуждения?
-
В 11.07.2019 в 10:15, yatcheh сказал:
Формально - так. Реально разрыв связи C-Hal и отрыв протона могут идти одновременно, без образования полноценного оксониевого катиона. Был бы растворитель достаточно хорош для сольватации протона.
Впрочем, это не суть важно...
Понял, большое спасибо.
-
15 минут назад, yatcheh сказал:
Замещение в первичных алкилгалогенидах идёт по механизму SN2. Это как бэ - общее место.
Из общих соображений - таки да: первичный карбкатион - это крайне высокоэнергетическая частица, а нуклеофильность молекулы воды - величина, вполне себе весомая, и уж если гидролиз идёт, то он идёт преимущественно по SN2 механизму.
Получается, что гидроксониевое соединение, образовавшееся после основного механизма SN2 потом отщепляет протон и превращается в спирт?
-
Всем доброго времени суток. Подскажите, пожалуйста, по какому механизму происходит гидролиз бромэтана и других первичных галогенпроизводных водой? Предполагаю, что имеет место SN1, так как SN2 с нейтральными молекулами я встречал только с NH3 и производными фосфина. В то же время первичные катионы неустойчивы, что делает данный тип реакции невыгодным.
-
4 часа назад, yatcheh сказал:
Нет, нуклеофильность - это не имманентное свойство частицы, это характеристика её поведения в данной реакции, в данных условиях. И мерой нуклеофильности как раз и является скорость реакции с её участием. В апротонном полярном растворителе в ряду I > Br > Cl > F возрастает скорость, а значит - нуклеофильность.
Понял, спасибо большое.
-
1 час назад, yatcheh сказал:
О, да, и скорость реакции конечно же не зависит от растворителя! Бро, ты под вечер тупеешь! Внимательнее читай Сайкса нашего, Питера:
Хотя ряд и обращается, различия в нуклеофильности не так уж велико. И обращение ряда идёт за счёт увеличения нуклеофильности более мелкого галогенида, а не за счёт уменьшения нуклеофильности йодида.
Йодид-ион в такого рода исследованиях выбран как стандарт, кроме того, иодид хорошо растворим в большинстве полярных растворителей, что позволяет создать большой избыток иодид-аниона. Равновесие при этом смещается глубоко в сторону продукта замещения, а кинетика реакции отвечает псевдопервому порядку по субстрату.
Как-то так

Спасибо большое, это первый литературный источник, где эту обратную зависимость более менее подробно объяснили. Кажется, начал понимать: в апротонных полярных растворителях несколько увеличится скорость реакции SN2 для бромид- и хлорид-анионов. Однако, йодид-анион так и останется самым сильным нуклеофилом. То есть ряд, указанный Травнем больше отражает скорости реакций нежели нуклеофильность? Правильно ли я сделал выводы из прочитанного? Подскажите, пожалуйста.
-
1 час назад, Vimto сказал:
Про влияние растворимости я тоже думал, она наверняка тоже свой вклад вносит, но все-таки хотелось бы понять, как согласуется информация в учебнике с практикой.
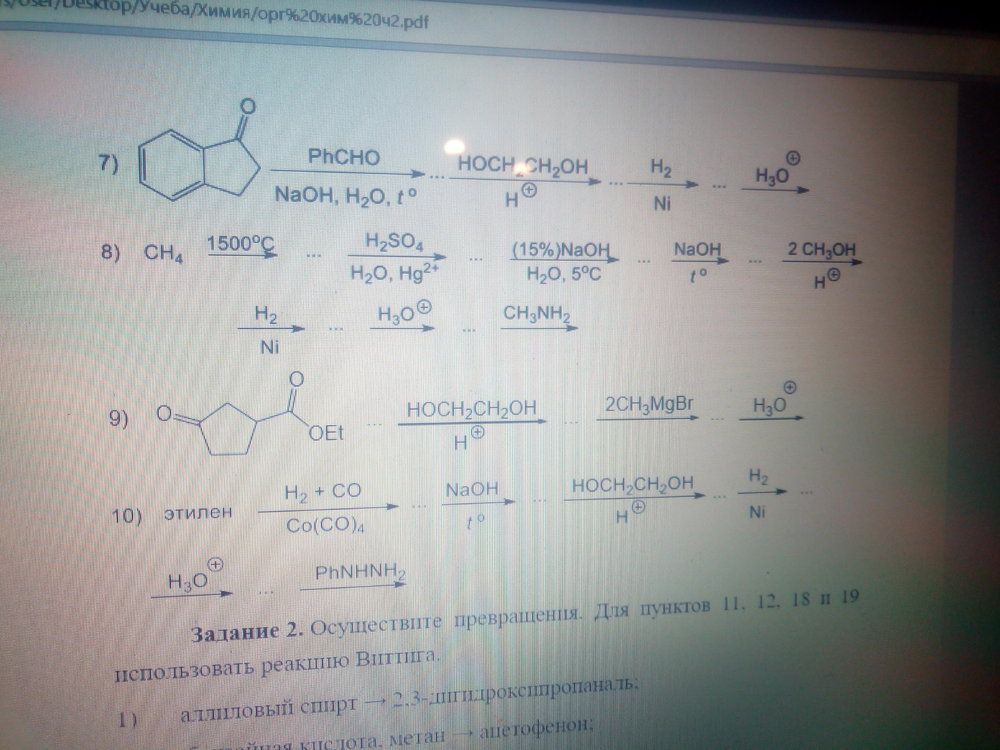






Восстановление кеталя и последующие превращения.
в Решение заданий
Опубликовано
Спасибо большое.