-
Постов
120 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные CopperKettle
-
-
Добрый день! Я перевожу текст по психиатрии, и мне нужно перевести сокращение 5-HIAA на русский. Английское название вещества - 5-hydroxyindoleacetic acid, следовательно, должно быть ГИУК (гидроксииндолуксусная кислота), однако я обнаружил, что в Гугле ее почему-то чаще называют "5-оксииндолуксусной кислотой", ОИУК (вот, например, в этом документе).
ОИУК и ГИУК это синонимы? Я уже давно не освежал химические знания и все забыл, подскажите, пожалуйста.
Может, правильнее будет сокращать 5-HIAA как ОИУК?
-
Пока наша страна ведет преступную войну против Украины, лучше воздерживаться от любых, даже самых дружелюбных, острот по поводу украинцев. Когда этот ужас кончится, можно будет снова жартувать про хохлов.

-
 1
1
-
-
Интересно, как эта реакция происходит..
-
А вот на Chemistry StackExchange человек написал в ответе, что MgO можно восстановить водородом при высоком давлении и температуре.
-
Cu + S = CuS
2CuS + H2 =t= Cu2S + H2S
2H2S + 3O2 = 2SO2 + 2H2O
Спасибо! Я начал искать, почему именно эта реакция возможна, и нашел вот такой ответ:
Интересно, почему железо - ведь железо стоит левее водорода, а значит, с большей легкостью отдаёт электроны, нежели водород. С медью понятно - она в ряду активности стоит правее, как и серебро, ртуть, платина, золото.
-
А можно ли как-нибудь получить из CuS сероводород?
Вот задание на сайте "Химуля" - я знаю, как превратить Cu в CuS, но ведь Cu стоит в ряду активности правее железа.
Что можно сделать? Растворить сначала в концентрированной азотной кислоте? А что потом?
-
 1
1
-
-
Сейчас поподробнее перечитаю правило Марковникова, чтобы понять. Я не думал, что оно может иметь отношение к этому случаю. Думал, что оно только про присоединение (но давно не повторял химию уже..)
P.S. Перечитал правило Марковникова, не понял, как его тут применить. -
Извиняюсь за некрофилию, но что такое HOSO3H? Серная кислота?
Я сейчас читаю вот эту страничку на Chemguide - там говорится, что двойная связь может образоваться и в позиции 1, и в позиции 2 (а в последнем случае мы еще получим либо cis, либо trans вариант).
В то же время вопрос ЕГЭ требует указать как продукт либо бутен-2 либо бутен-1. -
Добрый день!
Потребовалось перевести на русский это название: a-epoxyabiraterone.
Не подскажете, следует ли ставить дефис или нет?
α-эпоксиабиратеронили
α-эпокси-абиратерон?
-
Доброе утро!
Перевожу один документ с английского, не уверен, правильно ли формулирую по-русски:Efavirenz pentyne analog - "пентиновый аналог эфавиренза"?
Efavirenz pentenoyne - "эфавиренз пентеноин"?
Efavirenz aminoalcohol - "эфавиренз аминоспирт"?
Methyl efavirenz - "метилэфавиренз"?
Efavirenz amino alcohol methyl carbamate - "Эфавиренз аминоспирт метилкарбамат"? O_O
A-benzylefavirenz - "А-бензилэфавиренз "?
Efavirenz benzoylaminoalcohol - Эфавирензбензоиламиноспирт ?
Cyclobutenylindole analog - "Циклобутенилиндоловый аналог" или "Аналог циклобутенилиндола"?
Расшифровал, что такое Efavirenz penteneyne
Это заместитель с пятиуглеродной структурой. Интересно, русский химик не поморщится, увидев "Ефавирензпентенеин" вместо "Эфавиренз с группой 3-метилбут-3-ен-1-ин-1-ил"? Первый вариант гораздо легче уместить в табличке, что перевожу
-
Спасибо! Просто когда разбираю много заданий одно за другим, под вечер уже не думается.
"Скину вопрос в форум, утром гляну". (0:
-
-
Да, что-то я пропустил "избыток" в условии.
-
-
Потому что пропустили много CO2, что бы рН уменьшился до 7-7.5, а при таких pH может существовать только гидрокарбонат.
Он высокий, т.к. Na[Al(OH)4] составлена сильным основанием + слабой кислотой?
А зачем его нужно уменьшать?
В этой реакции его не нужно уменьшать:
2NaOH + CO2 → Na2CO3 + H2O
?
Что-то не совсем ясно... В одной реакции можно получить Na2CO3, а в другой нужно зачем-то давать избыток CO2.
-
]Я на похожую реакцию наткнулся в одной из задач номер 37 (ЕГЭ), только с натрием:
Задание 37 № 2365. К раствору гидроксида натрия добавили порошок алюминия. Через раствор полученного вещества пропустили избыток углекислого газа. Выпавший осадок отделили и прокалили. Полученный продукт сплавили с карбонатом натрия.Напишите уравнения четырёх описанных реакций.
Тоже написал слева воду, т.к. "через раствор" пропускаем газ все-таки. Но ясно, что её можно убрать.
Интересно, почему получается гидрокарбонат, а не просто карбонат.
Вот у Химули говорится, что при избытке получаем гидрокарбонат, а так - просто карбонат.
-
Можно сравнить с реакцией, в которой действительно образуется газообразный азот.
NaNO2 + NH4Cl -> NaCl + H2O + N2
Это реакция сопропорционирования. В NO2(-) ионе степень окисления азота = +3, в ионе аммония NH4(+) степень окисления азота = -3. Два иона сталкиваются, и два атома азота "аннигилируют" свои степени окисления до одной степени = 0. Получаем газ N2.
-
Оказывается, эта реакция - один из возможных тестов на нитраты. А сплав алюминия, меди (катализатор??) и цинка, используемый для определения нитрат-иона, называется "Сплав Деварда".
По поводу "почему не получится просто газообразный азот", получил коммент:
The half-equations and corresponding redox potential show that the reduction to NH3 is thermodynamically possible.
The formation of N2 would require combination of two N-containing intermediates.
Since the further reduction to NH3 is fast, it is unlikely that two such N-containing intermediates find each other.
Since the reduction to NH3 is faster than the competing reaction to N2, the reduction doesn’t stop at N2.
Since the solution contains NaOH, NH3 escapes as a gas, which shifts the equilibrium towards the formation of NH3.N-содержащие посредники имеют мало шансов повстречаться, чтобы образовать N2, и реакция по преобразованию в NH3 идет быстрее, чем формирование N2.
-
В зависимости от количества NaOH реакция протекает по-разному - 5 вариантов в последовательности с увеличением:
AlCl3 + NaOH = Al(OH)2Cl + NaCl;
AlCl3 + 2 NaOH = AlOHCl2 + 2 NaCl;
AlCl3 + 3 NaOH = Al(OH)3 + 3 NaCl;
AlCl3 + 4 NaOH = Na[Al(OH)4] + 3 NaCl;
AlCl3 + 6 NaOH = Na3[Al(OH)6] + 3 NaCl.
Это точно так?
Значит, если в условиях задачи написано просто "избыток", считать по 4 варианту?
Задание 37 № 4423. При сливании водных растворов сульфита калия и перманганата калия выпал осадок. Осадок при нагревании обработали концентрированной соляной кислотой, при этом наблюдалось образование газа. Полученный газ прореагировал с алюминием. Продукт данной реакции растворили в избытке раствора гидроксида натрия. Напишите уравнения четырёх описанных реакций.
В ответе посчитана реакция с тетрагидроалюминатом натрия.
-
Вот нашел в интернете, но тоже не очень понимаю:
Многие химические реакции, происходящие в метаболизме микроорганизмов, сопровождаются переносом электронов. Всякое передвижение электронов отражается на величине потенциала. Таким образом, обмен веществ связан с окислительно-восстановительным потенциалом системы. Величину окислительно-восстановительного потенциала обычно выражают в вольтах, т. е. в электрическом напряжении, возникающем на электроде, погруженном в исследуемую жидкость. Величину окислительно-восстановительного потенциала в биологии принято выражать через индекс rН2. Эта величина характеризует кислородно-водородное равновесие. pH среды показывает соотношение между Н+ и ОН— ионами, а rН2 — между Н2 и O2. Кроме того, rН2 характеризует суммарное окислительно-восстановительное состояние, обусловленное не только концентрацией (парциальным давлением) кислорода и водорода, но и всеми присутствующими окислителями и восстановителями. Таким образом, rН2 дает представление об окислительной или восстановительной способности сред для культивирования или других растворов. Преимущество этой величины перед потенциалом, выраженным в вольтах, заключается в том, что величина потенциала изменяется в зависимости от pH, а в индексе rН2 pH входит как составная часть, которую определяют отдельно и учитывают при расчете.Источник: http://www.activestudy.info/znachenie-ph-i-rh2-dlya-zhiznedeyatelnosti-mikroorganizmov/ © Зооинженерный факультет МСХА
-
думаю что зачтется. Оксид тут за окислитель идет а железо за восстановитель (получится закись железа). А у вас написана реакция с избытком окиси железа.
Но ученик может сказать - а в задаче не указаны пропорции исходных веществ: просто сказано "сплавили с железом".
-
Из примера 37 номер 42:
Fe2O3 + Fe -> 3FeO
А может реакция пойти так:
4Fe2O3 + Fe -> 3Fe3O4
Если да, то не зачтется ли это как ошибка?
-
Я прочитал весь школьный курс (Рудзитис), и могу сказать, что действительно, при прохождении примеров для ЕГЭ на каждом шагу - что-то новое.. по крайней мере, такое ощущение создается. Механизмы реакций (почему реакция протекает) по большей части знаю или узнаю благодаря chemguide, stackexchange и еще книжкам на английском языке. А без понимания механизма это зазубривание..
Про это совсем не знал, спасибо.
Слова лучше всего запоминать, используя их, а не "в двух столбиках".Да, они запоминаются лучше всего при использовании. Беда в том, что в литературном\научном языке слов и выражений так много, что следующее использование может наступить через месяц, когда уже все забыл. Заучивание "в столбики" можно разнообразить - сочинять нелепые истории или забавные предложения со словами, например, или выписывать цитаты из поэзии, литературы.
-
Мне кажется, что все задачи номер 37 в егэ содержат реакции, которые нужно механически зазубрить. Это так?

Есть ли какой-то способ зазубривания таких реакций? Может, как слова в англ. языке учат -- выписывать в два столбика реагенты\продукты и повторять каждый день?





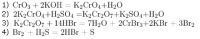
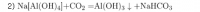
Folinic acid - фолиниевая кислота или фолиновая кислота? Как правильнее? (Терминология)
в Органическая химия
Опубликовано · Изменено пользователем CopperKettle
Добрый день! Интересно, какой перевод английского термина "folinic acid" более верен. В литературе нахожу и "фолиниевая кислота", и "фолиновая кислота".
Когда писал статью в Википедии в 2019 году, сначала думал, что "фолиновая", но потом где-то нашел, что верный вариант - "фолиниевая", и это название использовал. А сегодня кто-то заменил название на "фолиновая". Может быть, я был неправ? ?
Я уже не помню, как именно выбирал название.