-
Постов
120 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные CopperKettle
-
-
-
Интересный вопрос. У меня недостаточно знаний, чтобы на него ответить. Поискал по "valence carbon monoxide", наткнулся на обсуждение этого вопроса, но понять пока не могу.
Понял только, что the jury is still out, то есть все еще спорят, какая у него валентность - 2 или 4. Если берут валентность 4, объясняют это некоей теорией "латентных валентностей"(?).
Интересно, как это кислород отдает два электрона углероду для донорно-акц.связи, хотя у кислорода выше электроотрицательность.
-
Сожгите её! Читайте лучше Глинку... а лучше Некрасова. Ибо единственное, что могут развить в читателе подобные книги (говорю по собственному опыту
 ) это ненависть к химии в целом.
) это ненависть к химии в целом. Я думаю, это не проблема. До 18 века (ал)химики учились по таким книгам, что сейчас и с LSD не разберешься, и ничего.

Наверное, правда, они химичили больше практически, и это поддерживало интерес.
-
что за книга у вас?
ГДЗ Химия 9 класс к учебнику Рудзитиса\Фельдмана.
Ошибки и очепятки в оной книге очень развивают мышление.
Нужно к ней выпустить "сборник ошибок и опечаток".
-
Разве это возможно? Реакции не будет, ведь продукты полностью растворимы. В том же решебнике чуть выше говорится:
В чем же разница? Хлорид магния не реагирует с сульфатом калия по той же причине. Зачем они расписывают первое уравнение, а второе относят к невыполнимым?
-
Понятно, в решебнике - промежуточный вариант. В концентрированном виде сера отнимает аж целых 8 электронов, в разбавленном вообще окислителем выступает водород, отнимая всего 2 электрона, а в решебнике сера отнимает лишь 6 электронов. Интересно.
То есть если H2SO4 концентрированная, то S умудряется так много отобрать электронов у Zn, что у нее становится заряд (-2), за счет этого она привлекает к себе ионы H+ и образует H2S. Если быть точнее, захватывает H(+) из ионов гидроксония.
Если же концентрация чуть ниже, то сера просто восстанавливается до заряда (0) и записывается просто S. (по ошибке сначала записал "газ S2")
-
Оба правильные, первая с разбавленной кислотой, вторая с концентрированной.
Спасибо! Я так понимаю, составители решебника нафантазировали третий вариант. (0:
-
Спасибо! Тут ответили так же.
Я просто предполагал, что раз все, что отдает электроны - основания, то любые ионы будут изменять среду соответственно.
-
В интернете я нашел два варианта уравнения реакции:
Zn + H2SO4 → ZnSO4 + H2
4Zn + 5H2SO4 = H2S + 4ZnSO4 + 4H2O (на этом форуме, кстати)
А вот третий, возможно ошибочный, из сборника ответов к моему учебнику:Какой вариант реакции наиболее типичен? Что влияет на то, какие продукты будут у реакции?
-
Кислые свойства обусловлены ионом водорода H+
Ионы цинка записаны неверно. Надо так Zn2+ - 2+ это заряд.
Последнее уравнение показывает, что ионы цинка отрывают от молекулы воды частицу ОН-, а ионы водорода высвобождаются и дают кислую среду.
Если они (NO3(-)) как были, так и остались - значит в реакции не участвовали.
Значит их можно из уравнения реакции убрать
А эти 2NO3(-), они ведь дают основную среду? Как понять, что H(+) их перекислит?
(0:
-
заряды друг друга обнулят, но это обеспечит только электронейтральность системы (закон сохранения заряда, однако). другое дело что в результате гидролиза имеем равновесную смесь основной соли и азотной кислоты, отсюда и кислая среда.
Спасибо! Еще интересно, почему в последней строчке удалены группы NO3(-) из обеих частей формулы.
-
-
Окислитель ClO3-, восстановитель Cl-
Спасибо, но до меня еще не дошло.
Значит, у [ClO3] заряд сменился с -1 до -2. Где это заметно в правой части формулы?
P.S. Тут мне ответили, что на самом деле у хлора в ионе ClO3- степень окисления равна +5, оттого и redox реакция.

-
Вот реакция:
Насколько я понимаю, уровень окисления K остается +1, но часть атомов хлора меняют окисление с -1 до 0. Что же является окислителем хлора?
-
опечатка
Спасибо! Попытаюсь найти другой учебник, т.к. решебник к Рудзитису содержит слишком много опечаток.
-
-
-
Потому что написана полная чушь, марганец восстанавливается, но ни кто не окисляется.
4KMnO4 + 4NaOH = 2K2MnO4 + 2Na2MnO4 + O2 + 2H2O
Чушь в сборнике ответов, т.к. у марганца была степень окисления +7, и вдруг стала +4? Это должно было как-то повысить степени окисления других участников реакции?
-
Добрый день!
Из книги ответов к учебнику Рудзитиса (8 класс):

Почему в реакции не получается вместо этого NaMnO4 +KOH?
Возможно, это примитивный вопрос. Я лишь недавно решил освежить знания по химии. Пока что предполагаю, что соль + основание = другая соль + другое основание.

Подскажите, что почитать на эту тему.


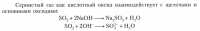


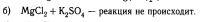
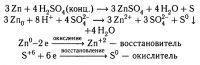
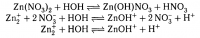


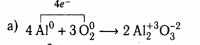
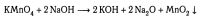
Как получить из сульфата натрия серную кислоту?
в Решение заданий
Опубликовано · Изменено пользователем CopperKettle
Присоединяюсь к вопросу. У меня в учебнике есть такая схемка взаимодействий соединений серы:
Можно ли из какого-либо сульфата получить серную кислоту? Нужно взять более мощную кислоту?
Посмотрите, сколько просмотров уже у этого вопроса. Хорошо бы иметь хотя б частичный ответ. (0: