-
Постов
5193 -
Зарегистрирован
-
Посещение
-
Победитель дней
26
Тип контента
Профили
Форумы
События
Сообщения, опубликованные Paul_S
-
-
В 06.05.2024 в 09:55, Jannni сказал:
Здравствуйте, подскажите, пожалуйста, как в органическом синтезе выбирается исходное вещество?
Этому учит ретросинтетический анализ

-
Гидразин разлагается на меди до аммиака и азота, на платине - до азота и водорода.
-
 1
1
-
-
В 02.05.2024 в 22:20, podlyinarod сказал:
Блин. Это для меня открытие. Я думал, что любая кислота, вернее, любой протон, в водных растворах существует в виде гидроксония H3O+. Так окажется, что и в растворе сульфата гидроксония, получающегося приливанием серной кислоты к воде - нет серной кислоты... 🧐
Перхлорат оксония - устойчивое твердое вещество, плавящееся при 50 С. Смеси воды и хлорной кислоты с мольным соотношением больше единицы - это растворы перхлората оксония.
-
 1
1
-
-
С гидроперитом его смешай

-
В 01.05.2024 в 18:24, yatcheh сказал:
Мононитро. И кислота одна, и субстрат со вкусом подобран - без изомеров мононитруется.
Ксилолы настолько легко нитруются, что с нитрующей смесью получить мононитропроизводное нереально. Просто с азоткой, наверно, можно. Думаю, реально будет 2,5-динитро-п-ксилол. Чего хотели авторы задачи, я не знаю.
-
В 01.05.2024 в 21:22, Ярослав Беспалов сказал:
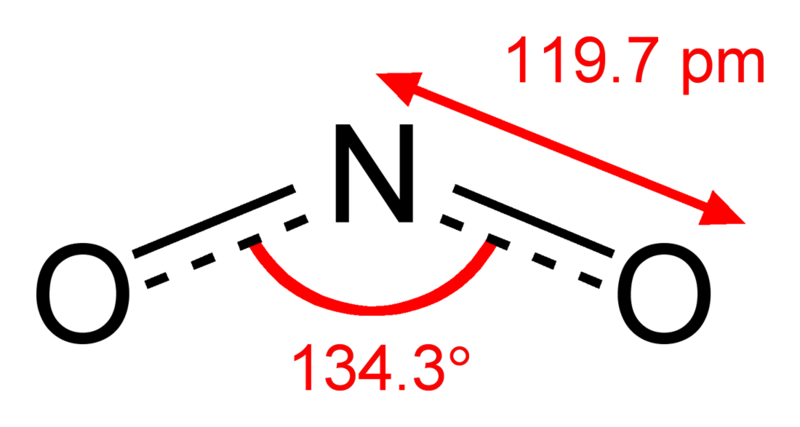
Сам удивился, но во многих источниках структурную формулу изображают вот так. Пунктиром показана пи-электронная система. Дело в том, что кратность связей с двумя кислородами, по идее, разная. Но валентные углы одинаковы.
Удивляет то, что негибридизированная p-орбиталь у азота всего одна - та самая, на которой неспаренный электрон. С чем тогда он сопрягается? С p-орбиталями кислорода?
Это семиполярная связь
https://ru.wikipedia.org/wiki/Ковалентная_связь#Виды_ковалентной_связи
-
Х5 - бутан, Х4 - изобутан, Х1 - соль изобутанкарбоновой к-ты. На последней стадии, думаю будет динитропродукт с нитрогруппами в орто-положениях к метилам.
-
В 01.05.2024 в 17:15, pauk сказал:
Грохать демократически избранного президента суверенного государства-члена ООН - это не наш метод.
Ну да. Наш метод - терроризировать население Украины, причем в русскоязычных регионах, в основном. Так победим!
-
В 01.05.2024 в 17:04, chemister2010 сказал:
Так это магнийтермия, а не реакция вольфрама с углеродом!

"из смеси оксида вольфрама, металлического магния, технического углерода и CaCO3"
-
Как ни удивительно, но 100-%-ная азотная кислота и ее концентрированные растворы, содержащие катионы нитрония NO2 + , но полностью очищенные от оксида азота(IV) 2 , вообще не вступают во взаимодействие в момент контакта с такими типичными восстановителями, как цинк, магний, иодоводород, сероводород, оксид серы(IV), арсин, фосфин, формальдегид. В то же время кислота, содержащая NО2, моментально и бурно (иногда со взрывом и воспламенением) окисляет эти восстановители. Реакции с участием азотной кислоты, очищенной от NO2, начинаются лишь по прошествии определенного интервала времени − так называемого индукционного периода, на протяжении которого в системе накапливается необходимое для начала реакции количество оксида азота(IV) за счет разложения НNО3. Индукционный период можно сократить введением извне в очищенную кислоту небольших количеств готового NO2 или нитритов, образующих его в кислой среде. Таким образом, окислительное действие азотной кислоты в очень концентрированных и концентрированных растворах определяется, фактически, окислительными свойствами продукта ее разложения − оксида азота(IV), который образуется на промежуточных стадиях
-
 1
1
-
-
-
Многие ионы переходных металлов парамагнитны, но наибольший магнитный момент у Mn2+ и Fe3+, у них по 5 неспаренных электронов на d-оболочке. Так что соли железа-3+ тоже должны сильным магнитом заметно притягиваться. Среди лантаноидов наибольший спиновый магнитный момент у Gd3+ (7 несп. электронов), но за счет орбитального вклада наибольший суммарный момент у Dy3+. Если насыпать соль лантаноида на бумажку и провести с другой стороны магнитом, кристаллики будут бегать вслед за ним

-
 1
1
-
-
Al2O3 диссоциирует на ионы в расплаве криолита

-
В 01.05.2024 в 11:46, chemister2010 сказал:
Да полно. Насколько я помню карбиды молибдена и вольфрама синтезируют самораспространяющимся синтезом.
Что-то совсем не верится, однако

-
В 01.05.2024 в 15:23, Alex Ferrum сказал:
Это вы так думаете или видели в каких-то источниках? Если видели в источниках, можете на них сослаться.
Да в Некрасове, по-моему, есть... NO и NO2 - радикальные частицы, поэтому они легко запускают редокс-процессы.
-
В 30.04.2024 в 18:57, fossilknife сказал:
Это как? Перхлорат оксония(H3OCIO4) можно представить как гидрат HClO4 • H2O. Соответственно раствор перхлората оксония = бодяженная хлорка
Я конечно могу и ошибаться
Ну да. А перхлорат аммония - хлорка, разбодяженная аммиаком

-
Соли лантаноидов с гадолиния по эрбий

-
 1
1
-
-
В 30.04.2024 в 16:40, fossilknife сказал:
 ...... а вы как узнали?
...... а вы как узнали?
На самом деле собираюсь вытеснять из перхлоратов сернягой, потому из растворов сульфатов магния и аммония
В растворе перхлората гидроксония НЕТ хлорной кислоты

-
В 30.04.2024 в 14:58, fossilknife сказал:
А как воду то тудой запхать? Мне хлорку(мл 5-10) надо экстрагировать из р-ра, а пишут, что она в галогенуглях растворима хорошо. А из них у меня только ЧХУ. Да и летучий он, испарится и будет чистая кислота
Из чего экстрагировать хлорную кислоту? Из водного раствора перхлората гидроксония?

-
В 29.04.2024 в 20:10, Wolfy36 сказал:
2NaClO + 2K2MnO4 + 2H2O -> 2NaOH + 2KMnO4 + 2KOH + Cl2
2KMnO4 + NaClO + H2O → 2MnO2 + NaClO4 + 2KOHГипохлорит окисляет манганат до перманганата, но перманганат окисляет гипохлорит до перхлората? Где логика? До перхлората в воде даже хлорат электролизом проблематично окислить. Кроме того, какое может быть выделение хлора в щелочной среде? Хлор со щелочью не реагирует?
Гипохлорит при восстановлении до хлорида в щелочной среде гораздо более сильный окислитель, чем перманганат и манганат.
ClO- + H2O + 2e = Cl- + 2OH- +0.89 +0.88 MnO4- + e = MnO42- +0.564 +0.54 MnO4- + 2H2O + 3e = MnO2 + 4OH- +0.57 MnO4- + 2H2O + 3e = MnO2{pyrolusite} + 4OH- +0.588 MnO42- + 2H2O + 2e = MnO2 + 4OH- +0.60 +0.58 Но перманганат склонен окислять воду, а гипохлорит - нет. Скорее всего, здесь имела место колебательная реакция с большим периодом, сводящаяся к окислению воды гипохлоритом при посредничестве перманганата и манганата. Перманганат окислял воду или гидроксид-ион, восстанавливаясь в манганат, который гипохлорит снова окислял в манганат, пока не израсходовался.
-
 1
1
-
 1
1
-
-
Исследовалась полимеризация стирола в CCl4, инициированная хлорной кислотой. Причем они прямо отгоняли HClO4 в CCl4 и использовали этот раствор. Так что он даже вполне стабилен.
https://www.tandfonline.com/doi/pdf/10.1080/10601327208056874
-
Для решения химических задач нужно, помимо знания арифметики, обладать химическими познаниями. Разложение иодидов на раскаленной проволоке применяется для получения высокочистого титана, циркония, гафния и еще некоторых переходных металлов. Иодид натрия разложить нагреванием непросто, можно догадаться об этом, просто вспомнив, что это очень активный щелочной металл, образующий прочные соединения с неметаллами, которые трудно разложить. Кроме того, температура кипения натрия тоже не особо высокая (883 С), и с раскаленной проволоки он просто испарится.
-
В 29.04.2024 в 16:19, Alex Ferrum сказал:
Из Википедии, поскольку ссылок на эту информацию не было, решил уточнить на форуме, насколько она соответствует или не соответствует действительности.
Это чьи-то мечты...
-
В 29.04.2024 в 12:32, Alex Ferrum сказал:
Насколько мне известно, в присутствии нитрата мочевины этерификации происходит даже в очень разбавленных растворах азотной кислоты.
Откуда Вам это известно?



С праздником, дорогие товарищи!
в Курилка
Опубликовано
В России пролетарская революция "устояла", а в Германии революционеров "утопили в крови"... Вы ничего не путаете, уважаемый? "Пролетарская" революция в РИ была совершена в первую очередь руками солдат, т.е., бывших крестьян, вырванных из традиционного уклада и приученных убивать на войне, которая для них потеряла всякий смысл. С их помощью легко удалось превратить "империалистическую войну в гражданскую", соблазнив их лозунгом "земля - крестьянам". А реальные вожди революции были почти полностью истреблены в 1936-38 гг. Троцкого заблаговременно выслали из страны, но Сталин и в Мексике устроил ему день ледоруба. Ленин очень вовремя умер в 1924 году, будучи совсем не старым. Он мог и до 1937 г. дожить. Тогда ситуация была бы интересней. Ленин-Троцкий-Сталин. Задача о трех телах....
В общем, то, что Сталин сделал во второй половине 30-х - это была явная контрреволюция, в результате которой он стал полноправным диктатором. Также как и Наполеон, достигший власти в результате Французской революции, в итоге короновал себя императором.