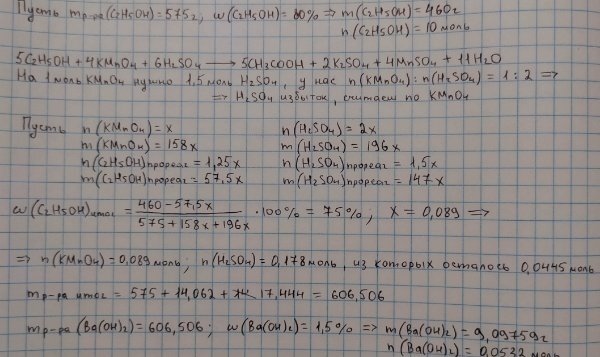Walter White 07
Пользователи-
Постов
53 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Весь контент Walter White 07
-
По моим рассчетам гидроксид бария ещё нейтрализует уксусную немного Не факт, что верно, сам шкил, но считаю, что верно! (Пришлось сжать чтобы отправилось, сайт не пускает выше 200кб фото) P.s. некоторые действия не расписаны, например найдено количество уксусной, которое прореагирует с гидроксидом бария, а ниже сразу вычитается масса этой уксусной из всей массы уксусной (6,675-1,044))
-
Здравствуйте! Кто учился или учится на химические специальности, расскажите, что варили? Как варили? Может быть какие-нибудь интересные истории есть))
-
Она хороший человек, я её уважаю, а также в чём-то даже понимаю, ибо в моём маленьком (на одном из самых больших в России) селе очень редко кто-то сдаёт химию, а химия в школе - базовая, с темами ЕГЭ, или просто углубленными темами она сталкивается раз в год при подготовке ребят, и то не факт. Работает она больше 20 лет, конечно за это время с такими условиями все забыла с ВУЗа своего А по поводу ссылочки, которую скинули, уже изучил и всё сразу понял, спасибо!
-
Про HF знаю одну штуку интересную, как образование кислых солей... Это связано с крайне сильной полярностью молекулы? Отсюда и сила водородных связей? Поэтому существуют устойчивые димеры? А отсюда и кислые соли димеров фтороводорода по типу NaHF2?
-
Нам преподают базовую химию, и то раз в неделю, и то училка утверждает, мол перманганат калия в нейтральной среде при окислении не даёт осадка
-
Вода диссоциирует? Я думал это условность школьных учебников, мол вода - это H+ и OH-... Из других источников давно знаю, что в воде протоны существуют в виде ионов гидроксония, и учитывая ваше высказывание осмелюсь предположить, что уравнение диссоциации воды: 2H2O = H3O+ и OH- А с чем это связано? С водородными связями между молекулами? Атомы кислорода одних молекул тянут на себя атомы водорода других молекул, благодаря чему и образуются H3O+ и OH-?
-
Для закрепления материала все же советовал бы проверить это на практике, так сказать сначала теория, затем практика (Шутка, хех)
-
Ради этого и стараюсь учиться, дабы была возможность дальше изучать любимую науку в ВУЗе и узнавать много нового)
-
Здравствуйте! В неизвестном неорганическом в-ве m(Fe):m(O)=2,333, нужно найти его формулу. Абсурдным ли является такой подход: m(Fe):m(O)=2,333:1 Пусть у нас 1 моль атомов Fe, их масса 56г, атомов O значит X моль, их масса 16x. 56/16x=2,333:1, откуда X=1,5 моль, значит на 2 атома Fe приходится 3 атома O, Fe2O3 Может как-то проще можно?
-
Да, конечно я изучал продукты восстановления азотки с Ме при различных конц., с этой таблицей я знаком, но она довольно общая, я ей не верил, и нам не советовали, мы изучали продукты восстановления индивидуально для каждого Ме (ЩА, ЩЗМ, Be, Al, Zn, Cr, Fe, Cu и т.д.), всему этому нас обучали, но на различных пробниках я ни разу не видел "...при взаимодействии с оч. конц. или оч. разб. азотной...", обычно просто конц./разб. Да и вопрос автора тоже подразумевал исключительно конц./разб. р-ры азотки, поэтому привёл уравнения р-ций именно на конц. и разб.
-
Слушай, если тебе, как и мне в этом году, для уровня ЕГЭ, то вот: P.S. готовлюсь по книге "Н.Е. Кузьменко, В.В. Еремин, В.А. Попкова. Начала химии", говорю лишь то, чему меня научила эта книга, а ей доверять можно: H2SO4 (конц.) + Zn —> SO2 + сольвода HNO3 (конц.) + Zn —> NO2 + сольвода HCl (конц.) + Zn —> H2 + соль H2SO4 (разб.) + Zn —> H2 + соль HNO3 (разб.) + Zn —> NO + сольвода HCl (разб.) + Zn —> Н2 + соль H2SO4 (конц., t°) + Fe —> SO2 + Fe2(SO4)3 + H2O HNO3 (конц., t°) + Fe —> NO2 + Fe(NO3)3 + H2O HCl (конц.) + Fe —> FeCl2 + H2 H2SO4 (разб.) + Fe —> FeSO4 + H2 HNO3 (разб.) + Fe —> Fe(NO3)3 + NO + H2O HCl (разб.) + Fe —> FeCl2 + H2 H2SO4 (конц.) + Cu —> SO2 + сольвода HNO3 (конц.) + Cu —> NO2 + сольвода HCl (конц., t°) + Cu —> H[CuCl2] + H2 H2SO4 (разб.) + Cu —> нет р-ции HNO3 (разб.) + Cu —> NO + сольвода HCl (разб.) + Cu —> нет р-ции Fe с HNO3 (конц.) или H2SO4 (конц.) без t°, т.е. при н.у. не реагирует из-за пассивации
-
Здравствуйте! В школе дали цепочку: CH3Br —> X1 —> CH3COOH Я не могу представить, как можно получить уксусную к-ту в 2 стадии из бромистого метила с помощью школьных р-ций Я предполагаю, что это: 1) CH3Br + KCN —> CH3CN + KBr 2) CH3CN + 2H2O —> CH3COOH + NH3 Но это не школьные р-ции! Возможно ли как-то проще это сделать? Если нет, то подскажите пожалуйста, возможна ли моя цепочка, и какие условия нужно подписать над стрелочками?
-
Слушай, ЕГЭ и химия профессионалов - разные вещи, тебе здесь могут наговорить кучу не то что бы неверных вещей, а, скорее, более правильных, чем нужно на ЕГЭ Я же правильно понимаю, что ты, как и я, сдаешь ЕГЭ? Так вот, для ЕГЭ есть следующее правило: На ионы расписывают сильные кислоты, сильные основания, растворимые соли В молекулярном виде записывают воду, слабые кислоты, слабые основания, малорастворимые/нерастворимые соли и прочие НЕэлектролиты И да, Ca(OH)2 может быть как щелочь, если брать её в реагенты, но в продуктах нужно считать его осадком, а следовательно его то расписывают, то нет (30 задание ЕГЭ)
-
Очень радует, спасибо, что всегда отвечаете на вопросы!
-
Здравствуйте! То, что материал по профильной химии, который преподносят ученикам в школе, отличается от материала, требуемого на ЕГЭ - факт, я считаю. Мне кажется, что школьный материал профильной химии обширнее требуемого материала на ЕГЭ. Однако в нашей школе преподают базовую химию, а это даже ниже уровня ЕГЭ. По этой причине последние полтора года я изучал химию в открытых источниках, но все они были нацелены на подготовку к ЕГЭ. Я пишу пробники ЕГЭ на 92-100 баллов, т.е. в принципе материал, требуемый на ЕГЭ, мною усвоен, НО Как я уже сказал, я считаю, что школьная химия профильного уровня даёт больше знаний, чем необходимо для сдачи ЕГЭ, а следовательно у меня имеются некоторые пробелы в знаниях. Собственно вопрос: в ВУЗе я смогу наверстать упущенные знания, т.е. будут ли в ВУЗе заново проходиться школьные темы, или же там абсолютно всё новое?
-
Всей душой меня тянет в область органической химии, и это далеко не переменное желание) Меня волнует лишь один вопрос: с какими ребятами я буду конкурировать при поступлении в РХТУ, ведь одно дело минимальные баллы для поступления (набрать их не составит абсолютно никакого труда), другое - уровень подготовки поступающих ребят, которые могут вытеснить меня из списка в случае более высоких баллов, чем у меня, из-за чего я не поступлю. Я считал, что ориентироваться стоит на баллы ребят, которые смогли поступить в прошлом году, но когда я увидел, что в такой "крутой" ВУЗ поступили ребята, набравшие всего 50 баллов по химии (это очень мало), меня начали терзать сомнения, те ли я документы посмотрел, точно ли они смогли поступить, действительно ли так
-
А как насчёт игры, где, к примеру, будут появляться определённые органические в-ва, а нам нужно будет из предложенных ниже вариантов его названия выбрать верный? Либо вместо вариантов названия варианты класса соединения, а также уровни сложности добавить, думаю это было бы очень интересно, но, конечно же, понимаю, что это не так просто, но идея есть идея :3
-
Воронка Бюхнера без шлифов, она держится на колбе с помощью резиновой прокладки под воронку Бюхнера... Возможно данный фильтр Шотта изготовлен под какую-либо прокладку, хз, имхо имхо имхо
-
Здравствуйте! Честно говоря очень плохо разбираюсь и ориентируюсь в различных документах на сайтах ВУЗов В РХТУ я просмотрел различные приказы о зачислении, и в некоторых из них, например в приказе о зачислении 17го августа, зачислили ребят, которые набрали 39 по химии, 50 по математике и 41 по русскому Вопрос: я всё правильно понимаю? Туда смогли поступить ребята с, прошу прощения, действительно на столько слабеньким уровнем подготовки? Просто когда я рассматривал этот вариант поступления я рассчитывал на жёсткий конкурс, в котором будут ребята с 260+ баллами ЕГЭ, но посмотрев, какие ребята туда смогли поступить в 2021 году я понял, что в 2022 году я буду конкурировать не исключительно с умными ребятами. Вообщем поступить туда, оказывается, легче, чем я думал, или я ошибаюсь?
-
Мы не можем округлять в соотношениях, это противоречит законам математики, даже не химии, мы должны домножать оба числа в соотношении на абсолютно любое Допустим 1:2, мы можем домножить на 5 и получить 5:10, можем на 50, будет 50:100, всё равно суть осталась одна и та же - справа число в 2 раза больше, чем слева У нас аналогично, 1:2,5 как 2:5, либо как 100:250, суть одна и та же - справа число в 2,5 раз больше, чем слева, но мы ищем формулу, значит берём наименьшие круглые числа - 2:5 В задачах на определение молекулярной формулы орг. в-ва мы можем придти к n(C):n(H)=1:1, но такого в-ва не существует, а в условии, к примеру, сказано, что это ароматическое соединение, значит мы домножим на 6 и получим 6:6 - бензол, соотношение не показывает точное количество атомов, оно показывает, условно говоря, во сколько раз тех или иных атомов больше, чем других, 1:1 - значит их одинаково, 1:2 - значит вторых атомов в 2 раза больше и т.д., 1:3:6 - значит вторых атомов в 3 раза больше, чем первых, и в 2 раза меньше, чем вторых
-
Окей, у тебя есть 10 яблок и 20 груш, они относятся друг к другу как 10:20, либо как 1:2, это то же самое
-
Пусть масса соединения 100г, тогда масса атомов Р = 43,66г и n(P)=1,4моль, масса атомов О = 56,34г и n(O)=3,5моль n(P):n(O)=1,4:3,5=1:2,5=2:5
-
https://scienceforyou.ru/teorija-dlja-podgotovki-k-egje https://chemege.ru/materials/ Советую пользоваться этими материалами при подготовке к ЕГЭ: 1 сайт абсолютно вся необходимая теория, кроме сложных задач 2 сайт более углубленная, не все попадется на ЕГЭ, но позволит расширить кругозор и выработать химическую логику, нужно долистать до "Курс подготовки к ЕГЭ, ОГЭ, ГИА" Сам благодаря первому сайту набрал первые 80 баллов на пробнике, на двух сайтах именно то, что нужно для ЕГЭ
-
Спасибо!