Walter White 07
Пользователи-
Постов
53 -
Зарегистрирован
-
Посещение
Весь контент Walter White 07
-
Здравствуйте! Реагирует ли бензамид с ацетилхлоридом? Получается ли соль? Если да, можно её нейтрализовать щёлочью?
-
Здравствуйте! Я знаю, что можно алкилировать NH3 с помощью CH3Cl до [CH3NH3]Cl, а также [CH3NH3]Cl может прореагировать с ещё одной молекулой NH3 в случае его избытка до CH3NH2 + NH4Cl Собственно вопрос: если CH3NH2 + CH3Cl даст [CH3NH2CH3]Cl, то возможно ли взаимодействие [CH3NH2CH3]Cl с ещё одной молекулой CH3NH2 до CH3NHCH3 и [CH3NH3]Cl? И ещё вопрос: [CH3NH2CH3]Cl реагирует с NH3?
-
Ничего подобного, даже школьная химия утверждает, что амфотерные оксиды/гидроксиды реагируют только с высшими кислотными оксидами, которым соответствуют сильные кислоты, по типу P2O5, SO3, N2O5 и т.д., а также с сильными кислотами (по причине того, что соль, образованная слабым гидроксидом и слабой кислотой подвержена необратимому гидролизу) Если учитель говорит, что Al2O3 реагирует с CO2, то выбрасывайте эту информацию из головы! Что касается нерастворимых основных оксидов, то они тоже реагируют лишь с высшими кислотными оксидами, однако соответствующие им основания могут с CO2 дать основные соли Нерастворимые основные оксиды и сответствующие им основания реагируют со всеми кислотами, кроме кремниевой P.s. именно так нас готовит учитель к ЕГЭ
-
Но ведь насыщенный раствор, содержащий 138г KNO3, будет весить 238г, т.е. 138г KNO3 на 100г H2O при 70°С Мы имеем 400г насыщенного раствора, значит в нём 232г KNO3 (по пропорции) Окей, 400г раствора, из которых 168г H2O и 232г KNO3, т.е. 232г KNO3 на 168г H2O Вода никуда не девается, нужно найти, сколько KNO3 при 20°С растворяется в 168г воды 31,6 в 100, значит Х в 168, Х=53 Окей, в 168г H2O при 20°C растворяется 53г KNO3, у нас изначально было растворено 232г KNO3 в 168г H2O, значит в осадок выпадут лишние 179г P.S. если считать с точностью до сотых, то ответ 178,82
-
Слишком интересно, спасибо!
-
Здравствуйте! Мне очень интересно, действительно ли в реальности реакции протекают так, как учат для ЕГЭ, а именно: Действительно ли получится толуол, если замешать бензол с AlCl3 и начать пробулькивать через него CH3Cl? Действительно ли получится бутан, если хлорэтан через натрий пропустить как-то Действительно ли получится 1,3,5-триметилбензол при пропускании пропина над активированным углем?
-
Правда вот это не ясно, ведь у катиона меди 2+ конфигурация 3d9 4s0 4p0, свободно всего лишь 4 орбитали
-
Ааа, господи, всё так просто оказывается, спасибо большое! Только наверняка вы имели виду незаполненные 4p орбитали, да, так и есть, действительно, спасибо! Разобрался, понял, спасибо большое! Жду не дождусь поступления на химфак!
-
Здравствуйте! В школе не преподают химию профильного уровня, а разобраться хочется: Al в возбужденном состоянии имеет три неспаренных электрона: 3s1 3p2 Каждый из этих электронов может спариться с неспаренным электроном кислорода в OH-, получится Al(OH)3, и т.к. кислород более электроотрицателен, то он перетянет на себя электроны Al, а это значит, что у Al теперь 3s0 3p0, свободные орбитали значит, в 3s0 может встать неподеленная электронная пара кислорода в ещё одной OH-, получится ион [Al(OH)]4-, верно? Тогда как объяснить образование [Cu(H2O)6]2+, откуда у меди 6 свободных орбиталей? Очень сложно эту тему понять Кстати, был бы очень рад какой-либо литературе
-
Горение сульфидов активных металлов: что образуется?
Walter White 07 опубликовал тема в Решение заданий
Здрасте! Я знаю, что сульфиды малоактивных металлов по типу CuS, PbS, Al2S3, FeS, FeS2 и т.д. горят с образованием оксида металла и SO2 А что происходит в случае сульфидов активных металлов? К примеру обжиг Na2S? Возможно ли образование сульфита? А сульфата возможно? А сульфит натрия будет гореть до сульфата? -
Здравствуйте! Объясните мне, что такое внешний энергетический уровень? Cu 1s2 2s2 2p6 3s2 3p6 4s1 3d10 Внешним является ВНЕШНИЙ? Т.е. у меди на внешнем энергетическом уровне 1 электрон, верно? Почему http://ru.solverbook.com/spravochnik/ximiya/11-klass/stroenie-atoma/cink/ здесь пишут, что Cl и Mn имеют одинаковое количество электронов на внешней электронной оболочке, ведь у Cl внешняя оболочка из 3s и 3p подуровня, на которых 7 электронов, а у Mn внешняя оболочка 4s, на которой 2 электрона!
-
w(в-ва)=(m(в-ва)/(m(р-ра)))×100% Мы не знаем ни w(в-ва), ни m(в-ва), ни m(р-ра), но знаем, что если к этой системе добавить 100г H2O, то w(в-ва) станет равна 8,4% Пусть m(в-ва)=x, m(р-ра)=y, тогда: x/(y+100)=0,084 Для решения такого уравнения нужно ввести ещё одно уравнение, чтобы составить систему уравнений и найти x и y. Мы знаем, что если отнять от системы 10г H2O, то w(в-ва) станет равна 15%. Запишем это: x/(y-10)=0,15 Составим систему уравнений: x/(y+100)=0,084 x/(y-10) =0,15 Упрощаем: x=0,084y+8,4 x=0,15y-1,5 Находим, что x=21, y=150 Находим, что m(в-ва)=21г, m(р-ра)=150г Это я к тому, что чтобы решать химические задачи, нужно владеть навыками вычисления, уметь преобразовывать какие-либо устные химические данные в алгебраические выражения, пусть и простейшие, а самое главное иметь химическую логику, дабы понимать, что из чего вытекает, что что значит и т.д., такое нарабатывается только благодаря нарешиванию различных задач
- 3 ответа
-
- 2
-

-

-
Реагируют ли карбонильные соединения с аминами? А какие условия реакции?
-
По поводу последних реакций: Смотрите, есть натрий, он, по правилам природы, отдаёт кому-то один электрон. Есть хлор, он, по правилам природы, любит принимать от кого-то один электрон. Натрий отдаёт электрон хлору, получается NaCl, где Na отдал электрон и стал положительно заряженым, Cl принял и стал отрицательно заряженым, вот они и притягиваются друг к другу, образуя молекулу NaCl. Хлор существует в виде молекул Cl2, а значит на такую молекулу нужно 2Na: Na + Cl2 = 2NaCl Фосфор любит отдавать 3 электрона, кислород любит принимать 2 электрона, значит на 2 фосфора (в сумме отдадут 6 электронов) нужно 3 кислорода (в сумме примут 6 электронов) Но кислород существует в виде молекул O2! Значит на 4 фосфора нужно 3 молекулы O2: 4P + 3O2 = 2P2O3 А если кислорода много, то фосфор отдаст целых 5 электронов: 4P + 5O2 = 2P2O5, то, сколько электронов отдаёт или принимает элемент - отдельная тема Не знаю, зачем я это все пишу, вам нужно изучать химию с нуля, дабы понимать самые базовые правила
-
Как так? Изучение химии начинают с основ, правил, законов... Должны объяснять, что и с чем реагирует, а потом уже давать задания. Читайте учебник, изучайте теорию от начала и до конца, разбирайтесь... P.s. CO2 + Ca(OH)2, взаимодействие кислотного оксида с щелочью, образуется соль CaCO3 + H2O
-
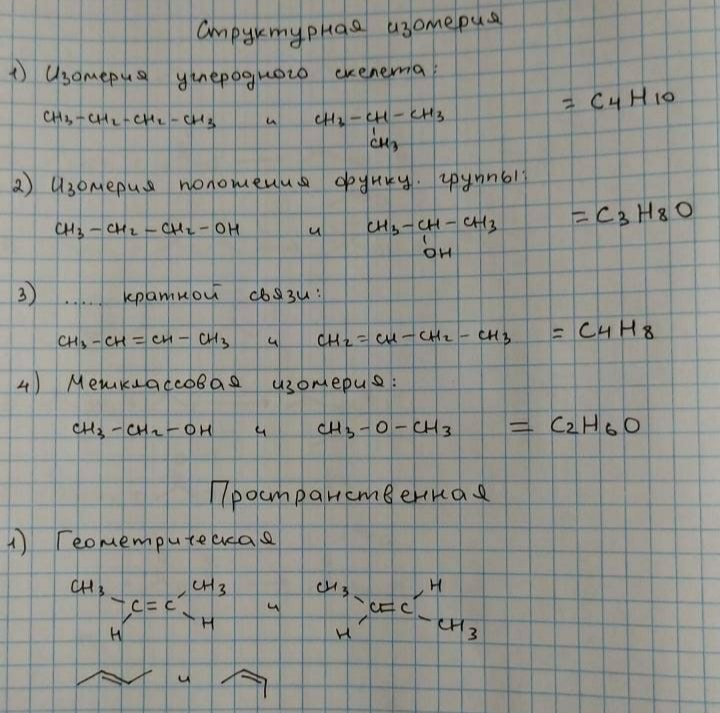
Мое фото мало что даст тебе, особенно пространственная изомерия, тут нужно разбираться, плюс забыл про оптическую написать, загугли в инете, там полно инфы. От себя скажу пару слов: Изомеры - вещества, имеющие одинаковый качественный и количественный состав, однако разное строение. Пропанол-1 и пропанол-2 имеют один и тот же качественный (одни и те же атомы) и количественный (сколько атомов углерода, водорода и кислорода в одной, столько и в другой), но отличаются строением
- 2 ответа
-
- 2
-

-

-
Смесь C2H4 и C2H2 1) C2H4 + H2 = C2H6 2) C2H2 + 2H2 = C2H6 Пусть V1(C2H4)=X, V2(C2H2)=Y V1(C2H4)+V2(C2H2)=X+Y=50л По уравнениям реакций: V1(H2)=V1(C2H4)=X V2(H2)=2V2(C2H2)=2Y V1(H2)+V2(H2)=X+2Y=70л Составим и решим систему: X+Y=50 X+2Y=70 Находим, что X=30, Y=20 Значит V1(C2H4)=30л, V2(C2H2)=20л Объемная доля C2H4=30/50=60% Объемная доля C2H2=20/50=40% 10л исходной смеси будет содержать: 60% C2H4 и 40% C2H2, значит: 10л исходной смеси будет содержать: 6л C2H4 и 4л C2H2 3) C2H4 + 3O2 = 2CO2 + 2H2O 4) 2C2H2 + 5O2 = 4CO2 + 2H2O По уравнениям реакции: V3(O2)=3V3(C2H4)=18л V4(O2)=2,5V4(C2H2)=10л Общий необходимый объем O2 = 28л Имеем уважение и ставим лайк на ответ
-
Здравствуйте! В пособии по химии пишут, что HClO3 окисляет P до P2O5: 5HClO3 + 6P = 3P2O5 + 5HCl Что за бред? Реакция же происходит в растворе, P2O5 будет реагировать с водой с образованием H3PO4!!! Почему реакция не выглядит так: 5HClO3 + 6P + 9H2O = 6H3PO4 + 5HCl
-
Бутадиен и дивинил - одно и то же вещество, т.к. это разные названия одного и того же вещества Метилбензол и пропилбензол - гомологи, т.к. вещества одного класса, отличающиеся на одну -CH3 группу Метилциклопропан и бутен-2 - изомеры, т.к. имеют одинаковую молекулярную формулу - C4H8 Аминоуксусная кислота и нитроэтан - изомеры, т.к. имеют одинаковую молекулярную формулу - C2H5NO2
- 1 ответ
-
- 1
-

-
Под описание подходит KMnO4, ибо именно его раствор при взаимодействии с KNO2 в кислой среде обесцвечивается (= MnSO4 + K2SO4 + NaNO3 +H2O, бесцветный раствор), в щелочной приобретает зелёный окрас (за счёт образования K2MnO4, ну и + NaNO3 + H2O ещё), а в водной выпадает бурый осадок диоксида марганца (= MnO2 + KOH + NaNO3)
- 1 ответ
-
- 1
-

-
Здравствуйте! Проблема в понимании протекания ОВР: какие вещества вступают в ОВР, какие продукты будут образовываться. Я знаю про KMnO4/K2Cr2O7/K2CrO4 в разных средах, знаю про HNO3/H2SO4 с металлами и т.д., т.е. общие школьные правила я знаю. Проблема в другом: то HNO3 даёт NO2, то NO при взаимодействии с НеМе, либо с какими-то соединениями, то HBrO3 переходит в HBr, то в Br2, и не ясно, от чего это зависит. Училка говорят, что зависит от силы восстановителя, но как понять, кто сильнее? PH3, или тот же P2O3? А HNO3 с ними до NO2, или NO восстановится? Как понять? Я бы запомнил, но запомнить абсолютно все невозможно! Мб есть литература, изучив которую я научусь прогнозировать продукты ОВР?
-
Смотрите: NaOH + HCl = NaCl + H2O На 1 моль NaOH нужно 1 моль HCl Получаем 1 моль NaCl и 1 моль H2O Количество хлорид-ионов = количеству NaCl = 1 моль Мы имеем 0,2 моль NaOH, если добавить 0,2 моль HCl, то получим 0,2 моль NaCl, т.е. 0,2 моль хлорид-ионов, однако гидроксид-ионов не получим, их источником является NaOH, значит нужно, чтобы в растворе остался NaOH... На 0,2 моль NaOH надо взять 0,1 моль HCl, чтобы получить 0,1 моль NaCl, останется 0,1 моль непрореагировавшего NaOH В итоге имеем одинаковое количество хлорид- и гидроксид-ионов, а значит масса HCl = 0,1×36,5=3,65г, следовательно массовая доля кислоты 3,65/73=0,05=5%