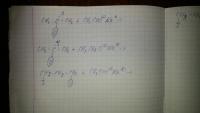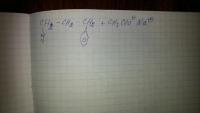Поиск
Показаны результаты для тегов 'Уравнения'.
Найдено 40 результатов
-
В каких кислотах можно растворить медь? составить уравнение соответствующих реакций и уравняйте их методом электронного баланса.
-
Спасайте. Заранее спасибо)
-
Определите, к какому типу относится покрытие, нанесенное на сталь (потенциал стали примите равным стандартному потенциалу железа φ(Fe(2+) /Fe) = -0,440 В). Напишите уравнения процессов, возникающих в случае разрушения покрытия: а) в морской воде, pH = 8; б) в воде системы отопления (деаэрированная среда). В какой среде коррозия протекает интенсивнее? Ответ подтвердите расчетом ЭДС коррозионного элемента,приняв активность ионов корродирующего металла равной 10^(‒6). Покрытие: Mn; φ= −1,175
-
помогите пожалуйста с уравнением: 1. СаСO3 - X - Y - C2h2 - Z - толуол - бензилхлорид(KOH\H2O) - ... (CuO,t) ...
-
- 1 ответ
-
- пропионовая кислота
- превращения
-
(и ещё 2 )
C тегом:
-
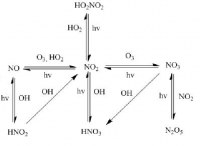
Предмет физико-химические процессы в техносфере, задание дали на всю группу, но никто ничего не понимает, хоть и изучали химию 2 семестра. Прошу помощьи, подсказок, советов по отдельным заданиям. Выполните задание: 1. Пользуясь схемой, составьте уравнения реакций, происходящих в атмосфере вблизи источника выбросов оксидов азота (например, котельной) в солнечную безветренную погоду. В атмосфере постоянно присутствуют: озон, радикалы ОН· и НО2. 2. Составьте схемы реакций превращения первичных продуктов: NO, N2O3, N2O5, HNO2, HO2NO2, NO3(реакции, которые идут при λ < 290 нм отбрасываются). 3. Пользуясь справочными данными определите константы скоростей реакций при соответствующих температурах (ориентируясь на температурный градиент атмосферы). 4. Из основных циклов превращений поллютантов выберите самые быстрые реакции, отвечающие за трансформацию основной массы атмосферной примеси. 5. Сделайте вывод, ответив на вопрос: какие продукты цикла оксида азота являются основными компонентами смога? Общая схема химических превращений оксидов азота в атмосфере: (рис в прил) Решите расчётные задачи: 1 Сравните скорости выведения из атмосферы молекул метана при их взаимодействии с гидроксидным радикалом в приземном слое и на высоте верхней границы стандартной тропосферы. Концентрация метана на этих высотах равна 1,7 млн-1. Энергия активации и предэкспоненциальный множитель для реакции взаимодействия метана с ОН-радикалом равны 14,1 кДж/моль и 2,3 см3 • с-1 соответственно. Концентрации гидроксидных радикалов на этих высотах принять равными: [ОН]1 = 5 • 105 см-3, [ОН]2 = 2 • 106 см-3. 2. Определите, каким будет соотношение скоростей процессов газофазного и жидкофазного окисления SО2, если принять, что основной вклад вносят следующие реакции: SО2{г) + ОН(г) ? HSO3(г) (1) SО2{р-р) + Н2О2(р-р) ? Н2SO4(р-р) (2) Константы скоростей реакций окисления: k1 = 9∙10-13 см3 ∙ с-1; k2 = 1 ∙ 103 л ∙ моль-1 ∙ с-1. Концентрации примесей в газовой фазе составляют: [ОН] = 5 ∙106 см-3, [sO2] = 10-4 % (об.); [Н2О2] = 10-7 % (об.). Расчеты провести для атмосферного воздуха, имеющего температуру 25о С и содержащего 0,00001 г свободной воды в каждом литре воздуха, Считать, что при растворении в воде концентрация SО2 в газовой фазе не меняется. Газы считать идеальными и подчиняющимися закону Генри. Давление принять равным 1 атм. 3. Какое было бы отношение концентраций NO и NO2 в равновесной системе на высоте 11 км, если их взаимную трансформацию можно было бы ограничить следующими реакциями: М + NO + О = NO2 + М* , если М — молекулы кислорода NO2 + О = + NO + О2? Константы скорости реакций на этой высоте равны соответственно: k1 = 8 ∙ 10-32 см6 ∙ с-1,; k2 = 1∙10-12 см3∙с-1.
-
- атмосферные процессы
- органика
- (и ещё 3 )
-
Если эти ярко-оранжевые кристаллы внести в пламя спиртовки, мы увидим фиолетовое окрашивание пламени. К таким же кристаллам прилили серную кислоту концентрацией 97%. Выпал осадок красного цвета, который отфильтровали и высушили, а затем добавили этанол. Произошло воспламенение, выделился газ, который пропустили через известковую воду, и образовался зеленоватый порошок. Напишите уравнения происходящих реакций. Помогите с данным заданием, буду очень благодарна!
-
составить окислительно-восстановительные реакции: K2S + NaOCl = S + K2SO4 + (просто интересно, если в левую часть добавлю H2SO4, а в правую- NaCl, это законно?) NaBr + CaCl(OCl) + H2O = Br2 + CaCl2 + (в этой реакции очень смущает CaCl(OCl), про него даже в интернете нечего не найти, он растворяется, эго можно разделять на ионы?)
-

Используя потенциалы, допишите уравнения реакций, составив к ним электронно-ионные схемы
Гость опубликовал тема в Решение заданий
Используя потенциалы, допишите уравнения реакций, составив к ним электронно-ионные схемы. Для реакции металлов с H2SO4(конц) и HNO3, значение потенциала окислителя более 1В. Al+NaOH+H2O+O2 -
Соединение Х с брутто-формулой C8H7NO обладает характерным запахом и часто является причиной тяжелых и даже смертельных пищевых отравлений. Дело в том, что в желудочном соке это соединение расщепляется на два компонента А (высокотоксичен) и Б. Первый из них (А) может быть легко идентифицирован добавлением содержимого желудка к подщелоченному раствору железного купороса, содержащего примесь сульфата железа (III), с последующим нагреванием, фильтрованием и подкислением разбавленной соляной кислотой, что сопровождается выделением хлопьевидного осадка синего цвета. Второй компонент (Б) под действием щелочей превращается в два новых соединения (В и Г), первое из которых (В) легко окисляется во второе (Г). Соединение Г хорошо растворяется в растворе щелочи и повсеместно используется в пищевой промышленности в качестве консерванта. Интересно, что при взаимодействии соединения Б с раствором соединения А в щелочи не образуется вновь соединение Х, а получается новое вещество Д. Необходимо определить строение и названия соединений и составить уравнения всех приведенных выше реакций.
- 2 ответа
-
- органика
- азотсодержащие соединения
- (и ещё 4 )
-
ZnCl2+(NH4)2[Hg(SCN)4] Участие комплексных ионов в реакциях обмена
Артем-метра опубликовал тема в Работа
Доброе утро. Добрый день. Добрый вечер. ZnCl2+(NH4)2[Hg(SCN)4] Необходимо найти: 1.Молекулярное уравнение. 2.Ионное уравнение. 3.Наблюдаемое явление. 4.Заряд комплексообразователя. 5.Координационное число комплексообразователя. -
Необходимо сделать: Bi(NO3)3+KI 1)Молекулярное уравнение 2)Ионно-молекулярное уравнение 3)Ионизация комплекса в растворе 4)Уравнение диссоциации комплексного иона 5)Кn константа нестойкости
-
ZnCl2+(NH4)2[Hg(SCN)2] Молекулярное и ионное уравнения
Артем-метра опубликовал тема в Решение заданий
Необходимо выполнить: ZnCl2+(NH4)2[Hg(SCN)2] Молекулярное уравнение Ионное уравнение Заряд комплексообразователя Координационное число комплексообразователя -
MnO2+K2SO3+H2SO4= MnO3F +H2O= Na2SO3+Na2MnO4+H2O= K2MnO4+MnSO4+H2O= KMnO4+SO2+H2O= Re+H2O2+NH3= MnF6+KF= ReS2+O2=
-
Помогите пожайлуста записать эти цепочки превращений в полное ионное уравнение и если не трудно, проверьте правильно ли я записал цепочки. это -- вместострелочки 1.Na2O+H2O--NaOH 2.NaOH+HCl--NaCl 3.NaOH+H2OSO4--NaSO4 4.NaOH+HNO3--NaNO3 5.NaOH+H3PO4--Na3PO4
-
Привет,нужно записать уравнения реакции иллюстрирующие следующие превращения. Al->AlCl3->Al(OH)3->Al2O3->Al А то вообще не могу понять как решать уравнения с этими стрелками. Спасибо за помощь!
- 3 ответа
-
- неорганическая химия
- жесть боль
-
(и ещё 2 )
C тегом:
-
-
В химии полный "0" 1.Составте молекулярные и ионно-молекулярные уравнения реакций взаимодействий в растворе между веществами: 1)Сr(OH)3 и Na2CO3 2)Zn(NO3)2 и LiOH 3)FeCO3 и HCl 2.Составьте по три молекулярных полных ионных уравнений реакций,которые выражаются сокращенными ионными уравнениями: H(сверху + ) + OH (сверху - )= H20
-
1) Вычислите pH формиатного буферного раствора, содержащего 0,5М муравьиной кислоты и 0,8М формиата натрия. Какова буферная емкость данного раствора? 2) Вычислите растворимость оксалата кальция в 1М уксусной кислоте. 3) Напишите уравнения реакций Ba(OH)2 + H2CO3 SrCl2 + (NH4)2SO4 BaC2O4 + CH3COOH NH4Cl + H2O Li + N2 (при нагревании) Спасибо.
- 1 ответ
-
- Раствроимость
- Уравнения
-
(и ещё 2 )
C тегом: