Поиск
Показаны результаты для тегов 'коррозия'.
Найдено 58 результатов
-
После испытания в камере соляного тумана (5%) спустя уже 48ч на пленке появляются пузыри. Краска ВД-АК. Что пересмотреть в рецептуре, для того, чтобы их избежать? требования заказчика - 196 ч
-
Избавить копаный метал от ржавчины в домашних условиях
faver опубликовал тема в Неорганическая химия
Здравствуйте. В наличии имеются копаные вещи (железные) со следами коррозии: старинные замки, ножи, топоры и тому подобные. Цель: избавить от ржавчины простым способом, но максимально сохранить сам металл. На просторах интернета нашел такой способ (и думаю следовать ему): Раствор лимонной кислоты (5-7%), прокипятить 10 минут. В моющий раствор (хоть лимонка, хоть фосфорка) обязательно добавлять 0,1% ингибитора кислотной коррозии (бензотриазол, КИ-1, каптакс, на худой конец обычный уротропин). В моющий раствор обязательно добавлять 0,5% НПАВ (лучше всего лаурилдиметиламиноксид). Далее деталь промыть водой и сразу же погрузить в 3% раствор нитрита натрия с добавкой 1% кальцинированной соды (рН должна быть 8-9). После этого поверхность не будет покрываться слоем ржавчины на воздухе за счет образования тонкой пленки магнетита. Вид изделия просто отличный - матовый свинцовый цвет. Но есть вопросы: 1. Что лучше добавлять как ингибитор коррозии: бензотриазол или уротропин? БТА добавлять в сухом виде- порошке?; 2. Чем можно заменить вот этот компонент: 0,5% НПАВ (лаурилдиметиламиноксид) ? не нашел его в продаже; 3. В качестве нитрит натрия подойдет вот этот компонент "Нитритная соль - смесь пищевой соли с пищевой добавкой Е250, посолочная смесь 0,6% NaNO2 нитрит натрия" ? Раствор для пассивации изготавливается на обычной воде? И сколько необходимо времени держать в растворе предмет? 4. Подойдет ли данный способ очистки для других металлов: алюминия (если побелел или потускнел), меди (если позеленел), бронзы, латуни? Спасибо. -
Абсолютно не имею понятия, как решать эти задачи... Буду рад, если поможете. Задание №1: Сепаратор подшипника из латуни марки ЛЦ40С на основе меди и цинка с добавлением свинца и сурьмы покрыт слоем кадмия. 1. Определите тип покрытия относительно основного металла. 2. Рассмотрите два возможных варианта протекания процесса коррозии изделия при частичном нарушении покрытия (царапина): а) в атмосферных условиях; б) в растворе разбавленной серной кислоты. 3. Для каждого случая составьте уравнения электродных процессов. 4. Определите продукты коррозии. 5. При кислотной коррозии определите металл, на котором происходит локализация катодного процесса. Задание №2: Резьбовое крепежное изделие из инструментальной стали на основе железа, содержащей кобальт и медь, покрыто цинком. 1. Определите тип покрытия относительно основного металла. 2. Рассмотрите два возможных варианта протекания процесса коррозии изделия при частичном нарушении покрытия (царапина): а) в атмосферных условиях; б) в растворе разбавленной серной кислоты. 3. Для каждого случая составьте уравнения электродных процессов. 4. Определите продукты коррозии. 5. При кислотной коррозии определите металл, на котором происходит локализация катодного процесса.
-
-
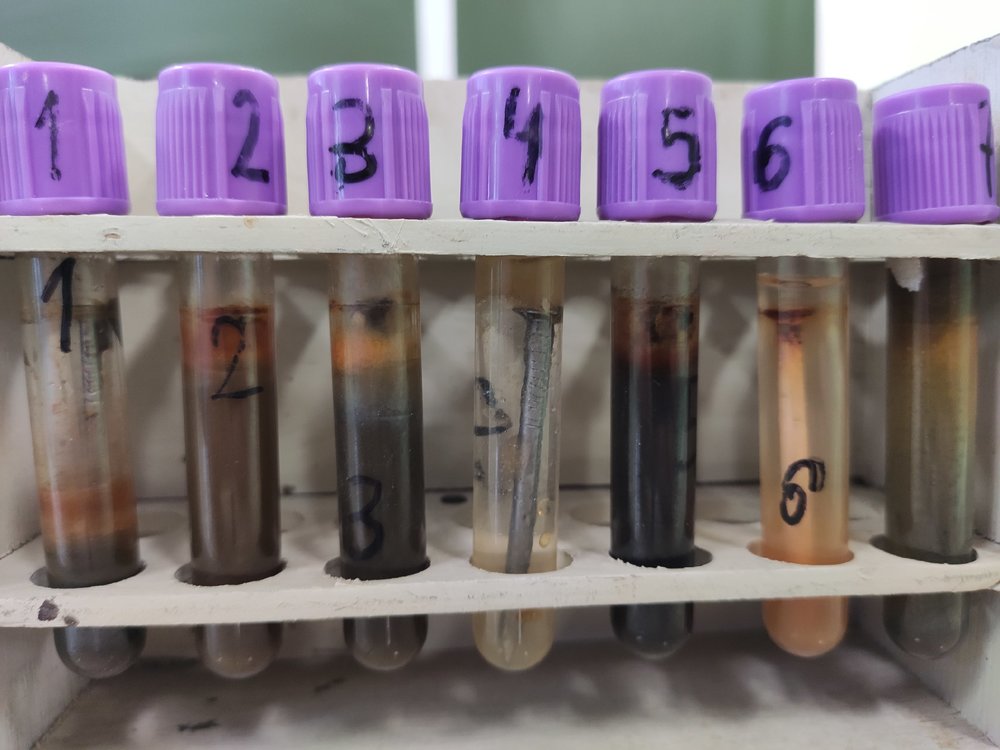
Люди, нужна помощь. Почему гвоздь ржавеет в кислоте и почему в дистиллированной воде лучше происходит коррозия, чем в обычной воде . Гвоздь, наполненный наполовину H2O 2. Гвоздь, погруженный полностью в воду 3. Гвоздь в дистиллированной в воде 7. в растворе кислоты
-
Всем здравствуйте! Я в этом деле новенькая, если кто-то работал с этим, то подскажите пожалуйста в некоторых вопросах. 1. Для травления образцов перед испытанием нужно использовать такие реактивы, как: аммоний фтористый, азотная кислота 65% и дистиллированная вода. в какой последовательности смешивать все эти реактивы и можно ли это делать сразу в колбе, в которой в дальнейшем планируется храниться этот раствор, так как его очень большой объём? 2. образцы сразу нужно шлифовать и полировать Перед испытанием , а потом травить или наоборот? 3. Нужно ли закрывать холодильник Хлоркальцевой трубкой? 4. по окончанию испытания снова отшлифовать и протравить, правильно понимаю? 5. И как долго может храниться приготовленный раствор для испытания? P.S. Не указала, что метод испытания АМУ заранее всем огромное спасибо!
-
Услуги по исследованию материалов (коррозионностойкость) на потенциометре рассмотрим все варианты. kravchenko-v@yandex.ru
-
- услуги
- исследования
-
(и ещё 1 )
C тегом:
-
-
- коррозия
- защита от коррозии
- (и ещё 3 )
-
Здравствуйте, помогите сделать задание. Как происходит коррозия a)лужёного железа и b)лужёной меди на влажном воздухе, если покрытие повреждено? Написать схему коррозии гальванического элемента и уравнения реакции катода и анода.
-
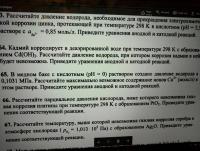
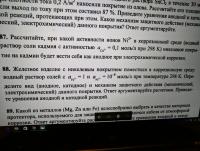
Прошу помочь решить 4 задачи по химии на тему "Коррозия". Надо решить номера: 64,88,65,85. Фотографии заданий в приложенных файлах. Буду КРАЙНЕ признателен вам)))
-
- коррозия химия
- химия
-
(и ещё 2 )
C тегом:
-
Опишите, как протекает коррозия технического цинка (содержит примеси железа, меди, свинца и др.) на воздухе. Напишите процессы, протекающие на анодных и катодных участках.
-
Подскажите пожалуйста вещество или вещества, которые могут ускорить процесс коррозии. Это нужно для разбрасывания с беспилотного летательного аппарата с целью выведения из строя боеприпасов к гаубицам ВСУ.
-
Определите, к какому типу относится покрытие, нанесенное на сталь (потенциал стали примите равным стандартному потенциалу железа φ(Fe(2+) /Fe) = -0,440 В). Напишите уравнения процессов, возникающих в случае разрушения покрытия: а) в морской воде, pH = 8; б) в воде системы отопления (деаэрированная среда). В какой среде коррозия протекает интенсивнее? Ответ подтвердите расчетом ЭДС коррозионного элемента,приняв активность ионов корродирующего металла равной 10^(‒6). Покрытие: Mn; φ= −1,175
-
Добрый вечер. Подскажите, пожалуйста, решение данной задачи. Какой металл может служить протектором при защите железа от коррозии в водном растворе с рН 10 в контакте с воздухом? Напишите уравнения реакций протекающих процессов Как я понимаю, нужно выбирать те металлы, что левее в ряду. Алюминий подходит. У нас среда щелочная с доступом кислорода. Тогда выходит: Анодная реакция: Al = Al3+ + 3e Катодная реакция: O2 + 2H2O + 4e = 4OH- Суммарная реакция: 4Al + 6H2O + 3O2 = 4Al(OH)3 Верно?
-
Добрый вечер. Помогите с решением: Составить уравнение анодных и катодных процессов, протекающих при коррозии Sn-Pb сплава в растворе хлорида натрия при контакте с воздухом. Предложить анодное и катодное покрытие для сплава. Какие процессы будут иметь место при коррозии данного сплава в случае нарушения сплошности анодного покрытия? Хотя бы скажите, что делать с хлоридом натрия?
-
Имеется железная пластина, покрытая слоем никеля.Защитит ли никель железную пластину от коррозии при нарушении целостности покрытия? Написать реакции. Ответ обосновать.
-
1)дайте схему коррозии луженого железа и луженой меди в кислой среде. 2)распишите уравнения протекающие при коррозии следующих гальванопар: Cr/H2O, O2/CO; Cr/HCl/CO
-
Привет всем!помогите плиз срочно! Железо покрыто хромом. Какой из металлов будет корродировать в случае нарушения поверхностного слоя покрытия в атмосфере промышленного района, где влажный воздух содержит, в частности, оксид углерода (IV), оксид серы (IV) и сероводород? Составьте схемы протекающих химических реакций. Спасибо всем!!!!!!!!!!!!!!
-
Коррозия стали и влияние механических напряжений на коррозию
LeonidP опубликовал тема в Решение заданий
Помогите, пожалуйста, с выводом к опыту. Появление малинового цвета (там где механических напряжений практически нет) обусловленно реакцией фенолфталеина на среду. А голубая окраска (там где присутствуют механические напряжения) - так называемая "берлинская лазурь". Нужно объяснить почему так происходит? Дали подсказку: вся "фишка" в углероде в сплаве стали.-
- коррозия
- электрохимия
-
(и ещё 2 )
C тегом:
-
зависимость скорости коррозии стали от напора реагентов
cynepnaxa опубликовал тема в Неорганическая химия
Привет всем! Помогите новичку пожалуйста. Хочу понять, как замедляется коррозия стали, если замедлить поступление пара и кислорода к поверхности, например нанеся слой полимера. Они все газопроницаемы в различной степени. Наверно для начала сколько надо воды и кислорода чтобы окислить 1 кг железа. -
1.Рассчитать изменение энергии Гиббса и определить, возможно ли окисление меди в воздухе и кислороде при температуре 1073 К по реакции если давление диссоциации ее оксида при этой температуре 2.Оценить коррозионную стойкость алюминия на воздухе при температуре 757 К. Образец алюминия поверхностью, равной 17*10^(-3) м^2, имел массу до испытания 72,4611 г. , после 204 ч. окисления на воздухе при температуре 757 К его масса составила 72,4635 г. 3.Определить по уравнению жаростойкости глубину коррозионного разрушения стали 12Х2МФБ за 7000 ч. окисления в продуктах сгорания природного газа при температуре 873 К.
-
Укажите вид и механизм защитного действия покрытий: а)оцинкованное олово; б) посеребренная медь. Напишите уравнения электродных процессов и суммарной реакции, протекающих при атмосферной коррозии в случае нарушения целостности указанных покрытий.
-
Алюминиевое изделие в контакте со свинцовой пластиной находится при 298К в деаэрированном растворе с рН=6 и активностью ионов корродирующего металла, равной 10^(-4) моль/л. Определите металл, который подвергается разрушению. напишите уравнения электродных процессов и суммарной реакции. Рассчитайте ЭДС коррозионного элемента и ΔrG(298) коррозионного процесса.