Поиск
Показаны результаты для тегов 'практика'.
Найдено 7 результатов
-
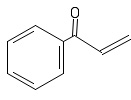
Привет всем Форумчане !!! Вопрос ! Есть такая структура. Через какие вещества возможно ее синтезировать ?
-
Здравствуйте химики-практики! Задался вопросом узнать окончательно к какому же виду по проявляющим себя свойствам проявляют себя следующие элементы: Бериллий, Магний, Цинк, Кадмий, Ртуть. Дело в следующем: поискав и посмотрев различного рода литературу по анализу и по химии выяснилось (и самое главное что до сих пор толком невыяснено) что в каждой книжке и справочнике или каком другом пособии даются "свои оценки" по отношении к этим элементам (и групы бора). Единого единогласия в литературе нет. Одни утверждают что они амфотерны, другие что они основания по Бору вообще не пойми что то ли гидроксид то ли кислота и т.п. В связи с чем было принято решение спросить на форуме у химиков-практиков, которые неоднократно работая с этими элементами пришли к однозначному выводу к какому класу их можно отнести. Если допустим они проявляют основные или амфотерные свойства, то в какой степени по мере уменьшения они относятся. Какой литературе (справочник, монография, книга, букварь) больше верить? К примеру химик-практик многократно испытывая на опыте элемент вычисляя ее рН и свойства, обращаясь к той или иной литературе сверялся и подтверждал свой результат. Существуют ли какие-то "эталоны" определения свойств элементов? Благодарю за расширеный и грамотный ответ!
- 29 ответов
-
- амфотерность
- основание
- (и ещё 4 )
-
Здравствуйте. Интересуют книги или методические издания о работе с газовыми хроматографами о практической работе с газовым хроматографом, например как избежать ошибок оператора, как повысить сходимость результатов, выбор шприцов, тонкости работы с теми или иными детекторами, выбор НЖФ в колонке и прочее. Спасибо за помощь!
-
Извиняюсь, "гуру" никак не являюсь, опровергнуть или предположит не могу, но усердно учусь, чтобы мочЪ . Есть такая чудесная работа в практикуме, "Определение молярной массы эквивалента металла". Ничего интересного, всё должно быть просто и понятно. Ну, без аккуратности, конечно, проблематично. Если кратко, проблема в следующем. Вроде как всё замерил, а (о, какая неожиданность) результаты не сходятся. Растворял алюминий в соляной кислот (достаточно концентрированной). Как правильно, по корочке, проводить опыт знаю. Разве что единственный грешок - терпения мало, не стал дожидаться, когда полностью остынет, а кислоты закинул сразу излишек(из-за этого и ищу погрешность). Нужно перечислить варианты, от чего возникла весьма приличная погрешность (причём очень приличная, от нужного результата превышен в два раза). Такая банальщина как "подняли бюретку, попал воздух" или "плохо закрепили пробирку, часть водорода не "промазало"" неинтересно, за этим следил тщательно. Мои варианты: изначальная неточность в измерении массы металла (брал около 3 сотых грамма, а весы показали только 2 "вещественных" знака после запятой) но таки столь большой разницы быть не должно; бюретка не имела ед. отрезок и шла на сужение (ладно, ед. отрезки просчитал вручную, да и сужение особой погоды не сделало бы); в формуле не учитывал P водяного пара (температура в комнате была около 22,5, но до неё не остужал); закинул около 3 мл "крепкой" кислоты из-за чего температура резко поднялась, энтальпия образования твёрдого 3-хлорида алюминия около 700 КДж, авось и с таким количеством что-то пошло наперекосяк (кислота закипела, 3-хлорид перешёл в свою "газовую" фазу", но сомневаюсь, что достигло температуры 180С*); хотя сразу залил прилично кислоты, большая часть осталось, может из-за резкого повышения температуры она что-то придумала; пробирка была влажной (внутри), может это на что-то повлияло. Изначально думал, что проблема в "нетерпеливости", те, что я так и не довёл до комнатной. Объём вышел около 68,6 мл. Не надо долго считать, чтобы придти к выводу, что это осуществимо или при очень малом давлении (минимум на момент опыта - 99,29 КПа), или при очень большой температуре (около 264 С* у меня вышло по расчётам). Но ведь при моём количестве вещества это... Это вообще возможно? Собственно, вопрос следующий - из-за чего такая большая погрешность (кроме "кривых рук") и если проблема в температуре, то возможно ли достижение необходимой T* с моим количеством вещества (где-то 0,0027 гр Al на 3 мл HCl).
-
Извиняюсь, "гуру" никак не являюсь, опровергнуть или предположит не могу, но усердно учусь, чтобы мочЪ . Есть такая чудесная работа в практикуме, "Определение молярной массы эквивалента металла". Ничего интересного, всё должно быть просто и понятно. Ну, без аккуратности, конечно, проблематично. Если кратко, проблема в следующем. Вроде как всё замерил, а (о, какая неожиданность) результаты не сходятся. Растворял алюминий в соляной кислот (достаточно концентрированной). Как правильно, по корочке, проводить опыт знаю. Разве что единственный грешок - терпения мало, не стал дожидаться, когда полностью остынет, а кислоты закинул сразу излишек(из-за этого и ищу погрешность). Нужно перечислить варианты, от чего возникла весьма приличная погрешность (причём очень приличная, от нужного результата превышен в два раза). Такая банальщина как "подняли бюретку, попал воздух" или "плохо закрепили пробирку, часть водорода не "промазало"" неинтересно, за этим следил тщательно. Мои варианты: изначальная неточность в измерении массы металла (брал около 3 сотых грамма, а весы показали только 2 "вещественных" знака после запятой) но таки столь большой разницы быть не должно; бюретка не имела ед. отрезок и шла на сужение (ладно, ед. отрезки просчитал вручную, да и сужение особой погоды не сделало бы); в формуле не учитывал P водяного пара (температура в комнате была около 22,5, но до неё не остужал); закинул около 3 мл "крепкой" кислоты из-за чего температура резко поднялась, энтальпия образования твёрдого 3-хлорида алюминия около 700 КДж, авось и с таким количеством что-то пошло наперекосяк (кислота закипела, 3-хлорид перешёл в свою "газовую" фазу", но сомневаюсь, что достигло температуры 180С*); хотя сразу залил прилично кислоты, большая часть осталось, может из-за резкого повышения температуры она что-то придумала; пробирка была влажной (внутри), может это на что-то повлияло. Изначально думал, что проблема в "нетерпеливости", те, что я так и не довёл до комнатной. Объём вышел около 68,6 мл. Не надо долго считать, чтобы придти к выводу, что это осуществимо или при очень малом давлении (минимум на момент опыта - 99,29 КПа), или при очень большой температуре (около 264 С* у меня вышло по расчётам). Но ведь при моём количестве вещества это... Это вообще возможно? Собственно, вопрос следующий - из-за чего такая большая погрешность (кроме "кривых рук") и если проблема в температуре, то возможно ли достижение необходимой T* с моим количеством вещества (где-то 0,0027 гр Al на 3 мл HCl).
-
Здравствуйте! Хочется провести ряд опытов с детьми. Но при этом не вдаваться в объяснения и подробности. А чтобы было наглядно и можно было что-то с собой унести на память. Может быть кто-то знает подобные реакции?
-
Производственная практика по фармацевтической технологии
Bydiamant опубликовал тема в Решение заданий
Необходим дневник и отчет по практике, с описанием каждого дня . Каждый день должно быть два рецепта на латинском языке,описание приготовление формы и пр.(все требования к рецептам и дневнику указаны в методичке по практике) ОНА ИМЕЕТСЯ , ПРЕДОСТАВЛЮ . Аптека в которой проходит практика является внутрибольничной, в ней НЕ изготавливаются лек. формы с ядовитыми веществами , суппозитории,пилюли. Изготавливаются формы необходимые для стационара. Время прохождения практики с 16 июня по 26 июля 2014 г. Прошу помощи! Заплачу деньги разумеется , нужно хотя бы рецепты . Если сделает кто-то все, плачу щедро. Очень нужно.