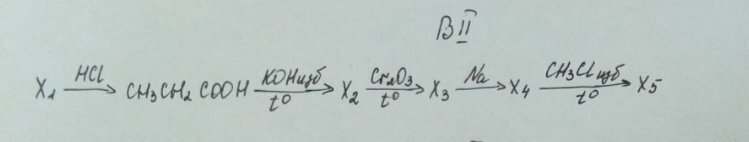Поиск
Показаны результаты для тегов 'химия'.
Найдено 399 результатов
-
Добрый день, Дорогие Химики! Моя компания занимается экспортом горного оборудования, преимущественно на Ближний Восток. Одному из основных клиентов требуется поставить антислеживатель для хлорида кремния. Как оказалось, химиков у нас в команде нет, а поиск на просторах интернета ничего полезного не дал. Обращаюсь на ваш форум за помощью. Подскажите, пожалуйста, есть у нас составы, производимые в промышленных масштабах с такими характеристиками, как на прикрепленной фотографии? Заранее огромное Спасибо!
-
Здравствуйте, подвернулась вот такая вот задача, очень буду рад подробному решению: При действии воды на 15 г смеси карбида и гидрида кальция выделился газ с плотностью по водороду равной 4,3. Определите массу гидрида кальция в смеси. Ответ округлите до целого числа. Правильный ответ: 7 Знаю, что при двух разных реакциях получается 2 разных газа, ацетилен и водород. Составил соотношение между ними, приравнял к количеству молей гидрида кальция и карбида, но выходит 9.5.
-
Молярная масса углерода= 100-51,064-29,787-6,343= 12,806% Моли водорода=6,383 Азота=2,127 Кислорода = 3,191 Углерода = 1,064 Истинная формула получилась CH6O3N2 что очень странно. Где я допустила ошибку? Помогите пожалуйста, спасибо
-
Помогите пожалуйста решить цепочку. Я думаю Х1 это соль - пропионат калия. Х2 не знаю, в ступоре. Помогите пожалуйста. Может там должен получиться бензол?
-
Здравствуйте! Продаю химическую посуду в ОТЛИЧНОМ состоянии или новую. В список продаваемого входит: холодильник для испарителя, воронки, мерные цилиндры, колбы, стеклянные фильтры. Фото посуды прилагаю: https://drive.google.com/drive/folders/1FMZ7476KUo6gp4V4JeJluTIhAIRVxu-G?usp=drive_link. Нахожусь в Москве, в пределах мкада можно встретиться для передачи посуды. Связаться со мной можно по телефону 8(926)617-42-17, прошу писать в вотсап или телеграм, звонок могу не услышать.
-
Группа компаний «Феникс» занимается скупкой химии с хранения, если на Ваших складах образовался объем химикатов с истекшим сроком годности, и вы не знаете, что делать с просроченной лабораторной химией или куда сдать химию, свяжитесь с нами по номерам, указанным в объявлении, и специалисты нашей компании помогут в решении данного вопроса. Приемка материалов с хранения производится на наших специализированных площадках по утилизации, так же наша компания осуществляет вывоз различных эмалей, грунтов с ваших складов. Мы покупаем соли, кислоты, окиси, порошки, смолы, пигменты, красители, металлические порошки, лабораторные остатки в любом количестве и качестве, бор аморфный, карбид бора, нитрид бора. Куплю неликвидный: парафин, модельные составы, воск в любом виде и в любом качестве, и многое другое. Оплату произведем: наличными и безналичными. Вывезем материалы с любого города РФ и стран СНГ. Телефон: +79638549177 Почта: 89638549177@mail.ru
-
Перед лаборантом находятся 3 пробы с неизвестными веществами. Пробы порошкообразны, причем одна из них является навеской чистого металла (второго по распространенности среди металлов в земной коре), вторая - многокомпонентным неорганическим веществом, кислая соль, применяемая в домашнем хозяйстве и пищевой промышленности и медицине (как нейтрализатор химических ожогов кислотами и для снижения кислотности желудочного сока), а третья природным пищевым полимером, который получают из картофеля и кукурузы. Известно, что при взаимодействии с CH₃COOH с одной из проб происходит бурная реакция с выделением газообразного вещества. При взаимодействии с водой другая проба приобретает необычные физико-химические параметры и меняет вязкость. Третья проба при контакте с парами воды выделяет бесцветный легкий газ и образует с веществом пробы двойной оксид, но только при высокой температуре (более 400 °С). Вычислите объем бесцветного газа, образовавшегося в ходе одной из описанных реакций и имеющего меньшую молекулярную массу, при условии, что масса продукта реакции составила 3370.0 граммов. Ответ дайте в литрах с точностью до десятых.
-
Помогите с задачами, пожалуйста Буду очень благодарна!!!!
-
- химия
- общая химия
- (и ещё 3 )
-
Моё авторское определение: Химический синтез — превращение совокупности веществ в другую совокупность веществ, имеющую большую цену в данной общественно-политической обстановке. Химический синтез — понятие экономическое, а не химическое Обычно KCl —> KClO3 рассматривают как синтез. Однако если я нашёл на помойке тонну бертолетовой соли, то для меня будет синтезом KClO3–>KCl.
-
-
Как правильно довести до метки окрашенные растворы? И Как довести прозрачные растворы?
- 1 ответ
-
- химия
- аналитическая химия
-
(и ещё 3 )
C тегом:
-
Как правильно довести до метки окрашенные растворы? И Как довести прозрачные растворы?
- 1 ответ
-
- аналитическая химия.
- лаборатория
-
(и ещё 2 )
C тегом:
-
Рассмотрите строение молекул метиллития и хлористого метила. Укажите наиболее существенное отличие связей C-Li и C-Cl. Назовите ионы, которые должны образоваться из этих молекул при гетеролитическом разрыве указанных связей. Опишите строение органических ионов.
- 3 ответа
-
- химия
- элементорганика
- (и ещё 2 )
-
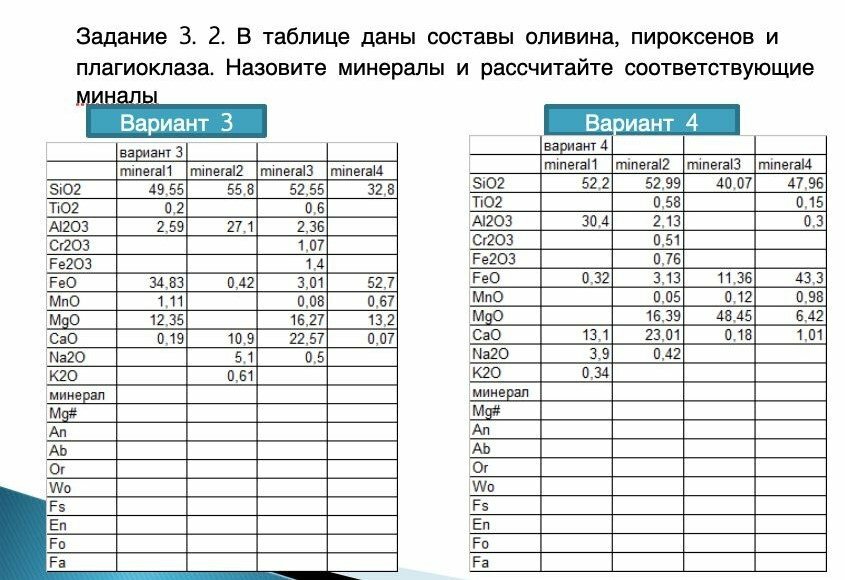
Петрология. Понятие о миналах, методы их расчета.
MironchelloGeolog опубликовал тема в Решение заданий
Доброго времени суток, передо мной встала сложная, но весьма интересная задачка по расчёту соответствующих миналов. Весь вечер сижу, не могу понять как это сделать. (Прикрепил файл с заданием) Буду безумно признателен, тому кто поможет или хоть как то подскажет))- 2 ответа
-
- петрохимия
- геология
-
(и ещё 2 )
C тегом:
-
Помогите решить задачу. Вычислить массу выпавшего осадка.
SpideCode опубликовал тема в Решение заданий
К 80 г раствора хлорида бария с массовой долей растворённого вещества 6,5% добавили избыток раствора серной кислоты. Вычислите массу выпавшего осадка. -
a) (CH3)2C=CH2 б) CH2=CH-CH-CH=CH+CH3 в)CH3-C тройная связь С-СН3 д) (СН3)3С-СН=СН2
-
- органическаяхимия
- химия
-
(и ещё 1 )
C тегом:
-
Скажите, пожалуйста, почему валентность Li и F равна 1, хотя Li в 1 группе, а F в 7?
- 1 ответ
-
- валентность
- химия
-
(и ещё 1 )
C тегом:
-
ХИМИЧЕСКАЯ ТЕРМОДИНАМИКА 3.1. Запишите реакцию взаимодействия указанного по варианту элемента с кислородом. Используя данные, рассчитайте энтальпию образования оксида. Данные для решения: Элемент: Al Масса элемента,г : 8,1 Формула оксида: Al2O3 Выделенное тепло, кДж: 251,4 Типовая задача 3.2. Для приведенной реакции рассчитайте: стандартный тепловой эффект процесса (кДж), изменение энтропии в ходе процесса (Дж/К), проанализируйте полученные результаты. Определите возможность протекания реакции в стандартных условиях, а также температуру, при которой система будет находиться в состоянии равновесия. Используя данные, рассчитайте энтальпию образования оксида. Данные для решения: Уравнение реакции: Al2O3(к)+3SO3(г)=Al2(SO4)3(к)
-
1. Вычислите потенциал электрода, на котором установилось равновесие O2 + 4Н++4ē ↔ 2Н2О при рН=4, РO2 = 1. Укажите тип электрода. Дайте его характеристику. В какую сторону сместится равновесие, если электрод будет работать в качестве анода? Как при этом изменится значение равновесного потенциала? 2. Условная схема электрода – Мn2+│Мn. Укажите тип электрода. Дайте его характеристику. При каких условиях потенциал этого электрода будет иметь стандартное значение? Составьте схему элемента, с помощью которого можно измерить стандартный потенциал укапанного электрода. Чему равна его ЭДС? 3. Сравните восстановительную активность цинкового электрода в щелочной и кислой среде при стандартных условиях. Составьте схему элемента из указанных электродов. Вычислите ЭДС. Как называется такой элемент? 4. Укажите химические реакции, которые можно использовать для организации гальванического элемента: 2FeCl3 + 2KI → 2FeCl2 + I2 + 2KCl; SО3 + H2O → H2SО4; Na2CO3 + 2HCl → 2NaCl +CO2 + H2O; H2 + Cl2 →2HCl. При использовании какой реакции ожидается максимальная ЭДС? 5. Составьте схему, напишите уравнения электродных процессов и токообразующей реакции, вычислите ЭДС элемента, составленного из электродов: 1)Cd в 0,01 моль/л CdCl2, α = 60%; 2)Pt в 0,1М NaOH при РH2=1. Укажите виды поляризации этих электродов. Как поляризация отражается на работе гальванического элемента?
-
Нужно решить вот эти 4 задания, пожалуйста помогите! 1.При взаимодействии 150 граммов раствора H2SO4 с массовой долей кислоты - 9% с 120 гр раствора BaCl2 с массовой долей 15% выпал осадок. Рассчитайте массу осадка. 2.При приливании раствора соляной кислоты к Алюминию, массой 113 грамма выделился газ. Найти объем газа. 3.При взаимодействии сплава магния и меди, массой 72 граммов, с соляной кислотой выделился газ. Найти массу газа, если массовая доля меди составляет 30%. 4.Найдите массу углекислого газа, выделившегося при взаимодействии 35 граммов мрамора с серной кислотой. Учтите, что массовая доля примесей в мраморе составляет 12%.
-
1. Thorpe's Dictionary of Applied Chemistry, 1946, Longmans, UK (английский язык, 7 томов) - 1500 руб. 2. Анорганикум. Перевод с немецкого. Москва, Мир, 1984 (2 тома) - 700 руб. 3. Органикум. Перевод с немецкого. Москва, Мир, 1992 (2 тома) - 700 руб. 4. N.L. Glinka. Genral Chemistry. Moscow, Mir, 1990 (английский язык, 2 тома) - 500 руб. 5. Элемениарный учебник физики. Под ред. Г.С. Ландсберга. Москва, Наука, 1995 (3 тома) - 500 руб. 6. Общая и неорганическая химия. М.Х. Карапетьянц, С.И. Дракин. Москва, Химия, 1993 - 300 руб. 7. Неорганическая химия. В.И. Спицын, Л.И. Мартыненко. Москва, МГУ, 1991 (2 тома) - 800 руб. 8. Advanced Inorganic Chemistry. Cotton & Wilkinson. USA, Interscience, 1962 (английский язык) - 500 руб. 9. Treatise on Inorganic CHemistry. H. Remy. Elsevier Publishing, 1956 (английский язык, 2 тома) - 500 руб. 10. Количественный анализ. Дж. Фритц, Г. Шенк. Перевод с английского. Москва, Мир, 1978 - 500 руб. 11. Химия в действии. М. Фримантл. Перевод с английского. Москва, Мир, 1991 (2 тома) - 1000 руб. 12. Основы общей химии. Б.В. Некрасов. Москва, Химия, 1974 (2 тома) - 400 руб. 13. Экспериментальные методы в неорганической химии. Г. Лукс. Москва, Мир, 1965 - 300 руб. 14. Неорганическая химия в вопросах. Р.А. Лидин и др. Москва, Химия, 1991 - 300 руб. 15. ИК Спектры и спектры КР неорганических и координационных соединений. К. Накамото (пер. с английского). Москва, Мир, 1991 - 500 руб. 16. Физическая химия. Д.Г. Кнорре и др. Москва, Высшая школа, 1990 - 300 руб. 17. Physical Chemistry. Atkins P.W. Oxford University Press, 1998 (английский язык, в комплекте с CD) - 2000 руб. 18. Начала современной химии. Рэмсден Э.Н., Химия, 1989 - 500 руб. 19. Молекулы. Эткинс П., Москва, МИР, 1991 - 300 руб. 20. Collins Cobuild English Language Dictionary. Collins, London, 1995, 1703 c. – 2000 руб. 21. Англо-русский словарь по химии и химической технологии. Под ред. Кафарова В.В. Москва, Русский язык, 1986 – 600 руб. 22. Русско-английский научно-технический словарь переводчика. Циммерман М., Веденеева К. Москва, Наука, 1991 – 400 руб. 22. Химия в помощь абитуриенту. Кузьменко Н., Еремин В., Попков В. Москва, Дрофа, 1995 – 300 руб. 24. Средства для очистки и ухода в быту. Хауталь Г.Г., Вагнер Г. Фирма Клавель, 2007 – 300 руб. 25. Справочник по аналитической химии. Лурье Ю.Ю. Москва, Химия, 1967 – 200 руб. 26. Практикум по органической химии. Гитис С.С., Глаз А.И., Иванов А.В. Москва, Высшая школа, 1991 – 200 руб. 27. Косметическая химия. Вилламо Х. Москва, Мир, 1990 – 200 руб. 28. Высокотемпературные сверхпроводники. Слейт А.У., Мессмер Р.П. и др. Москва, Мир, 1988 – 300 руб. 29. Аналитическая химия. Пилипенко А.Т., Пятницкий И.В. Москва, Химия, 1990 – 300 руб. 30. Практикум по неорганической химии. Под ред. Зломанова В.П. Москва, МГУ, 1994 – 300 руб. 31. Кинетика химических реакций. Семиохин И.А., Страхов Б.В., Осипов А.И. Москва, МГУ, 1995 – 200 руб. 32. Аналитические реагенты. Саввин С.Б., Чернова Р.К., Штыков С.Н. Москва, Наука, 1991 – 200 руб. 33. Избранные статьи и лекции. Замараев К.И. Сибирское отделение РАН, 1999 – 300 руб. 34. Основы химической технологии. Мухленов И.П., Горштейн А.Е. и др. Москва, Высшая школа, 1991 – 200 руб. 35. Experiments in Physical Chemistry. Wilson J.M., Newcombe R.J., Denaro A.R. Pergamon Press, 1962 (английский язык) – 300 руб. 36. Quantitative organic microanalysis. Steyermark A. Academic Press, 1961 (английский язык) – 200 руб. 37. Химия в нашем доме. Юдин А.М. Москва, Химия, 1990 – 300 руб. 38. Practical organic chemistry. Nekrasov V.V. Mir Publishers Moscow, 1978 (английский язык) – 200 руб. 39. General Chemistry. Whittaker R.M. Chemical Publishing Co., New York, 1959 (английский язык) – 200 руб. 40. The chemistry of organometallic compounds. Rochow E.G., Hurd D.T., Lewis R.N. John Wiley & Sons, New York, 1957 (английский язык) – 200 руб. 41. Иллюстрированный химический словарь. Годмен А. Москва, Мир, 1988 – 200 руб. 42. Inorganic Chemistry an advanced textbook. Moeller R., John Wiley & Sons, New York, 1953 (английский язык) – 300 руб. 43. Кинетические методы в аналитической химии. Перес-Бендито Д., Сильва М. Москва, Мир, 1991 – 200 руб. 44. Химическая связь и превращения оксидов. Резницкий Л.А. Москва, МГУ, 1991 – 200 руб. 45. Методы разделения и концентрирования в аналитической химии. Москвин Л.Н., Царицына Л.Г. Ленинград, Химия, 1991 – 200 руб. 46. Тонкий органический синтез. Евстигнеева Р.П. Москва, Химия, 1991 – 200 руб. 47. Методы геохимического моделирования и прогнозирования в гидрогеологии. Под ред. Крайнова С.Р. Москва, Недра, 1988 – 200 руб. 48. Карбоновые кислоты и карбоксилатные комплексы в химическом анализе. Чарыков А.К., Осипов Н.Н. Ленинград, Химия, 1991 – 200 руб. 49. Неорганическая химия в вопросах и ответах. Лилин Р.А., Аликберова Л.Ю., Логинова Г.П. Москва, Химия, 1991 – 200 руб. 50. Quantitative analysis. Pierce W.C., Sawyer D.T., Haenisch E.L. John Wiley & Sons, New York, 1958 (английский язык) – 300 руб. 51. Основы общей химии. Некрасов Б.В. Москва, Химия, 1974 (в двух томах) – 400 руб. 52. Экспериментальные методы в неорганической химии. Лукс Г. Москва, Мир, 1965 – 200 руб. 53. Физическая химия. Кнорре Д.Г., Крылова Л.Ф., Музыкантов В.С. Москва, Высшая школа, 1990 – 300 руб. 54. Модель отталкивания электронных пар валентной оболочки и строение молекул. Гиллеспи Р., Харгиттаи И. Москва, Мир, 1992 – 300 руб. 55. Аналитическая химия. Барсукова З.А. Москва, Высшая школа, 1990 – 300 руб. 56. Inorganic Chemistry for Higher Education. Brockington J., Stamper P.J. Longman, London&New York, 1983 (английский язык) – 300 руб. 57. Коллоидная химия поверхностно-активных веществ и полимеров. Ким В.Е., Гродский А.С., Кривощепов А.Ф. и др. Топ-книга, 2003 – 300 руб. 58. Прогресс химии углеводов. Под ред. Торгова И.В. Москва, Наука, 1985 – 300 руб.
-
Задача. Рассчитайте ХПК сточной воды. Исходные данные. Сульфанол – 180 мг/дм3; Сульфат натрия – 15 мг/дм3; Нитратный ион – 60 мг/дм3; Фенол – 13 мг/дм3; Хлорид натрия – 390 мг/дм3.
-
В гальваническом цехе установили улавители кислых паров с ванн хромирования. Пары улавливаются фильтром, который потом, в свою очередь, омывается раствором кальцинированой соды, ph раствора колеблется от 9 до 9,5. Вопрос:как в этом растворе обнаружить хром в любом виде? Нужны качественный, количественный методы определения, хотя бы что-то, что помогло бы это анализировать. Анализ нужен для того, чтобы понимать в какой момент нужно менять раствор, так как в очистные мы можем слить раствор, содержащий не более 50мг/л хрома.
- 11 ответов
-
- химия
- гальваника
- (и ещё 4 )
-
Расположить в ряд по легкости диссоциации на свободные радикалы
DZH77 опубликовал тема в Решение заданий
Расположить в ряд по легкости диссоциации на свободные радикалы : а) 2,2,3,3-тетраметилбутан, гексафенилэтан, 1,1,2,2-тетрафенилэтан, гекс-п-дифенилэтан; б) гексафенилэтан, гекс-п-нитрофенилэтан, 2,3-диметил-2,3-дифенилбутан. -
В 240 мг фруктобората кальция содержится 6 мг бора, мне нужно узнать, сколько там мг кальция. Формулу соединения не смог найти в мнтернете, сам не могу составить, так как после школы химией не занимался