Поиск
Показаны результаты для тегов 'фармхимия'.
Найдено 12 результатов
-
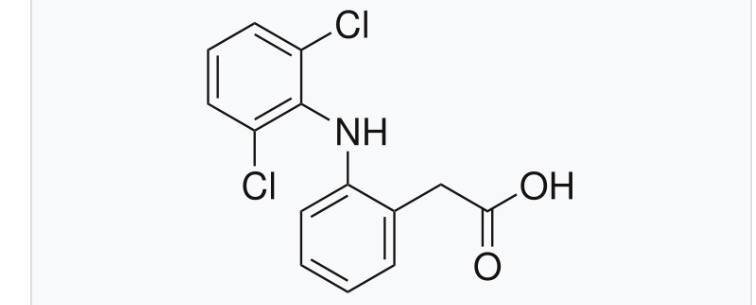
Необходимо добавить к этой молекуле (действующее вещество диклофенака) минимум 3 новых элемента, ранее не входивших в состав исходной молекулы. Предположить как минимум 3 последним стадии синтеза необычного производного вещества с использованием реагентов, подразумевающих значительные структурные изменения, сделать обоснованное предположение о том, как такая модифицированная молекула влияет на путь экскреции препарата
- 5 ответов
-
- органическаяхимия
- школьные
-
(и ещё 1 )
C тегом:
-
а) Дайте обоснование применению реакции с минеральными кислотами в оценке качества натрия гидрокарбоната, натрия цитрата и ортофена. Напишите схемы реакций; б) Рассмотрите использование минеральных кислот в качестве титрованных растворов при количественном определении натрия цитрата и ортофена методом кислотно-основного титрования в водных и неводных средах. Напишите уравнения реакций. Укажите условия титрования.
-
- фармхимия
- фарманализ
- (и ещё 3 )
-
Приведите уравнения реакций количественного определения натрия барбитала методом ацидиметрии. Рассчитайте молярную массу эквивалента барбитала натрия, титр по определяемому веществу, содержание натрия барбитала в анализируемом образце, если на титрование навески массой 0,5042 г затрачено 25,0 мл 0,1М хлороводородной кислоты (К=0,99). При расчётах учтите содержание свободной щёлочи в анализируемом образце натрия Барбитала, которое равно 0,2%.
-
Как правильно довести до метки окрашенные растворы? И Как довести прозрачные растворы?
- 1 ответ
-
- химия
- аналитическая химия
-
(и ещё 3 )
C тегом:
-
Кислоты хлористоводородной 1% – 200 мл; Кислоты аскорбиновой 1,0. Рассчитайте средний титр и навеску лекарственной формы (мл), чтобы на суммарное титрование кислот хлористоводородной и аскорбиновой пошло 2,0 мл 0,1 моль/л раствора натрия гидроксида (К=1,0). Спасибо большое тому, кто поможет
- 1 ответ
-
- фармхимия
- средний титр
-
(и ещё 3 )
C тегом:
-
Микстура: Раствора Натрия бромида 6,0-200,0 мл; Новокаина 1,0; Барбитал – натрия 1,5. а. Рассчитайте навеску лекарственной формы (мл), чтобы на титрование в ней новокаина пошло 2,0 мл 0,1 моль/л раствора натрия гидроксида (К=1,01). б. Рассчитайте объем 0,1 моль/л раствора кислоты хлористоводородной (К=1,01), который пойдет на титрование барбитал-натрия в 10,0 мл микстуры. Спасибо большое!!!
-
- фармхимия
- титрование
-
(и ещё 1 )
C тегом:
-
Приготовлено 200мл 40% раствора глюкозы для инъекций. Анализ показал, что раствор содержит 38% препарата. Сколько надо добавить глюкозы с влажностью 9,8% до получения 40% раствора с плотностью 1,1498 г/мл. Кажется по методу креста нужно делать, но не пойму, что куда подставить. Напишите, пожалуйста. И еще не пойму, что делать с показателем плотности Помогите пожалуйста. Спасибо большое заранее!
- 2 ответа
-
- фармхимия
- технология
- (и ещё 3 )
-
Напишите, пожалуйста, методы идентификации никодина, где они возможны и их уравнения Спасибо большое!
- 2 ответа
-
- 1
-

-
- никодин
- методы идентификации
- (и ещё 5 )
-
Рассчитайте массу таблетки анальгина (М.м. 351,36), если на ее титрование истрачено 12,00 мл 0,1М раствора йода (КП=1,0000), содержание действующего вещества в субстанции- 99,2%, потеря в массе при высушивании - 5, 24%. Помогите, пожалуйста, решить задачу. Очень нужно!
-
Доброго времени суток! Куплю или приму в дар следующие книги (название, автор, год): 1) A Guide to Organophosphorus Chemistry, Louis D. Quin (2000) 2) Organic Chemistry, Jonathan Clayden, Nick Greeves, Stuart Warren, Peter Wothers (2001) 3) Органический синтез. Наука и искусство,: Вильям Смит, Алексей Бочков, Кейпл Кейпл (2001) 4) Основы медицинской химии, В.Г. Граник (2006) 5) Химия и токсикология органических соединений фосфора и фтора, Б. Сондерс (1961) 6) Фармацевтическая химия. Книга 2. 4 курс, В. Чупак-Белоусов (2012) Знаю, что большая часть этого списка есть в интернете в свободном доступе, но я ищу именно в бумажном варианте. Буду признателен, если поделитесь информацией, где можно заказать или купить данные книги.
-
- ФОС
- Токсикология
-
(и ещё 2 )
C тегом:
-

задача на фактор эквивалентности и массовой доли вещества
фамацевт Т опубликовал тема в Решение заданий
Количественное определение тимола проведено по следующей методике: около 0,5 г препарата (точная масса) растворяют в 5 мл раствора натрия гидроксида в мерной колбе вместимостью 100 мл и доводят объем раствора водой до метки. Отмеренные 10 мл полученного раствора переносят в колбу, прибавляют 0,5 г бромида калия, 40 мл разведенной хлороводородной кислоты, 3 капли раствора метилового оранжевого и при сильном взбалтывании титруют 0,1 моль/л раствором бромата калия до исчезновения розового окрашивания. 1 мл 0,1 моль/л раствора бромата калия соответствует 0,003755 г тимола, которого в препарате должно быть не менее 99,0%. Дайте обоснование метода, приведите уравнения реакций, фактор эквивалентности, молярную массу эквивалента, титр и расчетную формулу определения массовой доли вещества (в %) в препарате. KBrO3 + 5KBr + 3H2SO4 → 3Br2 + 3K2SO4 +3H2O +2Br ==== f=1/2´1/2= ¼ Получаеться титр равенT(KBrO3/C10H14O)=0.00375г отсюда можно вычеслить M(f)=Т*1000/С титранта ,тогда M(f)= 0,00375 *1000/0,1=37,5 или я не в правильном направлении иду? -
Этаминал натрия растворяют в нейтрализованном диметилформамиде или смеси диметилформамида и бензола и титруют 0.1м раствором NaOH ?Используют индикатор тимоловый синий.Диметилформамид,являясь основным растворителем присоединяет протон т.е NA+ (Получается HCON+Na(CH3)2??) усиливая при этом кислотные свойства этаминала натрия При последующем титровании гидроксидом натрия,последний образует натриевую соль.Не пойму зачем из натриевой соли опять натриевая соль ?