-
Постов
586 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные BauVictoria
-
-
12 часа назад, M_GM сказал:
Когда добавлено эквивалентное количество соли, то в результате ее реакции с HCl в растворе будет муравьиная кислота с концентрацией 0,2М. Видимо рассчитали рH для 0,2М раствора этой кислоты.
рН в растворе слабой кислоты можно рассчитать по упрощенной формуле.
Но у меня этот расчет дает другое значение:
рН= 0,5рК -0,5lg(С) =0,5*3,75-0,5*lg(0,2) = 1,526
Хотя тут даже по вашему расчету не получается, потому что там выходит рН=2,2, т.к
рН=0,5*3,75-0,5lg0,2=1,875-0,5*(-0,698)=2,224
А там 1,8... В чем же тогда дело?
-
-
10 часов назад, M_GM сказал:
Когда добавлено эквивалентное количество соли, то в результате ее реакции с HCl в растворе будет муравьиная кислота с концентрацией 0,2М. Видимо рассчитали рH для 0,2М раствора этой кислоты.
рН в растворе слабой кислоты можно рассчитать по упрощенной формуле.
Но у меня этот расчет дает другое значение:
рН= 0,5рК -0,5lg(С) =0,5*3,75-0,5*lg(0,2) = 1,526
Хорошо, благодарю!) рН в растворе слабой кислоты при а<5% (если кислота диссоциирована мало) считается по формуле рН=1/2(рКа+рСна), а если а>5%, то [Н+]=(-Ка+sqrt(Ka^2+4KaCна))/2
-
4 часа назад, M_GM сказал:
pH буферного раствора рассчитывается по формуле pH=pK + lg(C(соли)/С(к-ты))
pK муравьиной кислоты равна 3,75 (табл)
Отсюда lg(C(соли)/С(к-ты)) = рН-рК = 4,3-3,75=0,55
C(соли)/С(к-ты) = 100,55 = 3,55
Кислоты HCl в растворе n=C*V =0,2*0,1=0,02 моль
Эквивалентное ей количество соли составит тоже 0,02 моль
После добавления эквивалентного HCl количества соли концентрация НСООН в растворе станет равной 0,2М
Далее добавляем соли до концентрации C(соли)=0,2*3,55=0,71M
Объем раствора здесь считается неизменным, 100 мл=0,1 л, поэтому добавить нужно
n=C*V =0,71*0,1=0,071 моль
Общее количество добавленной соли 0,02+0,071 = 0,091 моль
Ее масса будет равна m=M*n = 68*0,091=6,188 г
Всё

И кстати: не химией единой >>
Вот, посмотрите, пожалуйста:)
-
3 часа назад, aversun сказал:
Вот как раз Позин о таких полимерах и упоминает, я давал ссылку
Вообще дело было так: это соединение было увидено мною в книге по аналитике Золотова(практикум) и там было написано так: летучие соединения бора(H3BO3,BF3, эфиры бора) окрашивают пламя горелки в зеленый цвет. Большинство боратов разлагаются конц H2SO4 с выделением летучей H3BO3. Реакцию проводят в ушке платиновой или нихромовой проволоки. Предел обнаружения бора 0,2-0,3 мкг. Мешают соли Ba, Cu, Tl, а также фосфаты и молибдаты. В присутствии PO4 3- образуется нелетучее соединение (BO)PO3, в чем собственно говоря и был вопрос:)
2 часа назад, yatcheh сказал:Ну, это уже экзотика. На всё платины не напасёшься...
2 часа назад, Paul_K сказал:В комплексах и с тройной связью существует

https://pubs.rsc.org/en/content/articlelanding/2010/CC/c0cc01802c#!divAbstract
Я смотрю по моему вопросу здесь теперь очень оживленная дискуссия
-
3 часа назад, M_GM сказал:
pH буферного раствора рассчитывается по формуле pH=pK + lg(C(соли)/С(к-ты))
pK муравьиной кислоты равна 3,75 (табл)
Отсюда lg(C(соли)/С(к-ты)) = рН-рК = 4,3-3,75=0,55
C(соли)/С(к-ты) = 100,55 = 3,55
Кислоты HCl в растворе n=C*V =0,2*0,1=0,02 моль
Эквивалентное ей количество соли составит тоже 0,02 моль
После добавления эквивалентного HCl количества соли концентрация НСООН в растворе станет равной 0,2М
Далее добавляем соли до концентрации C(соли)=0,2*3,55=0,71M
Объем раствора здесь считается неизменным, 100 мл=0,1 л, поэтому добавить нужно
n=C*V =0,71*0,1=0,071 моль
Общее количество добавленной соли 0,02+0,071 = 0,091 моль
Ее масса будет равна m=M*n = 68*0,091=6,188 г
Всё

И кстати: не химией единой >>
Спасибо за ответ!) но как было посчитано число 1,8? То есть если добавляем формиата натрия эквивалентное количество хлороводородной кислоте, то концентрация НСООН в растворе 0,2 моль/л и рН раствора составляет 1,8, а по условию нужно 4,3 и поэтому, чтобы снизить концентрацию ионов водорода добавляют избыток ацетата натрия(это взято из книги Васильева(аналитическая химия), хотя Ваше решение мне понятнее). Можете, пожалуйста, объяснить мне, почему они так пишут? Откуда посчитали 1,8? Вы считали по другому и ответ у вас верный!)
Р. S красивые поделки по ссылке:))
-
-
Какую массу твердого HCOONa нужно добавить к 100 мл 0,2M HCl, чтобы получить буферный раствор с рН 4,3? Есть объяснение этой задачи: при добавлении HCOONa к раствору НCl образуется HCOOH. Если HCOONa добавлено эквивалентное количество хлороводородной кислоте, то С(HCOOH)=C(HCl)=0,2 моль/л и рН раствора составляет 1,8. Но по условию надо получить с рН 4,3 и т.д..... Так вот, как была посчитана цифра 1,8, если добавляли эквивалентное количество? Помогите, пожалуйста!
-
3 часа назад, aversun сказал:
метафосфат борила
Спасибо! :))
3 часа назад, Paul_K сказал:Это BPO3, а я спрашивала про (BO)PO3

-
Как называется соединение (BO)PO3?
-
2 часа назад, Аль де Баран сказал:
В аквакомплексах меди к.ч. тоже равно 4. См. хотя бы у Глинки. Вообще, комплексы меди с к.ч. 6 ещё надо потрудиться поискать. Вроде бы, с этилендиамином есть комплекс [CuEn3]2+, но не шибко устойчивый

Ага, хорошо, понятно:)
-
9 минут назад, Аль де Баран сказал:
Не-а, в аммиакатах к.ч. меди равно 4. Вода внутрь может входить только за счёт вытеснения NH3, например, [Cu(NH3)2(H2O)2]2+
А как же аквакомплекс [Cu(OH2)6]2+ в нем замена молекул воды на NH3?
-
-
Нужно показать, что Al(H2O)5(OH)2+ является амфолитом. В 1) я уверена, а во втором нет
1) Al(H2O)5(OH)2+(кислота1) +Н2О(основание2)=Н3О+(кислота2)+Al(H2O)4(OH)2+(основание1)
2) в этом пункте я написала 2 варианта, подскажите, пожалуйста, какой правильный:
H3O+(кислота1)+Al(H2O)5(OH)2+(основание2)=Al(H2O)63+(кислота2)+Н2О(основание1) или может быть так: H2O(кислота1)+Al(H2O)5(OH)2+(основание2)=Al(H2O)63+(кислота2)+ОН-(основание1)
Помогите, пожалуйста!)
-
-
Почему в водном растворе слабой кислоты H2S [HS-]<<[H2S] и [S2-]<<[HS-]? В квадратных скобках указаны равновесные концентрации
-
-
1 час назад, yatcheh сказал:
Не очень понятный вопрос.
Поскольку ТСХ зиждется на процессах сорбции-десорбции, то чем полярнее фаза, тем быстрее движется пятно. Помимо, собственно - скорости, есть ещё параметр дифференцируемости (селективности), но это предсказать невозможно. В одной фазе пятна делятся, в другой идут стадом. Тут уже надо поэкспериментировать. Обычно полярность фазы регулируют, используя смесь полярного и неполярного растворителя, считается, что чем больше разница в полярности - тем выше селективность, но это далеко не всегда так

Благодарю!

-
Как влияет подвижная фаза на скорость продвижения компонента в ТСХ? (Например, аскорбиновая кислота в разных подвижных фазах)
-
В 14.09.2019 в 23:06, pinkylee сказал:
черный считается, но не в вашем случая - нет полного расхождения пятна. в моем случае в остатке было серое пятно на старте. и попробуйте ставить более тонкое пятно
Хорошо, благодарю!
-
-
8 минут назад, yatcheh сказал:
И чёрный надо считать. Это же тоже краситель.
А ТСХ - неудачная. Надо, ИМХО - концентрацию уменьшить на порядок. Из фото величина Rf не видна. Так, что, может и систему стоит поменять. Или применить двумерную ТСХ на квадратной пластинке. Для красителей это особенно эффектно (и эффективно) получается.
Неудачный выбор, такая система будет тащить всё подряд.
Спасибо за ответ! Мне не нужно было измерять Rf (это ознакомительная работа:)) скажите,а вот на пластинке виден серый цвет, его получается не считать? ( серый же смесь цветов)
-
Здраствуйте, фломастер был черный, сама пластинка(алюминиевая фольга, силикагель, силиказоль),подвижная фаза- этанол и ацетон(3:1). А нужно ли считать черный цвет?
-
Сколько красителей и какого цвета входит в состав пасты фломастера? Помогите, пожалуйста, разобраться в полученном результате:)


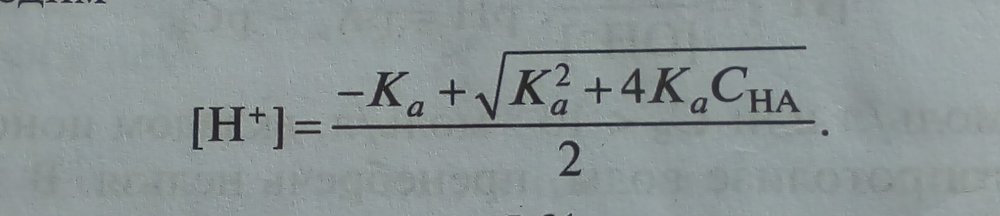


Буферные растворы
в Решение заданий
Опубликовано
Насколько я понимаю, но по этому смотрят,что ацетат натрия будет в избытке, а это важно для задачи, там же в условии не написано, что в избытке