-
Постов
586 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные BauVictoria
-
-
1 час назад, Paul_K сказал:1 час назад, bacan сказал:
Спасибо) не знаю, как учебник, а вот в задачнике этого автора ошибок очень много:)
-
2 часа назад, Nemo_78 сказал:
Второй - тетрахлоростаннат(II)-анион, а первый существует ли, вообще?
Да, существует, у меня в учебнике написан
-
12 часов назад, M_GM сказал:
1/6 - это фактор эквивалентности для дихромата калия.
Для окислителя/восстановителя fэ = 1/(число принятых/отданных электронов)
Запись 1/6 K2Cr2O7 - обозначает эквивалент дихромата - 1/6 моля
А всю строчку надо понимать так: число эквивалентов дихромата равно числу эквивалентов йода и равно числу эквивалентов тиосульфата натрия (закон эквивалентов для этих реакций)
По формуле: m(K2Cr2O7)/M(1/6 K2Cr2O7 ) - масса навески/(молярную массу эквивалента) - находим число моль эквивалентов в навеске, которую растворили в мерной колбе
делим на Vк (100 мл) - находим число моль эквивалентов в 1 мл полученного раствора;
- умножаем на Vп (25 мл) находим число моль эквивалентов в пробе взятой для реакции с KI
Спасибо, очень понятное обьяснение! Единственное в решении задачи при нахождении титра подставляют Vk=200, почему и откуда берется 200? Ошибка? Я подставляла 100
-
-
-
38 минут назад, bacan сказал:
Нашла, спасибо!))
-
30 минут назад, bacan сказал:
Просто я исходил из того, что должны получиться устойчивые вещества и среда должна быть нейтральна. 1) вариант неустойчивоее соединение НClO2; 2) - щелочная среда, 3) и 5) - выделение газов; 6) - образуется щелочь. Это мои рассуждения и пото, я нашел на одном сайте как правильно составлять уравнения полуреакций - это сайт http://buzani.ru/.
как-то так
Хорошо, спасибо!!!) А где именно на сайте вы нашли, я смотрю тут много всего?

-
23 минуты назад, chemister2010 сказал:
Число значащих цифр результата обычно равно числу значащих цифр погрешности. Это так в официальных методиках выполнения измерений пишут.
Это получается как должно быть записано?
-
Подскажите, пожалуйста, что не входит в константу равновесия. Знаю, что твердые вещества точно не входят, но вот у меня есть следующие ОВР реакции:
1) 2S2O3+I2=S4O62- +2I- (входит ли I2?)
2) Cr2O72- +6Cl+14H+=2Cr3+ +3Cl2+7H2O (входит ли газ хлор?)
3) 3N2H4+2BrO3-=3N2+2Br- +6H2O ( входит ли N2H4 и N2?)
Есть какое-то общее правило для решения этого вопроса?
Помогите разобраться)
-
9 часов назад, yatcheh сказал:
Правильно понимаете. Обычно для этой цели используют стандартизованный раствор соли Мора. Он достаточно устойчив к окислению кислородом воздуха.
Спасибо за ответ!
-
2 минуты назад, yatcheh сказал:
Это получается обратное титрование. В чём проблема-то? Как назвать эту херню?
Да, обратное, ага, значит я правильно рассуждала. И скажите, пожалуйста, вот когда идут слова: по окончании реакции восстановления реакции перманганата в щелочной среде раствор подкисляют и титруют избыток MnO4- раствором железа(2) я правильно понимаю, что железо 2 в бюретку заливаем?
-
1 час назад, bacan сказал:
Подойдет 4)
Реакция FeSO4 с KClO3 протекае при подкислении (в кислой среде Н+)
Уравнения электронного баланса:
Восстановитель 6|Fe2+ - 1(электрон) = Fe3+ процесс окисления
Окислитель 1|ClO3- + 6Н+ + 6(электронов) = Cl- + 3Н2О процесс восстановления
Ионно-молекулярное уравнение:
6Fe2+ + |ClO3- + 6Н+ = 6Fe3+ + Cl- + 3Н2О
Составляем уравнение реакции, получим:
6FeSO4 + KClO3 + 3H2SO4 → KCl + 3Fe2(SO4)3 + 3H2O
Метод полуреакций:
http://buzani.ru/raznoe/metodika/677-okislitelno-vosstanovitelnye-reaktsii
Спасибо вам за ответ! Я там выше допустила описку, я тоже считаю, что подходит 4 реакция и написала уравнение как у вас, но я к сожалению, не пойму как вы выбрали между вариантов, которые я сфотографировала) я правильно понимаю, что я должна выбирать реакцию, где получается устойчивый продукт, значит не подходит 3) и 5) . А среди оставшихся как выбрать?
-
Подскажите, пожалуйста при взаимодействии Fe3+ +ClO3- =Fe3+ +..... Вероятнее всего до чего пойдет реакция?
В справочнике Лурье полуреакций много. Тема: скачок титрования и его расчет, т.е титруют FeSO4 раствором KClO3. Значит продукты должны быть устойчивыми и 3) и 5) не подходят. Далее судя по потенциалам(потенциал пары в котором участвует окислитель KClO3 должен быть наибольшим, а потенциал пары в которой участвует восстановитель наименьшим, т.к любая реакция в стандартных условиях протекает между более сильным окислителем и более сильным восстановителем, но у меня в задании есть оН и он не равен 0, условия нестандартные) выходит 5) полуреакция? Помогите, пожалуйста, объясните, почему не могут подойти другие реакции
-
28 минут назад, aversun сказал:
В щелочной среде MnO42- получается без всякого восстановителя, только за счет разложения перманганата.
У меня написано это в учебнике. Я просто не пойму это какой способ титрования? Обратный?
-
1 час назад, aversun сказал:
23.8±0.6 -- значит, на каком-то там доверительном уровне (история об этом умалчивает), максимальное значение может быть 24.4, а минимальное 23.2, т.е. постоянной остается только цифра 2
Спасибо!!
-
Определяют используя восстановление MnO4- в щелочной среде MnO4- +e=MnO4 2-. Органические соединения окисляются до карбоната. По окончании реакции восстановления перманганата в щелочной среде раствор подкисляют и титруют избыток MnO4- раствором железа(2). Это получается обратное титрование? И в бюретку лить соль железа(2)?
-
Как будут называться ионы FeCl(2+) и SnCl4 (2-) ?
-
31.10.2019 в 21:27, M_GM сказал:
Да, судя по этому тексту я был не прав - сравнивать надо не с половиной максимального значения разряда, а с половиной единицы разряда
Цифра 23, стоит в разряде единиц , половина от 1 равна 0,5,
0,6 > 0,5 значит цифра 3 и все последующие неверны
Цифра 2 стоит в разряде десятков, половина от 10 равна 5
0,6 < 5 значит цифра 2 и все предыдущие (если бы они были) - верные
Да вот и я прочитав эту статью, немного удивилась тому, что написано в учебнике. Вы представляете, они вообще считают, что верными будут не только 2,3,но и цифра 8 да еще и с погрешностью 0,6...как вы думаете это все-таки ошибка?
-
32 минуты назад, M_GM сказал:
А я бы сказал так: цифра 8 стоит в разряде десятых максимальное значение этого разряда 0,9
0,6>0,9/2 - значит цифра 8 неверная
Цифра 23, стоит в разряде единиц , максимальное значение этого разряда 9
0,6< 9/2 - значит цифра 3 верная
Поэтому результат запишется так: числе 23,836 ~= 23,8+/-0,6
А, я просто нашла в интернете, вот ссылка на подобный пример( определение 2.2, пример 2.4 в ссылке ниже), но то, что написано в учебнике мягко говоря поразило.
-
Представление результатов эксперимента с учётом погрешности. Цифра в числе считается верной, если погрешность не превосходит половины разряда, в котором расположена данная цифра ( гласит учебник) и дается пример, который мне вот уж никак непонятен. Например, в числе 23,836 , полученном из эксперимента с погрешностью 0,6 , верными считаются все цифры, используемые для записи целой части числа, а также цифра 8 из дробной части. Цифра 3 и 6 в этом случае неверные. Такая большая погрешность, и так много верных цифр. По моему расчету верная цифра только одна и это 2 (0,6<=1/2 * 10^1).
В чем тогда дело? Помогите, пожалуйста:)
-
30.10.2019 в 10:53, aversun сказал:
Спасибо за последнюю реакцию, а ту я написала:
Mn(OH)2+H2O2=MnO(OH)2+H2O
-
-
2 часа назад, St2Ra3nn8ik сказал:
Если хорошо помню и не туплю, то сухой способ - это сорбент просто насыпается в колонку (может и с уплотнением его вибрацией (вот это точно не вспомню)). А мокрый - в колонку наливается суспензия сорбента с последующим сливом жидкости после отстаивания. Но могу и ошибаться.
 2 часа назад, Nemo_78 сказал:
2 часа назад, Nemo_78 сказал:Да так всё, вроде бы б, хоть и давно это было. Насчёт вибрации не помню, но то, что подолгу пробрасывали колонки по длинным трубкам с резиновой подложкой внизу, утрамбовывая сорбент, помню отчётливо.
*Прим. Разумеется, имеется в виду "сухой" способ.
Спасибо за ответы! На счёт мокрого способа мы делали суспензию оксида алюминия со спиртом)
-
Колонка может быть заполнена сорбентом Al2O3 мокрым и сухим способом. Объясните, пожалуйста, что под этим подразумевается?





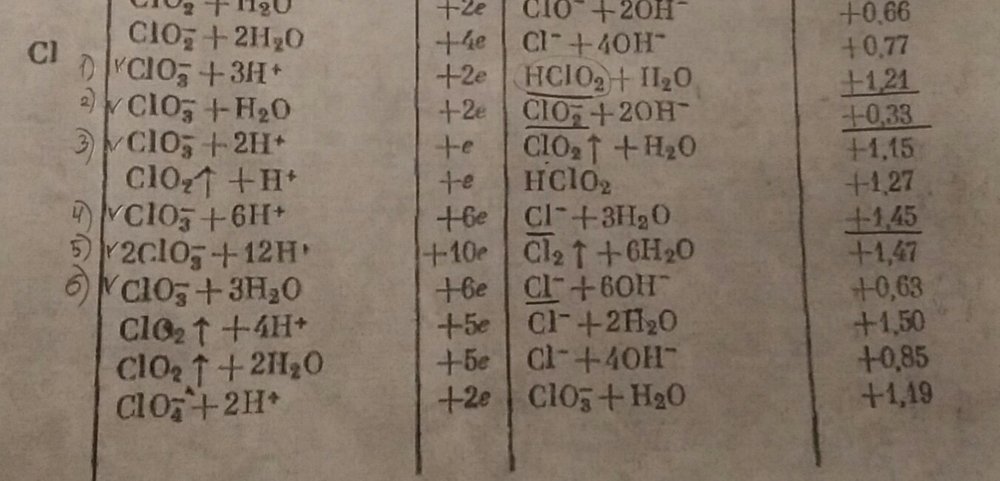

Названия ионов
в Решение заданий
Опубликовано
Спасибо:)