-
Постов
128 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные Папа_школьника
-
-
1 час назад, Paul_S сказал:
А можно поподробнее? Если очень много соли в растворе, то оксидная пленка исчезнет? А какая это реакция?
Насколько я понимаю, пока оксид алюминия не начал реагировать, будет происходить гидролиз купороса:
CuSO4 + 2H2O = Cu2+ SO42- 2H2O = Cu(OH)2 (слаб осн - по табличке должно выпадать в осадок) + 2H+ + SO42- (сильная кислота)
А то, что между Cu и H2O реакция вообще то не идёт, это не мешает, потому что здесь связываются ионы?
А дальше что? реакция нейтрализации, так?
6 H+ + 3 SO42- + Al2O3 = Al2(SO4)3 + 3 H2O, или в растворе 2 Al3+ 3SO42- + H2O. То есть по сути, ионы водорода, оставшиеся без ОН- после выпадения в осадок гидроксида меди, теперь отрывают кислород от оксида и тем высвобождают катионы Al3+, правильно?
Ок, если так, то вот мы добрались до алюминия под оксидной пленкой, и у нас есть как ионы Al3+ из оксида, так и свободный алюминий. Судя по книжке, ионы Al3+ должны связываться в слабое нерастворимое основание Al(OH)3, выпадающее в осадок, а свободный алюминий по книжке должен в реакции с водой давать также гидроксид и водород:
2Al + 6H2O = 2Al(OH)3 + 3H2 газ
Если всё так, то вопрос такой: а как вообще тут свободная медь может "выделиться"? По логике, ей должен вернуть электроны более активный алюминий, но где они тут встретятся? Если только не вся медь выпадет в осадок в виде Cu(OH)2 в самом начале и какая-то часть Cu2+ дождется появления Al0 из-под оксида?
-
Только что, Krolikoff сказал:
Скрепки обычно делают никелированными, чтобы не ржавели. Доступный образец железного изделия - обычные неоцинкованные гвозди.
Этого добра завались - сегодня повторю с гвоздём)
-
Только что, Леша гальваник сказал:
Имхо, скрепка как минимум никелированная (в руках бы подержать/посмотреть). А у алюминия окисная пленка мешает - снять бы ее в растворе гидроксида натрия (крота) примерно 100 г/л содержание (там сами увидите как снимается - поначалу редкие пузырьки, потом чаще, еще чаще, и вот уже пузырит вся поверхность - это буквально минуты времени), потом промыть и в раствор медного купороса.
И кстати, на пробирке с цинком пробка вылетела. Это наверное избыток цинка уже с водой реагирует с выделением водорода, да?
Zn + 2 H2O = Zn(OH)2 + H2
-
Только что, Леша гальваник сказал:
Имхо, скрепка как минимум никелированная (в руках бы подержать/посмотреть). А у алюминия окисная пленка мешает - снять бы ее в растворе гидроксида натрия (крота) примерно 100 г/л содержание (там сами увидите как снимается - поначалу редкие пузырьки, потом чаще, еще чаще, и вот уже пузырит вся поверхность - это буквально минуты времени), потом промыть и в раствор медного купороса.
Спасибо, а какую концентрацию щелочи лучше сделать? У меня нет крота, у меня просто сухой NaOH. Наверно, немного надо, нужно ведь просто одну гранулу окунуть. И как не передержать? Насколько я понимаю, там сначала с оксидом комплексная соль получится, а потом и с самим алюминием реакция пойдет?
2NaOH + Al2O3 + 3H2O = 2Na[Al(OH)4]
а потом
2Al + 6 H2O = 2 Al(OH)3 + 3H2
-
Делали школьный опыт - в раствор медного купороса положили (справа налево) гранулу алюминия, гранулу цинка и предположительно стальную скрепку. Через 2 часа цинка уже не видно за бурым налётом , а алюминий и скрепка никак не изменились (см. фото). Разве алюминий не самый активный из трех металлов и не должен ли он вытеснять медь наиболее активно?
-
01.03.2020 в 09:59, M_GM сказал:
Сути дела это не меняет, в растворе все равно таких молекул нет!
А вот если полученный раствор начать выпаривать, тогда и начинают выпадать кристаллы определенного состава.
В первую очередь выпадает наименее растворимая соль ( MgCl2 или MgBr2 или MgClBr - тут надо лезть в справочники и искать данные)
Если наименее растворима MgClBr будут выпадать кристаллы этой соли, до полного израсходования всех ионов в растворе
Если наименее растворима MgBr2 будут выпадать кристаллы MgBr2, но бромид ионов хватит только на половину ионов магния, когда их станет в растворе мало, начнут выпадать кристаллы MgCl2 и в результате мы будем иметь смесь двух солей
И т.п. На практике картина сложнее и обычно из такого раствора всегда образуются смеси солей, обычно с преобладанием той или другой.
По этой же логике, правильно я понимаю, что хотя (данная в пособии) реакция
KHSO4 + MgOHCl = MgSO4 + KCl + H2O
несомненно идет (образуется Н2О), какие именно соли останутся в остатке после выпаривания будет зависеть от их сравнительной растворимости, а в растворе это всё будет плавать в виде ионов Mg2+ SO42- , K+ и Cl-? -
Только что, aversun сказал:
Вообще-то HI формально более сильная кислота, чем HCl.
Потом, вы сравниваете силу кислоты и активность галогена, а это разные вещи.
Активность галогена тоже не такая простая вещь
KClO3 + I2 = KIO3 + Cl2
Что я имею ввиду. Вот например, в реакции
Cl2 + FeI2 = FeCl2 + I2 (в осадок)
нагревание, как я понимаю, ослабляет связи в ионном кристалле FeI2 и также разбивает молекулу Cl2 на 2 атома хлора, каждый из которых забирает по электрону у иона I- (потому что более высокая Э.О.) и в итоге замещает ион I- в кристалле соли.
А в реакции HI c FeCl2 наоборот
2H+ 2I- Fe2+ 2Cl- = 2HCl Fe2+ 2I-
ион хлора соединяется с H+ в более слабую HCl и таким образом по факту ион I- по факту замещает Cl- в хлориде. Если выпарить раствор. С другой стороны, ион Cl- замещает ион йода I- в кислоте....
-
Пытаюсь взаимно увязать 2 правила, относящихся к химическим свойствам солей:
1 - Сильные кислоты вытесняют слабые из их солей
2 - Более активные галогены (а может, и любые более активные неметаллы?) вытесняют менее активные из солей галогеноводородных кислот
Ну то есть, по правилу 1 хлорид железа II реагирует с йодоводородом так:
2H+ 2I- Fe2+ 2Cl- = 2HCl Fe2+ 2I-
(хотя наверное там не слишком много молекул HCl, а всё больше ионов H+ и Cl-, но всё же как я понимаю равновесие смещено в сторону более слабого электролита, так?)
то есть как бы йод замещает собой хлор в хлориде - ок, пусть не сам, а в результате уменьшения количества H+ в растворе
а по второму правилу получается, что наоборот, хлор должен вытеснять йод из йодида железа II:
Cl2 + FeI2 = FeCl2 + I2 в осадок
и фтор должен вытеснять хлор из хлорида
F2 + FeCl2 = FeF2 (или FeF3?) + Cl2 газ
Где логика? Ведь более активный галоген одновременно является остатком менее активной кислоты?
-
6 часов назад, M_GM сказал:
Углекислый газ в лаборатории обычно получают взаимодействием мрамора (CaCO3) с соляной кислотой

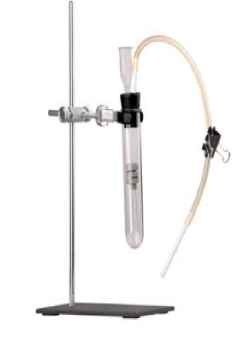
Зарядить на углекислый газ, значит в пробирку на медную сетку (сейчас вместо нее обычно используется резиновая шайба, с зазором входящая в пробирку) поместить мелкие кусочки мрамора (вместо гранул)
На боковой отвод одеть резиновую трубку с зажимом или краном (закрытым)
Плотно вставить пробку с воронкой в горлышко пробирки
Аккуратно наливать в воронку соляную кислоту.
Поскольку нижняя часть прибора замкнута, то в пробирку сможет зайти только немного кислоты, до мрамора она не достанет и реакция не начнется, основная часть кислоты останется в воронке.
Прибор готов к работе
Как только будет открыт кран, из пробирки начнет выходить воздух, а в пробирку будет поступать кислота из воронки. Когда кислота в пробирке достигнет мрамора - начнется реакция и из пробирки пойдет углекислый газ
Если затем кран перекрыть, выделяющийся углекислый газ начнет вытеснять кислоту обратно в воронку, ее контакт с мрамором будет нарушен и реакция автоматически прекратится.
Так ее можно будет запускать и прекращать неоднократно
Всё стало понятно, спасибо!
-
Прибор Кирюшкина - это просто вот такая пробирка с воронкой и трубкой в пробке? А если трубка отходит не из пробки, а сбоку из стекла, это все еще он?
Что означает "прибор Кирюшкина, заряженный на углекислый газ"? Опыт такой - в воронку прибора, "заряженного на углекислый газ", налить раствор соляной кислоты. Газоотводную трубку опустить в раствор гидроксида кальция, ждать получения прозрачной жидкости. Еще в ингредиентах - мрамор. Соляную кислоту в пробирку на мрамор что-ли наливать? Толком не написано.

-
15 часов назад, M_GM сказал:
Но это все не 8-й класс
Увы, я в курсе. А вот эти задания из домашки на прошлый вторник тянут на 8-й класс, даже и "профильный"? Мне особенно нравится, как восьмиклассники должны запросто с комплексными солями управляться. Они только в начале 3-й четверти начали оксиды, только что за полторы недели проскакали кислоты, и сейчас уже перешли к солям. План, видимо, за одну четверть всю неорганику закрыть (!!!). Учительница упорно преподает без учебника. С доски. И я её понимаю - просто не существует учебников, написанных на понятном для 8-го класса языке, которые бы настолько углублялись в тему. Пардон, в тех (реально уже институтских) учебниках, где разбираются особые свойства сульфидов в реакциях с кислотами, или про комплексные соли говорится, уже используется и терминология институтская. И можно ли за один, или даже два 45-минутных урока в классе на доске разобрать все свойства кислот, знания которых нужны для решения такой домашки?
В конце второй четверти я ее просил что-нибудь порекомендовать, раз штатный учебник (да, он есть!) не подходит. Она мне посоветовала пособия Хомченко, Еремина и т.д. На секундочку, это всё "Пособия для поступающих в вузы" или типа того. Или Врубельского - "Полный курс школьной химии!" Полный! С таким же успехом можно энциклопедию порекомендовать.

-
28 минут назад, chemister2010 сказал:
Квадратные скобочки здесь обозначают молярные концентрации (моль/л). Между ними подразумевается умножение. Оно опущено, как иногда делают в математике типа"xy = x * y".
В данном случае формула показывает взамосвязь концентраций ионов кислоты с недиссоциировавшими молекулами, через константу, которая называется константой диссоциации и приводится в справочниках.
Для произведения растворимости HgS формула будет выглядеть похоже: [Hg2+][S2-]/[HgS] = ПР, где ПР - это константа, называемая произведение растворимости.
Спасибо. Еще немного, и я пойму)
5 минут назад, M_GM сказал:В произведение растворимости входит лишь произведение концентраций ионов малорастворимой соли в степенях стехиометрических коэффициентов: ПР(HgS) = [Hg2+][S2-], ПР(Bi2S3) = [Bi3+]2[S2-]3,
Отдельное спасибо, а то бы я на этом споткнулся рано или поздно
-
02.03.2020 в 16:22, Nemo_78 сказал:
Тогда Вам (сначала для себя, что называется) нужно проштудировать какой-нибудь учебник по общей химии, Раздел "Равновесия в растворах электролитов". А уж потом с вопросами выходить, ежели не разберётесь. Так мне кажется...
Спасибо. Я пошел читать Некрасова, на стр.176 дошёл вот до этого места. Первое уравнение я понял - это ситуация, когда столько же молекул распадается на ионы, сколько пар ионов соединяются обратно в молекулы.
А вот что это за вторая формула? Что означают квадратные скобки? Количество? Или масса, раз упоминается некий "закон действия масс"? Между скобками подразумевается знак умножения? Я привык, что количество обозначается N, а умножение - точкой или звездочкой. Там словами нигде (ок, нигде рядом) не написано, что эта формула показывает. Чисто из здравого смысла, означает ли это, что для конкретного электролита в растворе любой концентрации частное от деления произведения количеств ионов на количество нераспавшихся молекул постоянно? Плиз хелп.

-
Правильно я понимаю, что не в воде, а в более сильной кислоте как HNO3 гидроксокарбонат меди распадется так
Cu(OH)NO3 CO32- 2H+ 2NO3- и затем получится
2 Cu(OH)NO3 + H2CO3, кислота разложится на CO2 и H2O. То есть, ионное уравнение будет CO32- 2H+ = CO2 и H2O ? А Cu(OH)NO3 будет плавать как ионы Cu(OH)+ и NO3- ?
Или CuOH тоже распадется в растворе HNO3 на Cu2+ OH-? И тогда с чем соединятся 2 протона? С ОН- из гидроксокарбоната или с более слабым кислотным остатком CO2-3?
-
3 часа назад, Nemo_78 сказал:
Думаю, что на нынешнем этапе Вашему отпрыску это просто не нужно, т.к. здесь сопрягаются ионное равновесие в растворе слабого электролита (H2S) и ионное равновесие образования/растворения малорастворимой соли (в Вашем случае - сульфида металла), т.к. количественная оценка этих равновесий - следующий шаг, который не следует слишком торопить.
Спасибо. А вот однако ж в домашке на завтра есть "Закончить уравнения реакций:
FeCl2 + H2S = ?
HCl + CuS = ?
Понятно, что чисто механически по указанными правилам это можно сделать (FeCl2 + H2S = FeS + HCl, вторая реакция не идет). Но раз уж я взялся быть его репетитором по химии, хотел в идеале найти какой-то способ логически объяснить эти исключения. А так видимо пока просто придется ему сказать, что H2S - особый случай, а почему - это вы дети "узнаете в старших классах"
-
Доброе утро всем!
Нет ли нестыковки между следующими двумя утверждениями?
1. Слабая сероводородная кислота H2S вытесняет даже сильные кислоты из растворов солей Ag, Cu, Pb, Cd и Hg, образуя с ними осадки сульфидов, нерастворимые не только в воде, но и в образующейся кислоте.
Пример: H2S + CuSO4 = CuS + H2SO4
2. Реагируют с более сильными кислотами нерастворимые в воде сульфиды (кроме Ag2S, CuS) - с выделением H2S
Пример: 2HCl + FeS = FeCl2 + H2S
Чисто логически, не должен ли набор металлов совпадать? То есть, сульфиды тех металлов, чьи соли реагируют с H2S в (1), не должны ведь обратно реагировать с сильными кислотами в (2) с выделением H2S? Иначе получается, что, например, свинец участвует сразу в 2-х реакциях по (1) и (2):
(1) H2S + PbSO4 = PbS + H2SO4, и обратно
(2) H2SO4 + PbS = PbSO4 + H2S
Возможно просто сульфиды Pb, Cd и Hg не поместились в "кроме..." ввиду нехватки места на странице?
И второй вопрос, а что собственно делает H2S такой особенной, что она даже более сильные кислоты из солей вытесняет?
-
Всем доброе утро!
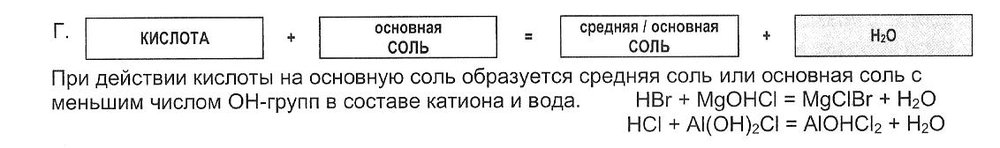
Вот есть такое утверждение: "При действии кислоты на основную соль образуется средняя соль или основная соль с меньшим числом ОН групп в составе катиона и вода".
Дан пример: HBr + MgOHCl = MgClBr + H2O
Хочу это как-то интуитивно увязать с общим правилом "Сильные кислоты вытесняют слабые из их солей", так как данный пример кажется слишком специфичным. Поэтому 2 вопроса:
1. А что, если будет 2 молекулы брома на каждую ионную молекулу соли? Пойдет ли реакция по общему правилу, то есть c с появлением более слабой HCl, что-то типа
2HBr + MgOHCl = MgBr2 + HCl + H2O
2. А что, если более сильная кислота двухосновная? Сильнее HCl я двухосновных не вижу, но предположим в аналогичной ситуации с HF:
HBr + MgOHF = MgFBr + H2O
H2SO4 + MgOHF = MgSO4 + HF + H2O - так?
Если мои догадки верны, то сначала H+ от кислоты бьются за OH- в составе соли, затем (если они еще есть) - за более слабые кислотные остатки, а когда H+ израсходованы, всё, что осталось (включая OH- на которых не хватило H+), сливается в некую мега-соль?
3. И кстати как называть соли типа MgClBr ?
-
Столкнулся с утверждением, что "Газообразные кислотные оксиды не реагируют с нерастворимыми оксидами металлов". Следует ли отсюда, что растворимые оксиды металлов, напротив, реагируют с газообразными кислотными? И причем для этого не обязательно растворение их в воде? И если да, то как это происходит? Типа, пустить (горячую) струю SO2 на порошок CaO -получится сульфит кальция, а на порошок FeO или даже MgO - ничего не произойдет?
Потому как если если идет речь об их реакции в растворе, то ведь это уже и не оксиды никакие, а просто основание + кислота? Смысл утверждения ускользает от меня.
-
3 часа назад, M_GM сказал:
Условие дурное, конечно, т.к. величина "выход" относится к продукту реакции, а не к исходным веществам.
Как верно заметили - должна быть указана плотность раствора (вариант - задача на самостоятельное понимание этого факта и на самостоятельное использование таблицы плотностей - для 8 класса обычно такое не дают)
Можно, конечно, посчитать "мл" опечаткой,
посчитать сколько КОН в 100 г раствора,
посчитать, сколько в нем должно раствориться Al2O3 (теоретически),
затем взять 80% от найденной массы (сколько прореагировало практически)"Если б было дано 100 мг, то 5.6г КОН" в 100 мг раствора не засунешь!

Спасибо. Добрые люди оказывается ведут сайт, где для любой концентрации и плотность, и моль/литр считаются. Выигрыш в точности однако мизерный - не 0.1 моль КОН в растворе, а 0.104 моль.
-
Дано (8 класс): При взаимодействии оксида алюминия с раствором едкого кали образуется комплексная соль. Какое количество вещества оксида алюминия может раствориться в 100 мл раствора гидроксида калия с массовой долей 5.6%, если реакция протекает с 80% выходом?
Если на секунду забыть про 80%-ный выход, то уравнение выглядит вроде так: Al2O3 + 2 KOH + 3 H2O = 2 K[Al(OH)4]
Вопрос такой: а можно ли вообще это решить, не зная плотности именно 5.6%-ного раствора гидроксида калия? Если б было дано 100 мг, то 5.6г КОН - это 0.1 моль, значит с ним прореагирует 0.05 моль оксида алюминия. Как думаете, это опечатка (что возможно - задача в домашке напечатана вручную, а не дана из учебника) или тут есть какая-то хитрость?
И второй вопрос, про "выход". К чему здесь это относится? Типа, должно было получиться 2 моль K[Al(OH)4], а получилось 1.6 моль, значит, и растворилось не 0.005 моль оксида, а 0.04?
-
8 класс, начали кислоты, оперируют понятиями "радиус атома" и "степень окисления"
В таблице силы кислот вижу: HNO3 сильнее, чем HClO3. Рядом, но всё таки сильнее. А почему так?
Насколько я понимаю, в молекуле H-O-NO2 у радикала NO2 набор э.о. 3.44, 3.44 и 3.04 для N, то есть, скажем, в среднем 3.3. Аналогично, у радикала ClO2 - 3.44, 3.44 и 3.2 для Cl, то есть, в среднем 3.36. Что всё таки чуть выше, чем у NO2. Значит, по логике связь с О у радикала ClO2 чуть менее полярная, чем у NO2, и значит связь у O с Н чуть более полярная и следовательно чуть более ионогенная. Так почему же азотная кислота указана как более сильная?
Думал, как здесь радиусы N и Cl могут влиять. Впрямую на удаленность H от O вроде никак. Додумался вот до чего (ищу интуитивное, "на пальцах" объяснение): хотя полярность в связи O-ClO2 чуть меньше, и соответственно плотность менее смещена от центра связи в сторону О, сама связь длиннее и таким образом "центр плотности" всё равно дальше от ядра О, чем в случае с O-NO2. А раз дальше от ядра, значит дальше и от протона H+, который поэтому притягивается слабее и значит отрывается диполем H2O легче.
Имеет такое объяснение право на жизнь или это совсем не в кассу? Аргумент против - это то, что спаривание электронов между О и центральным атомом радикала все равно происходит на подуровне 2p, который (наверное?) всегда одинаково удалён от ядра O. Хотя наверно не может быть одинаково, иначе не было бы понятия "смещение плотности".
Или тут в неподелённой электронной паре Cl дело?
Короче, хильфе битте. Требуется что-то очень простое для уровня 8 класса.
-
5 часов назад, M_GM сказал:
КЧ определяется соотношением многих факторов
- наличие свободных орбиталей для ДА-связей, причем орбиталей наиболее подходящих по энергии
Ве - элемент второго периода, на внешнем уровне - 4 орбитали близких по энергии 2s и три 2p орбитали
Правда, одна из орбиталей атома Ве занята электронами 2s22p0,
но при образовании иона Be2+ (а именно он образует комплекс) эти два электрона уходят.
Потому - четыре ДА-связи и характерное КЧ=4
- Соотношение размеров центрального атома и лигандов - если центральный атом маленький, то подойти к нему на достаточно близкое расстояние много крупных лигандов не могут. Поэтому, например, для одного и того же металла фторидные комплексы могут быть с КЧ=6, а йодидные только с КЧ=4 или ниже;
- Соотношение зарядов центрального иона и лигандов. Лиганды - часто отрицательные ионы, естественно между ними действуют силы отталкивания, этому отчасти противодействует положительный заряд иона металла и прочность ДА-связей. Тем не менее комплексы с КЧ=2z часто определяют максимальное значение КЧ
- реакционные соотношения реагентов. При недостатке реагента-лиганда могут образовываться комплексы с низким значением КЧ (например Cs[Be(OH)3]), при его избытке, в более конц. растворах - с более высоким КЧ, вплоть до максимального Cs2[Be(OH)4]
- В водных растворах часть координационных мест может заниматься молекулами воды, и могут образовываться смешанные комплексы типа К[Me(Н2О)2(OH)4] - а поскольку молекулами воды при записи уравнений и формул в водных растворах часто пренебрегают, то и принимают, что это комплекс с КЧ=4.
А если вспомнить, что на состав комплекса влияет также дентатность (зубастость) лиганда - то не стоит удивляться разнообразию комплексных соединений
В школе (8 класс) - запомнить наиболее часто встречающиеся типы комплексов для самых важных металлов.
Преогромнейшее спасибо! Это стоит того, чтобы заламинировать в памятку! (Я не шучу)
-
4 часа назад, yatcheh сказал:
У бериллия всё просто. Это p-элемент.
Это меня ставит в тупик. В возбужденном состоянии разве что?
Кстати, вспомнил, что в комплексных соединениях вроде должна быть как минимум одна донорно-акцепторная связь. Понятно, когда в sp3 гибридизации участвует хотя бы одна вакантная орбиталь - как например у бериллия было 2s2, стало sp3 - всего 4 орбитали, включая 2 пустых - тетраэдр. И Al(OH)3 сюда тоже хорошо вписывается с 3s2 3p1. Но как быть с d-элементами? И по какому интуитивному правилу получается КЧ=6 ? Понял из ответов выше, что чем больше радиус атома и чем больше электронная плотность, тем больше КЧ. Есть ли граница, после которой не 4, а 6?
-
41 минуту назад, dmr сказал:
ну нет, там вообще никак не объяснено, просто разжевывается определение. Буду пока считать, что это должно быть 4 или 6 - потому что тогда получается красивая объёмная пирамидка (одинарная или двойная). 2 и 3 не катят, потому что плоские, а 5 не подходит, потому что невозможно представить, как это выглядит в объеме. Если только кто-нибудь не подскажет какое-нибудь более интуитивное правило.

.thumb.jpg.8a6f751a33dd10b2b5836f441b0d541b.jpg)





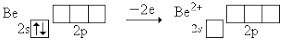
Школьный опыт - вытеснение Cu из CuSO4
в Решение заданий
Опубликовано
Пардон, был неправ - проверил по книжке, Zn правее алюминия и следовательно в реакции с водой должен давать оксид (не гидроксид) и водород.
Таким образом, идут сразу следующие реакции:
1. Окисление цинка
Zn + H2O = ZnO + H2 газ
2. Гидролиз купороса
CuSO4 + 2H2O = Cu2+ SO42- 2H2O = Cu(OH)2 (слаб осн - по табличке должно выпадать в осадок) + 2H+ + SO42- (сильная кислота)(остаток сильной кислоты)
3. Как-то должна выделиться свободная медь Cu0 ? Типа, те ионы Cu2+, которые еще не успели связаться и выпасть как Cu(OH)2, соприкасаясь с ещё не успевшим окислиться Zn0, вступают ним в ОВР и в растворе остаётся плавать Zn2+ , а Cu0 оседает на месте соприкосновения, то есть на грануле цинка?
И где тут цинк реагирует с серной кислотой гидролиза с выделением H2? Реакцию с оксидом вижу:
2H+ + SO42- + ZnO = Zn2+ SO42- + H2O