-
Постов
128 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Весь контент Папа_школьника
-
Уважаемый Пауль С.! Вы не могли бы дать мне какие-нибудь ссылки на получение водорода пиролизом метана - см. мой вопрос в соседней ветке? Ваши ответы самые толковые и по делу, надо признать. Спасибо!
-
Сейчас действительно его дешевле получать из газа паровым реформингом, и даже с учетом потенциальных затрат на улавливание и захоронение СО2 - все равно дешевле, чем электролизом. Однако вопрос был не про экономику процесса, а про условия протекания и механизм, энергозатраты, промышленное воплощение - в плазме / в расплаве. Экономику посчитают экономисты. Спасибо!
-
Ну, вообще то интересует именно пиролиз водорода разными методами - в плазме, в расплаве металлов и т.п., а не паровой реформинг. Вот компания, например, производит пиролизом именно углерод и водород, а никакой не ацетилен: https://monolithmaterials.com/ Возможно... но вопрос был не про конверсию, а про пиролиз: CH4 → C + H2, как-то так. Если на этот процесс расходовать электричество от ВИЭ, то углеродного следа нет вообще.
-
Уважаемые химики, не могли бы кинуть ссылку - где можно почитать про получение водорода пиролизом метана? Ну там, условия протекания и механизм, энергозатраты, промышленное воплощение (в плазме / в расплаве) и т.п. Для читателя с базовым пониманием химии. Если на русском нет, можно на языке шекспира. Спасибо заранее!
-
Подскажите, зачем в задаче подчеркивается, что указанный механизм- неполный? Я решил не добавлять обратную реакцию О2+О2 → О3+О и у меня все равно сошлось с ответом. Типа, есть еще какой-то неуказанный шаг, но он не влияет на скорость? Спасибо
-
Ещё раз перечитал свои заметки с буржуазных лекций... Понятно, что на Курсере не лучшие из лучших выкладывают курсы, а те, наверное, которым их универ какой-то бонус за это дал. В качестве маркетинга. Ну так вот, если рассчитать Formal Charge для этих структур, то он гораздо ближе к нулю для структуры с тремя двойными и одной одинарной. Для себя уяснил, что если ещё и Formal Charge надо в конце рассчитывать, то с таким же успехом (и даже быстрее) можно изначально это вручную делать... И кстати вопрос - а в советской/российской практике преподавания химии понятие Formal Charge вообще используется?
-
Хм, это как же, интересно, "сами"? Экспериментально?)) Про таблицу электродных потенциалов я в курсе, и даже в Кудрявцеве она есть, но что делать, если эту таблицу ещё не проходили, а домашка уже есть: c) KMnO4 + FeSO4 + H2SO4 -> … + … + …+H2O d) KMnO4 +HBr +H2SO4->… + HBrO + …+H2O e) SO2 + KMnO4 + H2O -> K2SO4 + … + H2O f) SnCl2 + K2Cr2O7 + HCl -> SnCl4 + CrCl3 + KCl +H2O g) FeSO4 + KClO3 + H2SO4 -> … + KCl + H2O (Они, кстати, и метод электронно-ионного баланса ещё не проходили, только электронного, и я вообще-то о@%еваю от такого преподавания - это так, примечание в скобках) Ну, положим, про MnO4- легко варианты заучить - их всего 3, и они во многих местах описаны. А вот с ClO3- не так просто - например, в (первом попавшемся на глазах) задачнике Кузьменко-Ерёмина такого окислителя нет среди "типичных": Поэтому и спросил про наиболее полную таблицу...
-
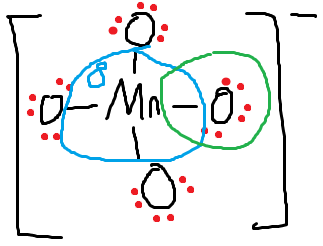
Так я ровно это и нарисовал!!! С черточками вместе поделенных ЭП. Мой вопрос был - почему в википедии и в прочих местах вокруг Марганца "семичетвертные" связи??
-
Типа вот такой, которая в Кудрявцеве, Сост-е уравнений, но чтоб современная и более удобная в использовании? Книга или сайт? Спасибо
-
Точно! Даёшь нашу родную закись-окись марганца вместо вражеского тетраоксида тримарганца!
-
Во-первых, спасибо, что отвечаете на мои дилетантские вопросы! Любопытно, что геометрия центрального атома всё равно тетраэдрическая во всех нарисованных вариантах. Геометрия Электронных Пар вокруг терминальных кислородов разная, но с ней - как я понял - никто не заморачивается и никто её не меряет. Ок, чтобы нарисовать вокруг марганца двойные или даже полуторные связи, кто-то должен был измерить их силу и выяснить, что они крепче (короче) одинарной. Это поэтому их так рисуют? И как это можно оправдать на пальцах? Mn настолько Э.О., что не отпускает свои электроны к кислородам, а оставляет их вокруг себя в "полуторных связях"? Есть наш отечественный путеводитель по рисованию структур Льюиса? Ну там, у Некрасова, Глинки, и т.д.?
-
Ну так я и хочу найти однозначный алгоритм рисования структур Льюиса. Я честно прослушал 2 разных курса на Курсере, и вот какой алгоритм там предлагается: 1. Посчитать общее количество валентных электронов. В случае MnO4- - 32 электрона. 2. Нарисовать базовую структуру с одинарными связями, поместив в центр наименее Э.О. атом. Ок, тратим на 4 связи 8 электронов, остается 24. 3. Помещаем оставшиеся электроны (у нас - 24) вокруг терминальных атомов, давая каждому октет. У нас на это чётко уходят как раз все 24 атома. 4а). Если бы электроны оставались после шага 3, то отдавали бы их центральному атому в виде НП - как в BrF5, например. Тут уже неважно, октет или больше - вокруг центрального атома 4б). Если бы электронов уже не оставалось после шага 3, а у центрального атома не было бы ещё октета, то сдвинули бы какие-то из НП терминальных атомов в двойные связи - как например у COCl2 или CO32- Но нигде я не вижу тут условия, что если после шага 3 у центрального атома - октет, и у терминальных - октет, то я зачем-то должен сдвигать НП от терминальных атомов в двойные связи с центральным? Или - почему марганец должен строить именно 7 связей, если у него 7 электронов? А если это донороно-акцепторная? И вообще, разве в ионе не одна общая каша из электронов? Только я порадовался, что хоть какой-то твердый алгоритм уяснил, а тут нА тебе. Я понимаю, конечно, что американские профессора на Курсере для вас может и не авторитет, и допускаю, что там может быть многое упрощено, но дайте тогда ссылку на какой-нибудь отечественный источник, пусть даже 1960-х годов, НО ТОЛЬКО ЧТОБ ОН ВСЕ СЛУЧАИ ПОКРЫВАЛ?
-
Почему не хватает? 8 электронов в 4-х одинарных связях вокруг марганца, ещё 6*4=24 в неподелённых парах вокруг кислородов. Всего 32, как и требуется - MnO41-
-
Цинк в щелочи, железо в кислоте? (Так, себя проверить)
-
Господа химики, а проясните пожалуйста, почему геометрию перманаганат иона рисуют так замысловато, с двойными или полуторными связями? Чем моя структура хуже, где у каждого атома октет? Откуда там берутся двойные связи, так что у марганца больше чем октет получается?δ
-
Спасибо! Зрелищно. Я имел ввиду, твердые оксиды с газообразными оксидами. А можно ссылку на эту книжку с опытами?
-
Вот-вот, и я тут недавно спрашивал про нагревание оксидов и распад их на ионы... В школьной методичке написано, газообразные с твердыми не реагируют. Но это звучит как-то слишком безапелляционно. А если (амфотерный) ZnO и (кислотный) SO2 очень сильно нагреть и ZnO мелко растереть? И на что распадется ZnSO3, если он не устойчив термически?
-
Если оксиды реагируют без воды - в расплаве - то распадаются ли они на ионы? Например, какое ионное уравнение будет у реакции BaO + SiO2 => BaSiO3 Вероятно, встретиться четырем ионам для создания BaSiO3 маловероятно, видимо просто молекулами плавают? Но затем в расплаве соль все таки в виде ионов Ba2+ и SiO32- ? А если ливануть SO3 на Na2O, то они сначала распадаются на ионы, чтобы затем сформировать Na2SO4? Спасибо!
-
Спасибо. Т.е. с одной стороны, связь H-А должна быть не очень-то полярна, чтоб диссоциация не так легко происходила, а с другой стороны в центре должен быть сильно э/отрицательный элемент в высокой степени окисления. Понятно, это исключает бескислородные кислоты. Я просто пытаюсь для себя какую-то интуитивную логику нащупать. Не запоминать же каждый раз - окислитель/не-окислитель и т.д. Я надеюсь, что за способность разбираться во всём этом хорошо платят где-нибудь... ))
-
Это для меня новое знание, приму это пока как данность. Из этого однако следует, что хлорноватая кислота HClO3 должна быть более сильным окислителем, чем хлорная - молекул HClO3 плавает больше, чем у хлорной, а С.О. хлора всё ещё достаточно высокая +5
-
Наглядно, спасибо. Остается понять, что именно разносит - Cl2 или какой-нибудь оксид Cl20 или ClO2 ?
-
Спасибо. А это какая реакция будет? а то в сервисах её нет. В Википедии пишут только: Неметаллы и активные металлы восстанавливают концентрированную хлорную кислоту до хлороводорода И "взрыв" - это что вообще? Очень быстрая сильно экзотермическая реакция?
-

.thumb.jpg.8a6f751a33dd10b2b5836f441b0d541b.jpg)