-
Постов
46784 -
Зарегистрирован
-
Посещение
-
Победитель дней
391
Тип контента
Профили
Форумы
События
Сообщения, опубликованные aversun
-
-
В 05.06.2024 в 13:52, Nemo_78 сказал:
Может, я уже сурово от жизни поотстал...
Но разве в электронном балансе не о степенях окисления речь?! А они, вроде раньше в отличие от зарядов ионов наоборот записывались, т.е. "+4"... Или сейчас всё настолько сурово в методике химии поменялось?
Таких тонкостей даже не знал, вероятно, в те времена когда я учился их не было, а может просто забылось....
Речь идет о степенях окисления, т.е. +4
-
В 05.06.2024 в 12:33, Вольный Сяншен сказал:
Левая и правая части не уравнены.
Так там не уравнение, а просто направление реакции...
-
В 05.06.2024 в 09:59, Solovey сказал:
4+
бывает...
-
В 05.06.2024 в 09:15, Aisha120 сказал:
N02 выделяется по условию
С конц. HNO3 так и будет
-
-
Zn + HNO3 => Zn(NO3)2 + NO2 + H2O
2|N5+ +e = N4+
1|Zn0 -2e = Xn2+
Zn + 4HNO3 = Zn(NO3)2 + 2NO2 + 2H2O -
В 04.06.2024 в 16:37, podlyinarod сказал:
Здрасьте, я Ваша тётя! Так ведь концентрация протонов околонулевая. Потеря гидратной оболочки играет роль, что ли?
Железо не раств. в воде и р-рах холодных щелочей, реагирует с разб. к-тами, образуя соли Fe(II), и горячими конц. р-рами щелочей.
Химическая энциклопелияFe + 2NaOH (конц.) + 2H2O = Na2[Fe(OH)4] + H2↑ [кип. в атмосфере N2]
4Fe + 20NaOH (конц.) + 3O2 + 6H2O = 4Na5[Fe(OH)8]↓ [20-25° C]
Лидин-
 1
1
-
-
В 04.06.2024 в 14:24, nuke86 сказал:
Спасибо. правда все еще остается вопрос, почему используется и сталь и пвх. 09г2с применяется для менее концентрированной из-за возможной кристаллизации, или в чем может быть причина
С высококонцентрированными растворами щелочи, особенно горячими, железо потихоньку взаимодействует с образованием водорода.
-
CO + SO3 = CO2 + SO2 при Т>450C
-
В 02.06.2024 в 17:16, Terminalhead сказал:
Здравствуйте.
Работал ли кто-нибудь с Yb2Ti2O7? Подскажите, пожалуйста, в чем его можно растворить? Может быть, ссылки на статьи есть?
В расплаве пиросульфата калия
-
В 02.06.2024 в 07:49, user2022 сказал:
Проблема контакта электроплитки со стекляшками похоже еще большая. Может там какую пластиковую прокладку можно ставить (типа силикона) ? Или ее может перегреть легко ? Большой воздушный зазор и сетки как-то намекают на большое тепловое сопротивление. Из простого мож ставить кольцо из жести вокруг стекляшки на плитку и засыпать песком все - но потом при разборке песок будет все засыпать ниже.

-
 1
1
-
-
В 02.06.2024 в 09:27, Himozza777 сказал:
В чём различие этих реакций?
В степени окисления.
-
В 01.06.2024 в 04:40, Родион21 сказал:
А если использовать флюс - состав конечного продукта изменится? Я собираюсь использовать просушенный хлорид кальция.
Вряд ли, да и не годится двуокись церия для этого, по лит. данным используется хлорид церия.
-
В 01.06.2024 в 07:47, dmr сказал:
Если жирные кислоты в свободном виде, а не в виде солей, то они легче воды, а нужные вещества тяжелее
а не растворяются ли нужные вещества в жирных кислотах, да еще лучше, чем в воде?
-
В 31.05.2024 в 22:35, yatcheh сказал:
Посадить на анионит.
Так может нудные вещества тоже кислоты....
-
В 31.05.2024 в 22:26, SFGn_5 сказал:
Есть некая смесь,состоящая из олеиновой,миристиновой и стеариновой кислоты,парочки нужных веществ и небольшого количества терпенов.Последними пренебрегу.Как избавится от жирных кислот?
Не зная, что за нужные вещества, нельзя сказать как отделить жирные кислоты...
-
В 31.05.2024 в 17:57, Родион21 сказал:
Здравствуйте, меня интересует получение металлического (желательно чистого) церия из его диоксида с помощью магния.
Но какие пропорции нужно соблюсти для оптимальной реакции?
Вы получите сплав магния с церием, именно так получают сплавы алюминия с церием, правда церий берется в виде фторида.
-
В 30.05.2024 в 19:34, Wolfy36 сказал:
Как синтезировать трихромат калия не используя хромовый ангидрид? нашел в одном месте что его можно получить добавляя к хромату избыток кислоты, через образование дихромата
и в некоторых местах про азотную кислоту видел, у меня есть только 57%
 Н.С.Ахметов Общая и неорганическая химия
Н.С.Ахметов Общая и неорганическая химия
-
В 29.05.2024 в 09:09, dmr сказал:
Чот загнул однако
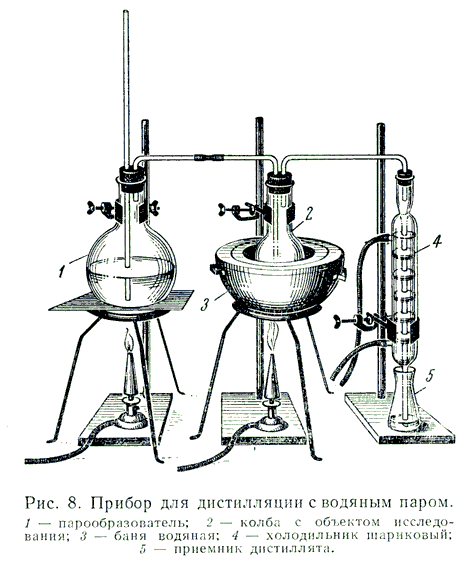
Ну, не водой, а острым паром при 450-500С, продувая его над NaCl так что бы он уносил HCl из зоны реакции.
-
В 29.05.2024 в 09:00, fossilknife сказал:
Здравствуйте! В справочнике Лазарева про гидразин гидрат пишут
Но разве основные опасности при работе с ним это химожоги и опасность возгорания?
Еще отравления, о которых четко пишет автор
-
 1
1
-
-
В 28.05.2024 в 18:51, Алиша0415 сказал:
Да, рассматривался этот раствор, потому что работа по фарм препаратам, поэтому такой дали.
Какие реакции протекают, если раствор 0.1% : 1-нагреть, 2- если его открыть , как он в с воздухом прореагирует, 3- и если его оставить на свету. Написать химизм реакции и попробовать их описать, можно простыми словами
Ну давайте, пишите, мы, если что неправильно, подскажем. Или вы хотите, что бы все сделали за вас, тогда на хрен нам нужны такие фармацевты, еще отравите...
-
 1
1
-
-
В 28.05.2024 в 16:20, Алиша0415 сказал:
Мы рассматриваем спиртовой раствор йода. (Антисептик 5%). Из него сделали раствор 0.1% И уже исследование проводится с ним. нужно описать и написать реакции под действием внешних факторов т. е. Свет, нагрев, воздух, что там происходит, какие протекают реакции.
Так что вы от нас хотите?
Кстати, раствор йода медицинский, это не совсем раствор йода, там еще и йодистый калий присутствует.
-
В 27.05.2024 в 07:39, ellamalyshka13 сказал:
я от балды написала конечно,но такое бывает ?🙏
Не бывает, маловат потенциал у перманганата в щелочной среде, что бы аммиак так окислить. Тут скорее просто аммиак улетит под воздействием щелочи, а перманганат перейдет в манганат и двуокись марганца.
-
 1
1
-
-
В 25.05.2024 в 08:50, Вадим Вергун сказал:
Если цель получить щёлочь - что соду, что поваренную соль, можно гидролизовать водой уже при 400С.
Так проще так Na2CO3 + Ca(OH)2 = 2NaOH + CaCO3↓
Старый испытанный способ


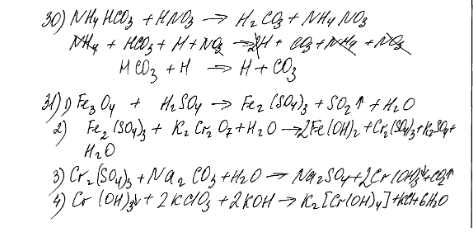
 Н.С.Ахметов Общая и неорганическая химия
Н.С.Ахметов Общая и неорганическая химия
Помогите найти ошибки в заданиях ЕГЭ
в Решение заданий
Опубликовано
Интересно, как пошла бы реакция при добавлении серной кислоты?