Поиск
Показаны результаты для тегов 'Комплексы'.
Найдено 20 результатов
-
Существуют ли доступные вещества, аналогичные краун-эфирам, способные образовывать хелаты с ионами щелочных металлов, кроме диглима? Может какие-то производные диэтаноламина способны проявлять аналогичные свойства?
-
Мне нужна помощь в реакциях периодатокупрата меди с соляной кислотой, щелочью, Na2S и KI какие будут продукты реакции?
-
Рассчитать Константу равновесия по уравнению Фуосса -Эйгена
Акулина опубликовал тема в Решение заданий
Используя уравнение Фуосса — Эйгена, рассчитайте значение Kравн. следующей реакции, если расстояние максимального сближения равно 2 Å. [Ni(H2O)6]2++NH3⇄{[Ni(H2O)6Y]2+} Ответ представьте в виде a⋅10b⋅м3/моль. В ответе приведите значения a и b с точностью до целых. _______________________________________________________________________________________________________________________ В теоретической части есть выкладки: Kравн.. можно оценить по уравнению Фуосса — Эйгена: Kравн.=4/3πa3NAe−V/RT где a — это расстояние максимального сближения комплекса и входящей группы, V — потенциальная энергия кулоновского взаимодействия ионов для данного расстояния. Последняя может быть рассчитана как V=z1z2e2/4πϵa Где-то бы посмотреть ходя бы подход к уравнению Фуосса-Эйгена. МГУ-шный учебник посмотрела. в интернете не нашла- 17 ответов
-
- фуосса-эйгена
- конст_равно
- (и ещё 3 )
-
Когда-то давно восстанавливал бихромат, с целью получения хромовых квасцов, добавлял серную, и органику – крахмал, сахар, целлюлозу, но точно не помню. Далее в горячий полученный раствор добавлял алюминиевые квасцы, при кристаллизации хром частично захватывался. Сейчас решил утилизировать раствор, осадив хром содой, однако никакого осадка не выпадает, не шипит, никакой реакции. Окраска раствора "хромовая" фиолетовая. К тому же раствор не испаряется, а стоял открытый года два, никакие кристаллы не выпадают. Наверное образовался сильный комплекс, хром алюминий карбоновая кислота? Любопытно узнать что это может быть.
-
осмос основные типы реакций и хим процессов в живых систем
HoholMAN опубликовал тема в Решение заданий
Прошу помощи по 1, 2 и 3 заданию, в первом ясно, что произойдет с клеткой, но как подтвердить это рассчетами? -
Рассчитайте длину волны максимума поглощения видимого света комплексом [CN (NH3)6]2+, если энергия расщепления d уровня составляет 180.1 кДж/моль.
-
Помогите посчитать координационное число соединения [Pt(NH3)6]4+ и тип гибридизации центрального атома. И объясните,пожалуйста,по какому принципу это ищется
-
Здравствуйте помогите с синтезом комплексов лития!
-
Друзья, срочно нужна помощь! Для дипломной работы нужно получить комплексы лантана (есть его хлорид) и церия (нитрат) с органическими лигандами (8-оксихинолин, салициловая кислота, 2,2`-дипиридил). Проблема в церии - с ним ничего не выходит :( Подскажите, пожалуйста, что можно использовать в качестве лиганда с церием? Может, кто-то им занимался? Как его можно исследовать? Конечная цель - измерить спектральные характеристики комплекса и посчитать Кн.
-
Объясните, почему при добавлении йодида калия к раствору нитрата диаминсеребра (I) наблюдается образование осадка йодида серебра. ответ подтвердите расчетом. KI+[Ag(NH3)2]OH + 2 H2O = AgI+KOH+2(NH3*H2O)
-
Есть комплексное соединение K4[Fe(CN6)] в растворе, концентрация Cисх = 0.1 моль/л, константа нестойкости = 10-37. Этот раствор содержит избыток лиганд(ов) в виде в-ва KCN с молярной концентрацией Cизб = 1 моль/л. Нужно найти концентрацию комплексообразователя и лиганда. Решал так: [Fe(CN6)] = Fe + 6CN x = концентрация комплексообразователя (Fe) По формуле Kнестойкости= x * ( Cизб + 6x )^6 ) / (Cисх - x) нашёл x. Вопрос: концентрация лиганда будет равна Cизб, Сизб + 6x или 6x?
-
Как рассчитать массу гексагидроксоарсената натрия в растворе?
АгатаКот опубликовал тема в Решение заданий
Найти массу гексагидроксоарсената 3 натрия, содержащегося в растворе, если на окисление его израсходовано 15 мл. 0,1 м раствора йода. Помогите пожалуйста -
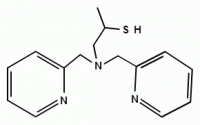
Здравствуйте, уважаемые форумчане! Я был бы очень признателен, если бы вы помогли справиться с одной задачей. Данная задача была во втором теоретическом туре заключительного этапа ВсОШ. Собственно, текст: Комплексное соединение Х, окрашенное в желтый цвет, было синтезировано в присутствии HBF4 в ходе окислительно-восстановительного взаимодействия ацетилацетоната меди (II) (далее Cu(acac)2) и N-(2-маркаптопропил)-N,N-бис(пиридилметил)амина (далее HL), его строение на картинке. В растворе Х имеется двухзарядный ион с отношением M\z = 335,91. При стоянии раствора Х на воздухе началась другая окислительно-восстановительная реакция, в результате которой цвет раствора Х начал меняться с желтого на зеленовато-голубой, а через 3 дня образовались кристаллы Y, в котором содержится четырехзарядный молекулярный ион с отношением M/z = 379,91. При взаимодействии комплекса Y с раствором соли Li, выпал белый осадок Z с M=101,9 г/моль. При электролизе оставшегося после фильтрования раствора комплекс X количественно регенерируется. Вопросы: 1. Определить состав катиона соед. Х и написать описанную реакцию его образования из Cu(acac)2 и HL в ионном виде. Обосновать свои выводы. 2. Определить состав соли Z и соединения Y. Ответ подкрепить расчетами и рассуждениями. В чем заключаются необычные свойства соединения X. Примечания. 1. Все реакции проводились в безводных растворах. Орг. растворители, применяемые в процессах, не входят в состав продуктов X, Y и Z. 2. Считать, что упомянутые комплексы содержат BF4- в качестве аниона. Катионы X и Y не содержат бора и фтора. Заранее спасибо!
-
какой объем свежеприготовленного 3,29% раствора NaOH(р=1,035) надо добавить к 158,19 мл 10% раствора нитрата алюминия(р=1,081 г/мл) для того, чтобы 10% катионов алюминия из раствора соли перешла в анионный комплекс. Что изменится, если вместо свежеприготовленного раствора щелочи возьмем раствор, простоявший в открытой банке в течение полугода? напишите уравнение реакций. напишите, хотя бы уравнения, или термины объясните. и какой комплекс будет?
-
Всем доброго времени суток, не могли бы вы подсказать как в комплексах, находить координационное число и составлять структурную формулу. Заранее спасибо.
-
- лиганды
- структурные формулы
-
(и ещё 1 )
C тегом:
-
К раствору соли Cu2+ добавьте по каплям разбавленный раствор аммиака.Полученный осадок гидроксида растворите в избытке раствора NH3(можно добавить 2-3 капли концентрированного NH3*H2O).Полученный раствор комплексного соединения разделите на 2 части.К 1 части добавьте 2-3 капли разбавленного раствора щелочи (NaOH или KOH), ко 2-й-столько же раствора сульфида натрия или аммония.Что происходит?Напишите уравнения реакций.Объясните наблюдаемые явления с позиций смещения равновесий,используя данные о величинах произведений растворимости соответствующих гидроксидов и сульфидов и констант образования комплексных ионов. Наблюдение:в 1-й части добавив раствор щелочи (NaOH) получается жидкость голубого цвета.Во второй части добавив сульфид натрия получается жидкость черного цвета (как нефть). Ур-ия реакций:CuSO4+2NH4OH=(CuOH)2+(NH4)2SO4...... Какие реакции дальше писать надо? Как объяснить наблюдаемые явления с позиций смещения равновесий, используя данные о величинах произведений растворимости соответствующих гидроксидов и сульфидов и констант образования комплексных ионов???
- 2 ответа
-
- Опыты
- Комплексные соединения
- (и ещё 3 )
-
Подскажите полярны молекулы или нет? Я кое-что по Гиллеспи для них рассчитал, а дальше не знаю что :( NF3: AX3E, тригональная пирамида (вроде полярная). CS2: AX2E, угловая ICl5: AX5E, квадратная пирамида [Al(OH)4]^- :AX4, тетраэдр
-
- Полярность
- форма молекулы
-
(и ещё 5 )
C тегом:
-
Помогите пожалуйста решить задачки: 1) Определите молярную концентрацию, титр и титр по определяемому веществу Со[Т(ЭДТА/Со)] рабочего раствора ЭДТА (V=18,46мл) по результатам титрования навески установочного растовра Zn m=0.0131г 2) Какую массу Co(NO3)2 * 6H2O содержащего около 7% индиферентных примесей, следует взять для анализа, чтобы на титрование ее потребовалось около 10 мл 0.1 М ЭДТА?
-
- аналитика
- титрование
- (и ещё 5 )
-
Здравствуйте. Помогите пожалуйста разобраться с комплексами. По какому принципу они образуются и как разрушаются? К примеру, дано задание: "Какое комплексное соединение получится при взаимодействии сульфата алюминия с избытком гидроксида калия. Составить выражение константы нестойкости. Как можно разрушить данное комплексное соединение?" Как узнать какое соединение получится и чем его можно разрушить. Спасибо.