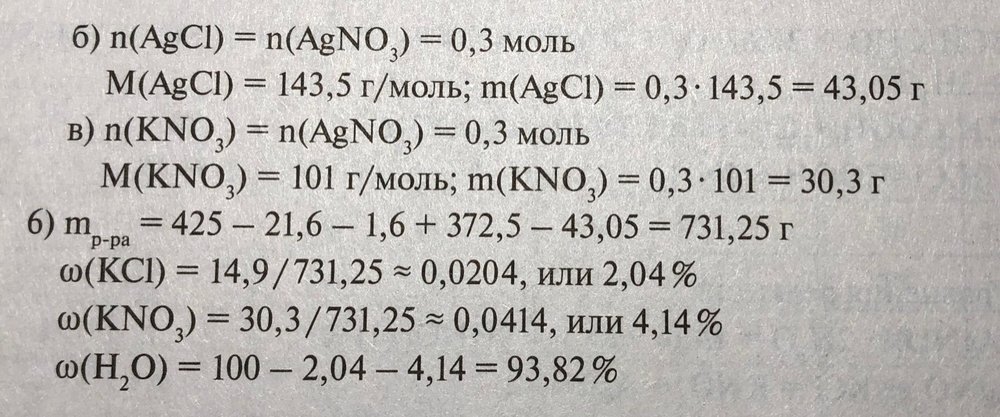Поиск
Показаны результаты для тегов 'Массовая доля'.
Найдено 49 результатов
-
Прокалили смесь гидрокарбоната и нитрата натрия и получили 20 дм³ (н.у.) смеси газов с относительной плотностью по водороду 20. Определите массовые доли солей в их исходной смеси
- 3 ответа
-
- смеси
- массовая доля
-
(и ещё 1 )
C тегом:
-
При взаимодействии карбида кальция массой 170 г с водой получили продукты реакции, среди которых присутствует непредельный углеводород, который при взаимодействии с аммиачным раствором оксида серебра даёт осадок массой 180 г. Необходимо рассчитать массовую долю (%, с округлением до сотых): 1) содержания элемента углерода в ацетилениде. 2) содержания примесей в карбиде кальция. Моё решение не приняли, у меня получалось (1) содержание углерода в ацетилениде ~10,01% и (2) содержание примесей в карбиде кальция ~28,24% (решения не приняли, но как минимум первый процент правильный) Учитель помогать не хочет и самого всё плохо получается. Желательно писать чуть подробнее чтобы было проще понять. Заранее спасибо за любую помощь!
- 1 ответ
-
- массовая доля
- примеси
- (и ещё 3 )
-
Здравствуйте! При решении задачи столкнулась с неточностью в ответе. В решении, указанном составителями сборника, в ответе не учитывается концентрация HNO3, хотя при расчёте массы раствора массу азотной кислоты не вычли. То есть в растворе она есть, но её массовую долю не находят. Можете ли объяснить, почему? Или же это просто неточность или опечатка? Заранее благодарю за помощь. Прикрепляю условия задачи и решение:
- 1 ответ
-
- егэ
- егэ по химии
- (и ещё 7 )
-
Как экпериментально можно определить массовую долю вещества в растворе?
-
Помогите, пожалуйста с задачей Определите массовую долю атомов хлора в смеси,состоящей из 1,12дм3-Cl2,11,2дм3-H2 и 2,24дм3-HCl (н.у.) Вот, что я нашла, а дальше тупик: n(Cl2)=0.05mol n(HCL)=0.1mol n(h2)=0.5mol m(cl2)=1.775g m(hcl)=3.65g m(h2)=0.5g Помогите, пожалуйста
- 15 ответов
-
- газы
- смесь газов
-
(и ещё 1 )
C тегом:
-
Помогите, пожалуйста с задачей Определите массовую долю атомов хлора в смеси,состоящей из 1,12дм3-Cl2,11,2дм3-H2 и 2,24дм3-HCl (н.у.) Вот, что я нашла, а дальше тупик: n(Cl2)=0.05mol n(HCL)=0.1mol n(h2)=0.5mol m(cl2)=1.775g m(hcl)=3.65g m(h2)=0.5g Помогите, пожалуйста
-
Как рассчитать массовую долю, если я не знаю массу навески?
MaryMry опубликовал тема в Решение заданий
Помогите, пожалуйста, решить задачу. Вроде в аналитике соображаю, но здесь растерялась На титрование 15,00 см3 раствора стрептоцида расходуется 9,40 см3 раствора нитрита натрия с титром по сурьме (III) равным 0,006055 г/см3. Рассчитайте массовую долю (%) стрептоцида в растворе.- 1 ответ
-
- анатилика
- массовая доля
-
(и ещё 1 )
C тегом:
-
Раствор гидрокарбоната калия прокипятили таким образом, что испаряющаяся вода конденсировалась и возвращалась в исходный раствор. В результате образовался раствор с массовой долей средней соли 3,49%. Определить массовую долю гидрокарбоната калия в исходном растворе. Ответ: 5%
- 1 ответ
-
- задача
- массовая доля
-
(и ещё 1 )
C тегом:
-
на раствор. при решении составленного уравнения ухожу в минус.
Oxana88 опубликовал тема в Решение заданий
у кого сойдется с ответом. я при решении составленного уравнения ухожу в минус Рассчитайте объем хлороводорода (н.у.), который следует пропустить через соляную кислоту массой 500 г с w(HCl) = 5% для получения раствора с молярной концентрацией HCl 2,0моль/л (плотность = 1,03 г/мл). Ответ : 7л -
Здравствуйте! Подскажите, пожалуйста, по вот такой теме : при расчете массовой доли вещества в растворе стоит ли учитывать массу образовавшегося осадка, или же из массы общего раствора необходимо ее вычитать?
-
92 г этанола нагрели в присутствии концентрированной серной кислоты. После приведения полученной смеем к нормальным условиям она была полностью поглощена 200 г 40 мас. % раствора брома в четыреххлористом углероде. Раствор при этом обесцветился. Определите состав продуктов, полученных при нагревании этанола, в массовых процентах, считая, что этанол прореагировал полностью. Образованием эфиров серной кислоты и этилового спирта пренебречь.
-
Смесь порошков алюминия и серы прокалили в токе кислорода, при этом масса полученных оксидов оказалась равной массе исходной смеси алюминия и серы. Найдите массовые доли алюминия и серы в их исходной смеси.
- 6 ответов
-
- массовая доля
- алюминий
-
(и ещё 2 )
C тегом:
-
какой объем свежеприготовленного 3,29% раствора NaOH(р=1,035) надо добавить к 158,19 мл 10% раствора нитрата алюминия(р=1,081 г/мл) для того, чтобы 10% катионов алюминия из раствора соли перешла в анионный комплекс. Что изменится, если вместо свежеприготовленного раствора щелочи возьмем раствор, простоявший в открытой банке в течение полугода? напишите уравнение реакций. напишите, хотя бы уравнения, или термины объясните. и какой комплекс будет?
-
Массовая доля элемента Х в кристаллогидрате Na2X2O7 ∙ 2Н2О составляет 34,90%. Вывести формулу кристаллогидрата. Закончить уравнение реакции: Na2X2O7 + SO2 + H2SO4 →
-
Какую массу продукта, содержащего 98% м-нитробензальдегида (М=151,13 г/моль), нужно взять на анализ, чтобы после добавления к ней солянокислого гидроксиламина выделившуюся хлороводородную кислоту можно было оттитровать 20,00 мл 0,1 М NaOH(К=1,048). Первым делом надо найти количество HCL и уже по нему определяться дальше?или я не так рассуждаю
-
Здравствуйте, скажите пожалуйста есть ли какая-нибудь книга в которой есть таблицы зависимость плотности раствора от массовой доли растворенного вещества. Желательно, на все соединения.
- 1 ответ
-
- плотность раствора
- концентрация раствора
- (и ещё 1 )
-
Помогите решить практическую задачу.Имеется раствор Н2SO4 20 г\л .Плотность исходной кислоты 1,83.Сколько % ным является этот раствор?
-
Подскажите решение задачки. Из руды (0,5000 г) получили осадок Zn2P2O7 и Cd2P2O7 общей массой 0,7532 г. После этого получили сульфид цинка и далее ZnO, массой 0,3942 г. Найти массовые доли цинка и кадмия в руде. Как я понял, цепочка будет такая: Руда(о.к. Zn, Cd)---Zn2P2O7, Cd2P2O7---ZnS---ZnO Находим массу цинка: m=F*m(гр.ф)=(M(Zn)/M(ZnO))*m(ZnO)=... Далее массовую долю цинка: ω(Zn)=m(Zn)/m(нав)=... А вот как найти кадмий?
-
-
- Массовая доля
- Титр раствора
- (и ещё 2 )
-
Помогите! Очень прошу!! Навеску алюминиевого сплава массой 0,500 г растворили в мерной колбе вместимостью 100.0 мл. После соответствующей обработки для определения Mg 20,00 мл раствора оттитровали 12,60 мл 0,01000 М ЭДТА. Вычислить массовую долю магния в алюминиевом сплаве.
-
- массовая доля
- титрование
- (и ещё 1 )
-
Из 25 г 30% NaOH раствора приготовили 150 г NaOH раствора
Capybara4 опубликовал тема в Решение заданий
Из 25 г 30% NaOH раствора приготовили 150 г NaOH раствора. Какая была получена массовая доля, выраженная в % ? -
1. Сколько граммов 25%-го раствора гидроксида калия нужно прилить к 400 мл воды, чтобы приготовить 15%-й раствор? 2. Сколько мл 2 н. раствора серной кислоты нужно взять для приготовления 3 л 0,06 н. раствора?