-
Постов
33306 -
Зарегистрирован
-
Победитель дней
1104
Тип контента
Профили
Форумы
События
Сообщения, опубликованные yatcheh
-
-
и перекись не с кислородом реагирует при тех условиях, а с оксидом азота.
Моя гипотеза страдает многими непонятками, но вот в реакцию перекиси с окисью азота я не верю, хоть убей - не верю!

Всё-таки считаю, что окись азота не разлагается, а просто - не образуется.
-
 2
2
-
-
Как? Помогите пожалуйста
Берём произведение растворимости сульфата свинца (ПР)
ПР = [Pb2+]*[sO42-] = 2.2*10^-8
Это есть произведение концентраций ионов свинца и сульфата в моль/л
Растворимость его в чистой воде (г/л) = корень.квадратный из ПР, умноженный на молярную массу сульфата свинца.
Получается 303*1.48*10^-4 = 0.045 г/л
Для раствора в 0.1 М растворе сульфата натрия вычисляем концентрацию ионов свинца:
C(Pb2+) = ПР/[sO42-] = ПР/0.1 = 10*ПР
И умножаем на молярную массу сульфата свинца. Опять же получаем растворимость в г/л
Получается 2.2*10^-7*303 = 0,000067 г/л
-
Так реакция перекиси с оксидом азота более вероятна, чем с радикала с оксидом азота - из-за концентраций. Вот я и пытаюсь найти такие, которые уменьшают скорость - другой вопрос, что не получается...
Атомарный азот может быстрее атомарного кислорода выбывать - например, на молекулах азота, которого очень много в данном случае ?
Разумеется, он выбывает, и атомарный кислород выбывает. Если бы не это выбывание - весь избыток кислорода давал бы NO. Я только о том говорю, что добавляя перекись, мы вводим дополнительную (и - мохбыть весьма эффективную) ловушку для радикалов, которая радикально (пардон за каламбурчик) укорачивает цепи, обрывая их, не давая им развиться даже в той мере, которую позволяют прочие обрывальщики.
Кстати, атомарный азот на молекулах азота "выбывать" никак не может
N + N2 = N2 + N
это вырожденная реакция.
У него и без азота есть на ком оторваться

-
 1
1
-
-
H2O2 + NO --> N + H2O + O2 ?
Ну, это уж совсем нереальная реакция! Да и толку от неё никакого, ибо дальше последует:
N + O2 = NO + O
O + N2 = NO + N
и всё вернётся на круги своя

Вы пытаетесь найти процесс, в котором NO возвращается к азоту, но перекись тут не поможет. Мне кажется, что дело как раз в том, что NO просто не образуется. Точнее - падает скорость её образования.
-
Вечная проблема - критики. Не так, не то... А сами что написали?
А МНЕ ПОНдРАВИЛОСЬ!
А кто спорит? Автор хотел критики - её есть у меня. Если бы он просто тиснул стих - я бы просто лайкнул (или не лайкнул).
Вечная проблема критика - знаешь как не надо, а как надо - не можешь

-
 1
1
-
-
1 Кроме написанных реакций возможны же подобные : N + N --> N2 O + O --> O2 O + CO --> CO2 и прочие варианты их выбытия. Пусть вероятность таких реакций не нулевая - может они в сумме с прочими реакциями и дают уменошение NOx ровно на 30% ?
Рекомбинация радикалов - это редкие случаи. Концентрация радикалов всегда мала, их встреча маловероятна. Гашение их, конечно, возможно разными способами. Но если мы к тем "гасителям", которые и так присутствуют в смеси и ограничивают образование NO, добавим ещё один гаситель, может быть более эффективный - это же должно как-то повлиять на процесс.
-
Здравствуйте! Помогите,пожалуйста с задачей:
"Каким способом можно получить из циклогексанола цис-1,2-циклогександиол? Как получить транс-изомер?"
1)Насколько я понимаю, можно вначале получить из циклогексанола циклогексен,а потом получить транс-1,2-циклогександиол (циклогексен реагирует с hcooh и h2o2(водным раствором)).
2) А вот как получить цис-изомер?) Подскажите,пожалуйста.
Цис-изомер получается гидроксилированием циклогексена четырёхокисью осмия или KMnO4 в щелочной среде. Промежуточный продукт - циклический эфир, при гидролизе которого разрываются связи металл-кислород, поэтому конфигурация атомов углерода сохраняется.
-
 1
1
-
-
Ожидаю конструктивной критики.
Ащ-щ-на! Какая может быть "конструктивная критика" в таком вопросе? Типа - "я бы лучше так написал: ", так что ли?

В целом: антивоенный манифест. Смысл ясен, посыл очевиден, никакой метафизики.
"Здер пальцы в кровь взводя гранату
Шагнул вперед - раздался взрыв"
"Здер" - это словотворчество, или что-то другое?
"взводя гранату" - ну, ладно, это оружейно-технические тонкости.
"Гремели танки". Гремели пушки - очевидно. Танкам всё же более пристало реветь, а не греметь.
"Взрывались мины, словно вата" - попытка уместить в три слова образ восприятия взрывов оглушенным солдатом, когда всё как сквозь вату. Но - неудачно, корёжит.
"За разум огненная плата
Бессмысленный кровавый вал"
Тире пропущено. "За разум"? Да здравствует разум, да сгинет маразм! ©

"Вмиг вспышка, грохот, гул моторов
И вертолетов быстрый ключ
Пытало небо, что есть взору
Тянулся смрад могильных куч"
"Ключ вертолётов"? Сомнительная метафора.
А вот "смрад могильных куч" - это вообще за гранью добра и зла. Могильным может быть холм, курган, ров, яма, наконец. Но - куча...
Да и рифма "ключ-куч" зубодробительно пошлая.
"А генералы в кабинетах
Костюм, при галстуке, в очках"
Генералы - и в костюмах?
Ну, дальше идёт пафосная кода.
"Я верю что вселенской тростью
Планета упокоит прах"
Что это за трость такая?
Или она возникла, как рифма для колосьев? Без колосьев-то никак

Критика была достаточно конструктивной?

Братья-химики во литературе! Заклинаю вас! Не будьте рабами рифмы! Не идите за ней!
И не тужьтесь! Она сама выйдет!

-
Потому что они не реагируют со щелочью?
Именно поэтому
-
-
-
Хоть бы одного сторонника увидеть/услышать. Какие-то они развоплощённые.
-
Спасибо большое!)
за счёт эффекта сопряжения образующейся кратной связи с метильными группами.
Блин, сверхсопряжения, сиречь - гиперконьюгации.
-
"При взаимодействии 2-бром-2-метилбутана с этанолом при 25 градусах цельсия образуются 3 соединения:
а)2-метил-2-этоксибутан
б)2-метилбутен-2
в)2-метилбутен-1.
Предложите механизм, объясняющий образование каждого. Как нужно изменить условия,чтобы главным стало б)? Чтобы главным стало в)?"
Подскажите,пожалуйста,решение)
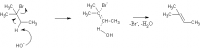
Образование продукта а) идёт по механизму Е1 в присутствии слабого основания (например, Na2CO3):
CH3-CH2-C(CH3)2-Br --(-Br-)--> CH3-CH2-C+(CH3)2 --(C2H5OH, H+)--> CH3-CH2-C(CH3)2-O-С2H5
Na2CO3 + HBr ----> NaHCO3 + NaBr
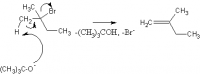
Отщепление по правилу Зайцева идёт по механизму Е2 под действием сильного основания малого объёма. Например - щёлочи:
В этом случае основным является стабилизация переходного состояния за счёт эффекта сопряжения образующейся кратной связи с метильными группами.
Отщепление по правилу Гофмана идёт так же по механизму Е2, но под действием сильного основания с большим объёмом, например - трет-бутилат-аниона:
Ещё лучше под действием триэтилметилата ((С2Н5)3СО-) - на 90% по Гофману.
В этом случае основную роль играет индуктивный эффект брома и лёгкость отщепления протона, поскольку атака по вторичному атому стерически затруднена.
-
 1
1
-
-
Я был скрытым диссидентом еще во времена СССР. Писал письма на Би-Би-Си, Севе Новгородцеву. Не доходили. За мной явно было ленивое наблюдение. Как-то на первомайской демонстрации (мероприятие обязательное!) один мой однокурсник начал себя не корректно вести. Ну, там, обычные псевдолозунги, вроде "Советскую милицию - в космос!", и так далее. На демонстрациях и не такое кричали. К нему подошли, спросили: ты - Иванов? Ну, вот такая у меня фамилия. Он Ивановым не был. Ожидали выходок именно от меня.
Ну, енто... Власть меняется, натура не меняется.
О, да! Настоящий интеллигент должен быть в оппозиции к любой власти!
В российских реалиях, правда, оппозиция (особенно в среде т.н. "творческой интеллигенции") часто становится суперпозицией (в квантовом смысле, как одновременная реализация взаимоисключающих состояний). Ну, скажем, нормально - обкладывать х..ми "сраную рашку" и брать у государства деньги на своё "творчество".
-
 1
1
-
-
Так как доказать/опровергнуть то?) Точку одинаковости искать?
хз... Подумать надо

-
Откровенный плагиат из Маяковского. Нечто из моих ранних стихотворений, воспоминания о дефолте.
Почему "плагиат"? "По мотивам". Весьма достойно!

Может, кто-то вспомнит первоисточник Маяковского, использованный во фразе про депутатов?

"Я лучше в баре блядям буду подавать ананасную воду!"
© "Вам!"
-
Настоящая или из песка? Вот в чем вопрос!
P.S.: Нашел уже ответ, но писать не буду пока.
ИМХО - половина из песка, половина - настоящая.
-
Получается типа, что перекись служит для атомарного кислорода более активным "восстановителем" из всех присутствующих. Тогда почему сам оксид азота не может быть восстановителем перекиси или О*
А как он будет с атомарным кислородом?
NO + O ----> N + O2
Реакция, обратная стадии развития цепи:
N + O2 ----> NO + O
Если она и идёт, то в рамках того же цепного процесса, никак на него не влияя.
С перекисью NO может реагировать, образующийся NO2 будет разваливаться, и всё сведётся к некоему параллельному процессу разложения перекиси.
-
Ну, как-то так...
В этой концепции, конечно, полно слабых мест, но радикальные цепные реакции - это такая капризная вещь.
-
 1
1
-
-
А как такой вариант объяснения : если впрыскиваем перекись, то горение смещается в сторону с избытком окислителей ( например того же "атомарного кислорода" или вообще килорода ) - поэтому относительно иннертная NO может быстро перейти в более активную форму типа NO2, которая уже или распадается до азота и кислорода ( не нарушая наличия избытка окислителя ) или полнее окисляет топливо ( уровеньизбытка кислорода уменьшается).
Проверить можно поиском "точки одинаковости" с перекисью по выбросам NOx, при увеличении содержания кислорода или воздуха в смеси.
NO2 всё равно раскисляется (разлагается) сначала до NO, так что у неё те же шансы восстановится (или разложиться) до азота, что и у NO.
А вот для образования NO надо разбить молекулу азота, а это под силу только весьма энергичному радикалу - атомарному кислороду. И самое важное, что процесс этот - цепной. А значит, при введении перекиси, мы можем наблюдать гашение атомарного кислорода (как я нарисовал), или "охлаждение" - переход в менее энергичные HO* и HOO*, что тоже скажется на длине цепи и выходе NO.
Это, конечно, сугубое ИМХО, но мне так ка-а-этся...

-
 3
3
-
-
так в вопросе нет существа, вот и веселится народ)))
Да и почему "не по существу"? Бычков, он что - не существо? Существо, и ещё какое! Глыба! Один такой! Одноглыба... Унопетра... Эйнштейн!

-
 1
1
-
-
а статьи почитать? ))
Дык - почитал.
Монометильные производные получаются или в условиях защиты амино-группы (сульфонирование), или через комплекс гость-хозяин, или через анилид лития при -60С.
О чём я и толкую: простым сливанием реагентов селективно прометилировать анилин в монометильный продукт не получаеццо. Иначе зачем бы такие заморочки?
-
Но ТНФ восстанавливается в другой интересный полупродукт:
А продукт - это DDNP?


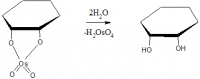
Наши стихотворения
в Курилка
Опубликовано
Вот оно что! Тогда надо было закавычить -
...
... вертолётов "ключ"
...
Оборот не стал бы яснее непосвящённому, но он перестал бы быть непонятной метафорой.