
Ан_Дм
-
Постов
158 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные Ан_Дм
-
-
3 часа назад, aversun сказал:
В соответствии с законодательством, мощность пневматики без лицензии не должна превосходить 7.5 дж. При налиции лицензии от 7.5 до 25 дж. Все остальное оружие не сертифицировано и является незаконным.
Наш магазин.
Купить можно даже 90 Дж, хотя вид мне не нравится, но купить можно.
http://mtbaltic.lt/priest-ii-cal-7-62-30-90j-pneumatinis-sautuvas.html?path=81_94
Есть и 60 Дж, подешевле.
-
2 минуты назад, yatcheh сказал:
Пульку модернизировать - высверлить нос
Есть такие.
 7 минут назад, yatcheh сказал:
7 минут назад, yatcheh сказал:вклеить кремень от зажигалки.
Где же столько кремния набрать?
-
17 минут назад, XemX64 сказал:
Если переборщите-пожалеете...
Вот поэтому пока и не тороплюсь.
Руки, ноги, пальцы .... не отрастают.
Хочется что-то ну очень тупое, чтобы срабатывало не по случаю, а исключительно при ОЧЕНЬ СИЛЬНОМ ударе, т.е. именно от пульки, а не при падении или случайном надавливании или как-то ещё.
-
2 часа назад, Митя сказал:
Детонация - эту уже за пределами правил форума. Но сразу вспоминается сигнал охотника. Может, по его патронам стрелять?
Дорогое удовольствие однако.
-
38 минут назад, XemX64 сказал:
Идиот детектед...
По людям пока не пробовал стрелять?Не? Странно. Обычно у таких "охотников" к этому всё сводится.Бросай это дело немедленно, ибо закончишь свой путь не там, где планировал...
Вообще-то воздушки у меня более 20 лет.
Первую купил ещё в 1996 году.
По людям и животным не стрелял и не имею желания, хотя на профильных форумах видел любителей пострелять ворон, даже счёт ведут. Не понимаю я таких людей.
Кстати, моя винтовка сосновую доску толщиной 35 мм. металлическим шариком пробивает навылет [пульки бывают разные, разного веса, формы, материала]. Толще доску не пробовал, небыло толще.
Т.е. убить с неё вполне реально, поэтому винтовка у меня под замком и я практически никому не даю стрелять, т.к. в случае чего и я несу ответственность.
Не люблю и оптику, с ней любой [ или почти любой ] дурак попадёт.
На мушку брать мишень куда интереснее.
Один грешок за мной всё же имеется - отстрелял прищепки на бельевой верёвке соседа. Было это лет 15 назад или около того.
Он понял, что моих рук дело и обиделся.
Вину я загладил, в том числе покупкой новых прищепок в количестве как минимум в 2 раза большем, чем расстрелял.
В общем всё закончилось благополучно, посиделками в беседке при красивом розовом закате..
Больше по чужому имуществу не стрелял, а только исключительно по своим различным мишеням, в том числе и пробкам.
Теперь вот хочу зрелищные мишени сделать и только.
За заботу спасибо.
Не судите всех одинаково.
-
19 минут назад, aversun сказал:
В соответствии с законодательством, мощность пневматики без лицензии не должна превосходить 7.5 дж. При налиции лицензии от 7.5 до 25 дж. Все остальное оружие не сертифицировано и является незаконным.
Это вероятно для России.
Я живу в Литве.
У нас до 7,5 Дж тоже можно без лицензии.
Лицензии есть 2 видов
1, Постоянная, выдаётся один раз и навсегда, если конечно не будет изъята за нарушения.
Позволяет приобретать и иметь газовые пистолеты, воздушки любой мощности и мелкокалиберное оружие.
2, Ограниченная по Времени [ на 5 лет ] для приобретения, хранения и пользования охотничьими ружьями и какими-то там ещё. Каждые 5 лет лицензию надо продлевать, проходя психолога и т.д.
,Я не охотник и мне хватает первого вида, поэтому оружие у меня легальное.
А вот луки и арбалеты у нас запрещены.
Чтобы их иметь нужно быть членом какого-то стрелкового клуба и прочие заморочки, а я себе арбалет купил бы.
-
Всем привет.
Имею дома пневматическую винтовку GAMO и частенько постреливаю в саду.
Винтовка мощная, 45 Джоулей, по паспорту скорость пули 470 м/с [ у мелкашки 510 - 530 м/с ].
На ютубе есть ролики охоты с такими винтовками, но у нас охота запрещена, поэтому развлекаюсь дома.
Честно говоря бумажные мишени как-то быстро надоели, поэтому стал стрелять по пробкам, в том числе и круглым пластмассовым от соков и бутылок Кока-Колы.
С пробками интереснее.
Пулька попав в пробку пробивает сквозное отверстие и при этом даёт ускорение пробке, которая иногда летит со свистом. Свист создаёт это самое отверстие в пробке.
Но и пробки стали надоедать.
Подумалось о чем-то пиротехническом, чтобы пулька, попав в мишень вызывала бы детонацию [ скорость пульки приличная, поэтому удар будет ощутимым ].
Больше интересует направление в сторону светового, а не шумового эффекта, не хочется пугать и нервировать соседей, к тому же в планах приобретение оптики ночного видения, что позволит стрелять в темноте, т.е. световой эффект будет проявляться очень эффективно. Попадание - яркая вспышка.
Готовую смесь думаю паковать или кубиками, или в те же пробки.
Что можете посоветовать?
В своём детстве мы делали взрывпакеты на основе алюминия и марганцовки, но их надо было поджигать, а здесь нужно срабатывание от удара, вот я весь в раздумьях, из чего сделать детонирующий фейверк.
Надеюсь на Ваши советы.
Спасибо.
-
15 часов назад, aversun сказал:
Суть катализаторов в том, что они ничего не отдают и не связывают. Они просто ускоряют реакцию, которая без их участия идет очень медленно. Сам катализатор в процесса реакции не изменяется.
Ну прямо вечный двигатель какой-то.
Делает работу и при этом сам не изменяется и не расходуется.
Если это катализатор, то почему от его количества сильно зависит свойство готового материала?
Ведь он, катализатор, должен работать постоянно, т.к. не расходуется и не вступает в реакцию..
Если кислоты мало, то пена не застынет.
Если много, то становится очень хрупкой, причём практически мгновенно.
Я смею всё же предположить, что там идёт реакция. вот только какая?
Что и как соединяется?
-
26 минут назад, Андрей Воробей сказал:
Фосфорная кислота вам "вредная". А озон, типа, сильно полезный...

Нет.
И всё же.
Если кислота катализатор, то как она работает со смолой?
Что-то отдаёт или как-то там связывает?
Как это работает, может кто-нибудь объяснить?
Спасибо.
-
Прочитал про формальдегид.
Та ещё гадость оказывается.
И ведь он нас окружает сплошь и рядом!
И как теперь с этим Жить???
Собирался идти спать и теперь точно не усну.
Кстати, а почему его тогда выпускают и делают из него предметы повседневнего обихода - мебель и т.п. и даже игрушки?
-
1 час назад, argon40 сказал:
"Опасность кислоты" на фоне мерзкой вонищи формальдегида это как вошь против танка.
Купился на дешевизну? А ты эту мерзость нюхал? Хоть в жидком, хоть отверждённом виде идёт мощная эмиссия формальдегида.
Едва уловимый запах формальдегида - это уже 700 ПДК.
А там не "едва уловимый" а слезоточивый. Даже у просушенного продукта.
Я поработал несколько дней на производстве этого "пенопласта мипора" , отлично знаю о чём говорю.
Спасибо.
Есть над чем подумать.
Как-то не вникал
.
ещё один момент.
Смолу нельзя держатьоткрытой на воздухе. т.к. она схватывается.
Подозреваю, что это влияние кислорода.
А если её вспенить не подачей кислоты, а озоном?
Озон будет работать как катализатор для смолы или нет?
-
1 час назад, yatcheh сказал:
Кислота тут - катализатор
А что ещё может быть катализатором для смолы?
-
Приветствую заглянувших в мою тему.
В современном строительстве в качестве утеплителя широко используется kaрбaмиднo-фoрмaльдегиднaя смoлa, формула которой представлена ниже.

Эта смола представляет из себя густую, жидкую субстанцию, которая без проблем разбавляется обычной водой.
В качестве отвердителя смолы используются практически любые кислоты, но в основном ортофосфорная H3PO4.
Технология получения аналога пенопласта проста.
В смолу добавляют воду и вводят вспениватель, чтобы порлучить пену при взбивании смолы.
Затем в пистолет подают смолу и разбавленную в воде кислоту.
В пистолете происходит взбивание этой смеси, в итоге кислота смешивается со смолой и при этом происходит вспенивание.
Т.е. на выходе получается пена, которую и заливают.
Далее происходит отверждение.
Технология проста и я хочу её попробовать для утепления своего дома.
Вот только меня напрягает использование кислоты. Опасная это вещь и хочется как можно реже с ней встречаться, тем более в быту.
Вопрос собственно в том, за счёт чего происходит отверждение смолы?
За счёт её окисления или какой-то иной реакции?
Если за счёт окисления, то можно ли отказаться от кислоты и использовать иные, менее агрессивные окислители?
Погуглил в интернете и нашёл не агрессивные окислители как например из доступных - перманганат калия - калиевая соль марганцовой кислоты. Химическая формула — KMnO4.
В общем вопрос заключается в замене кислот, как опасных и агрессивных на что-то менее агрессивное.
Допускаю, что возможно, что кислоты используют как самые дешёвые компоненты, что снижает затраты при коммерческом использовании, но мне не для комерции, а своих нужд, для утепления дома и я готов заплатить и больше, тем более, что мне много не надо. Главное - безопасность при работах.
Спасибо.
-
9 часов назад, mirs сказал:
Я бы взял серную кислоту.
У меня дома две полные 25 - ти литровые канистры с кислотами.
В одной ортофосфорная кислота, а в другой муравьиная.
Использовал кислоты когда утеплял сарай и гараж.
В общем осталась.
Жаль, что для этого дела их нельзя использовать.
-
Хорошо, вопрос поставлю иначе.
У нас есть гашённая известь - Гидрокси́д ка́льция (Ca(OH)2
Есть квасцы, например Сульфа́т алюми́ния-аммо́ния — NH4Al(SO4)2,
Эти 2 компонента смешиваютсяи к ним добавляется третий компонент, не из алхимии и т.л., т.е. конкретный, химический, который преврашает всё это хозяйство в крепкий монолит.
С точки зрения химии, что посоветуете попробовать?
Спасибо.
-
36 минут назад, Вадим Вергун сказал:
Думаю прокатит любой белок способный к уплотнению при денатурации. Например куриное яйцо.
Спрашивая о замене, я имел ввиду компонент, имеющий конкретную формулу., т.е.:
Яйца лучше употреблять по прямому назначению.
-
Всем привет.
Изучаю составы цементов.
Нашёл один из них, к моему удивлению широко используемый до сих пор, это китайский цемент Чио-Лиао.
Его состав.
ЦитатаКакая кровь свиньи?
Неужели на дворе не 21 век?
Чем в этом рецепте можно заменить эту самую кровь свиньи?
Или наука до сих пор бессильна?
Спасибо.
-
Здравствуйте.
Вычитал в одном рецепте, что применяется едкая известь.
Решил узнать,что же это такое.
Гуглю.
Энциклопедический словарь пишет:
ЦитатаЕдкая известь
то же, что гашеная известь
Справочник химика 21 пишет:
ЦитатаОксид кальция (едкая известь, жженая известь, негашеная известь)
Так гашённая или негашённая?
А ведь оба справочники!!!
-
У меня аквариум на 600 литров.
Там есть растения, которым нужен углекислый газ, иначе они начинают чахнуть.
Использовать баллон в доме не хочу, т.к. газ там под высоким давлением и если рванёт, то мало никому не покажется.
Есть варианты - брага ((дрожжи и сахар) или использованиеи кислоты.
Брага, это уже рукоблудие, а кислота опасна, т.к. её пары всё равно попадут в акву, сколько затворов не делай. Это уже пройденный этап.
Хочется что-то безопасное, например реакция с Озоном, который потом легче вывести, чем те же пары кислот.
Что можно растворить в воде, чтобы в последствии, пропуская через неё Озон, вызвать реакцию с выделением СО2?
Почему "давлю" на Озон?
Потому, что его легко получить.
При озонировании воздуха будут появляться и другие продукты, например окись Азота, но растениям она не страшна и многими даже усваивается.
Спасибо.
-
А как определяют, что он разложился?
Ведь так и рыбсов травануть можно.
11 час назад, Максим0 сказал:2NaOH+3O3+2H2O->2NaO(OH)2+3O2
Т.е. после всей реакции выделится лишь кислород?
Как называется 2NaO(OH)2, (или к какой группе относится), и что он из себя представляет в физическом плане?
Спасибо.
-
Я уже справшивал про соду и Озон.
Ясно, что газ с сухая сода не вступают в реакцию.
А если соду растворить в воде и озонировать воду?
И второй вопрос.
Озонирование воды используется при обработке воды, в том числе и аквариумной и питьевой.
Как из воды выводятся остатки Озона, ведь стабильное попадание его в организм ничего хорошего не сулит?
Спасибо.
-
Ещё вопрос.
Озон тяжелее воздуха, так как же озоновый слой держиться на высоте 10 - 15 Км, где значительное разряжение?
Ведь ввиду своей бОльшей плотности, он должен устремляться к поверхности Земли!!!?
На таких высотах и температуры низкие, а с понижением температуры газ сжимается, т.е. становится более плотным и его вес на единицу объёма увеличивается.
Т,е, Озон в плане объёма становится ещё более тяжёлым и тем более должен стремиться к поверхности планеты. -
Про опасность Озона я в курсе.
И ПДК знаю и Технику безопасности, т.к. работаю с высоковольтным оборудованием, а оно частенько прошивает.
Вопрос собственно потому и возник.
На счёт соды и озона понятно.
Спасибо.
Ещё один вопрос.
Озон хорошо растворяется в воде и некоторых жидкостях.
Основная масса эпоксидок в качестве отвердителя использует кислоты.
Застынет ли эпоксидка в среде Озона, ну или хотя бы образуется на её поверхности, контактирующей с Озоном, твёрдая корка?
Спасибо.
-
Приветствую заглянувших в мою тему.
Хочу просветиться по Озону и прояснить некоторые теоретические и практические вопросы.
Как всегда, для удобства, вопросы пронумерую.
1. Кислород поддерживает горенипе, это известно всем.
А как на счёт Озона?
Если да, то есть ли разница в эффективности скажем так?
Вопрос навеян отопительным котлом в доме.
Когда обогреваю дом, то через поддувало регулирую подачу воздуха и тут подумалось, а если подаваемый в печь воздух пропустить через озонатор?
2, Озон окислитель.
Кислота тоже.
В аквариумистике, для поддержания растений, используется углекислый газ.
Его либо подают из баллона, либо генерируют химическим способом, например кислота + сода.
Баллон вещь довольно опасная, т.к. находится под давлением.
Использование кислоты тоже имеет свои минусы, т.к. её пары могут попасть в аквариум.
При этом Озон тоже используют в аквариумистике для обеззараживания воды.
И тут возникла мысль, а почему бы Озон не использовать в качестве одного из компонентов для получения углекислого газа?
Что тогда должно быть вторым компонентом, не опасным для рыб и при этом активно вступающим в реакцию с Озоном?
3. Наверное детский вопрос.
Почему сода + кислота дают бурную реакцию, а сода + Озон никакую?
Пока всё.
Спасибо.

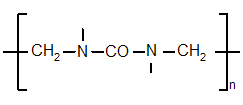
Рецепт клея для моделей
в Общий
Опубликовано
Я использую дихлорметан.
Ранее использовал дихлорэтан, но сейчас он для меня недоступен.