-
Постов
586 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные BauVictoria
-
-
Имеется методика приготовления состава эталонных растворов( расчет представлен для мерных колб вместимостью 50 мл):1).. 10^(-1)М- используют непосредственно рабочий раствор.
. .......... 2)....10^(-2)М- берут 5 мл рабочего стандартного раствора+5 мл фонового электролита и доводят объем до метки дист. Н2О
............. 3).... 10^(-3)М-берут 5 мл раствора 2) + 4,5 мл фонового электролита и доводят до метки дист. Н2О
И так далее, т.е один раствор готовят из другого. Соотношение объемов пробы и фонового электролита 10:1
Теперь сам вопрос: неясно как рассчитывают, сколько добавлять фонового электролита, особенно 3) случай.
3 случай: 10^(-2)*x мл =10^(-3)*50 мл. Это я рассчитала, что нужно взять 5 мл раствора 2), чтобы получить раствор с концентрацией 10^(-3). Далее в 3 растворе должно быть соотношение объемов пробы и фонового электролита 10:1. Но у меня уже в этих отобранных 5 мл раствора 2) фоновый электролит то есть, т.к при приготовлении 2) раствора его туда добавляли, как мне это учесть? Помогите, пожалуйста, запуталась: (
-
Можно ли оттитровать раствор тиосульфата натрия иодом в присутствии крахмала?
-
-
Для определения примеси алюминия в силикате магния 0,2 г сплавили с содой и после обработки кислотой довели объем раствора водой до 200 мл. Для приготовления колориметрируемого раствора аликвотную часть 20 мл после добавления алюминона довели до 50 мл. Оптические плотности этого раствора и раствора с добавкой 5 мл 5*10^(-4) М АlCl3 , измеренные относительно дистиллированной воды в кювете с толщиной слоя 2 см, были равны соответственно 0,25 и 0,55. Рассчитать содержание Al(в %) в безводном силикате магния, если известно, что силикат содержит 5% воды.
Вопрос: с помощью метода добавки я уже рассчитала Cx(Al) в 200 мл пробы . Сx(Al)= 1,0417*10^(-7) моль/мл. Как мне рассчитать в безводном с учётом 5% воды?
-
3 часа назад, M_GM сказал:
"В аликвоте: Сx(Аl)=4,75*10^(-6)*50 /1=237,5*10^(-6) г/мл." - г/мл - грамм чего? Надо думать алюминия?
"Затем С(Al)=2C(Al2O3) " - это справедливо для молярной концентрации, но не для масс/объемной, не для г/мл
Один из вариантов пересчета:
Находим молярную концентрацию алюминия : С(Аl)=Сx(Аl)/M(Al)=237,5/27*10^(-6) = 8,80*10^(-6) моль/мл
Пересчитываем на молярную концентрацию Al2O3 : С(Al2O3)=С(Аl)/2=4,40*10^(-6) моль/мл
И на его масс/объемную, концентрацию Al2O3: Сх(Al2O3)=С(Al2O3)*M(Al2O3)=4,40*10^(-6)*102 = 448,8*10^(-6) г/мл
далее m(Al2O3)=448,8*10^(-6)*100=0,04488 г, потом w(Al2O3)=(0,04488/0,1)*100%=44,88%
Все ясно!! Благодарю за помощь!
-
Вопрос: я нашла концентрацию по градуировочному графику С(Al)=4,75*10^(-6) г/мл. Это получается в 50 мл. Правильно ли я делаю перерасчёт, потому что с ответом у меня не сходится?
В аликвоте: Сx(Аl)=4,75*10^(-6)*50 /1=237,5*10^(-6) г/мл. Такая же концентрация и в 100 мл пробы. Затем С(Al)=2C(Al2O3) , отсюда Сx(Al2O3)=237,5*10^(-6)/2=118,75*10^(-6) ,далее m(Al2O3)=118,75*10^(-6)*100=0,011875 г, потом w(Al2O3)=(0,011875/0,1)*100%=11,875% .
Я правильно понимаю, что из градуировочного графика получаем концентрацию именно Аl? А не Al2O3?
-
Какой должен быть ход действий?
-
1 час назад, chemist-sib сказал:
А теперь мы плавно подошли к одному очень важному выводу: каждый шаг - даже если он осуществляется только на бумаге, мало-помалу увеличивает итоговую погрешность (метрологи бы поправили меня: неопределенность) всего определения. Попробуйте от полученной вами выше молярной (по хрому) концентрации раствора сравнения вновь перейти к его массо-объемной: 0,0385 х 51,996 = 2,00185 (г/л). Конечный результат у нас получается в третьем знаке после запятой. Согласны? А только на одной этой операции мы легко "швыряемся" этим третьим знаком... Общий подход здесь должен быть таков: все промежуточные операции выполняются с максимальной точностью (обычно - с числом значащих цифр на одну больше, чем должен получиться конечный результат); промежуточных округлений желательно избегать.
Вообще-то, в этой задаче много не очень красивого - с точки зрения метрологии химического анализа: очень разная точность исходных данных: титр раствора сравнения - одна значащая цифра (т.е., неопределенность его концентрации - где-то +/- 13%), в значении молярного коэффициента поглощения - то ли одна значащая цифра, то ли 4 (поскольку про однозначно определяющую это - запись величины в стандартном виде - составители задачи, видимо, не знают). Исходя из таких исходных неопределенностей, результат, получаемый с точностью 5-6 значащих цифр - это что-то слишком безрассудно смелое...
Хорошо, спасибо!!!

-
Помогите, пожалуйста
-
Для определения железа в концентрированной соляной кислоте используется реакция переведения его в фероин-иодид, экстрагируемый хллроформом. Хлороформный экстракт фотометрируют в кювете с l=1 см при длине волны 520 нм. Молярный коэффициент поглощения ферроин-иодида в хлороформе при длине волны 520 нм равен 1,15*10^4 л*моль(-1)*см(-1). Рассчитайте аликвоты концентрированной соляной кислоты (p=1,19 г/см3), необходимую для анализа, если: а) объем хлороформа для экстракции ферроин-иодида равен 10 мл б) оптимальный диапазон оптических плотностей, измеряемых спектрофотометром, составляет 0,1-1,7 в) массовая доля железа в соляной кислоте w,%= 1*10^(-5) . Ответ: Va,min= 40 мл, Va,max=700 мл. Есть некоторые наброски, но задача не выходит. Можете, пожалуйста, объяснить, как здесь нужно решать:)
-
2 часа назад, chemist-sib сказал:
Различие - лишь в количестве "шагов. У меня: расчет концентрации аналита в растворе сравнения в массо-объемных единицах; расчет "превышающей" молярной концентрации в исследуемой пробе; перевод последней в массо-объемные единицы; суммирование последних. Итого - 4 действия. У вас: расчет концентрации аналита в растворе сравнения в массо-объемных единицах; перевод ее в молярную концентрацию; расчет "превышающей" молярной концентрации в исследуемой пробе; суммирование последних; перевод суммарной молярной концентрации в массо-объемную. Итого - 5 действий. Я просто стараюсь избегать лишних телодвижений. Но, как во всяких всеобщих законах - все определяется начальной и конечной точками и не зависит от пути... Успехов в выборе - какой же из этих результатов является правильным.

Спасибо, но должны получатся одинаковые ответы. Даже если у меня шагов больше. А они почему-то разные. Может быть вы увидите ошибку в моем решении?
-
5 часов назад, chemist-sib сказал:
Итак, концентрация хрома в растворе сравнения: 0,004 х 25 / 50 = 0,002 (г/мл) = 2 мг/мл.
Превышение концентрации хрома в исследуемом растворе над концентрацией в растворе сравнения: 0,398 / (4000 х 5) = 1,99 х 10-5 (М/л).
Переводим молярную концентрацию хрома в массовую: 1,99 х 10-5 х 51,996 = 1,035 х 10-3 (г/л) или 1,035 х 10-3 (мг/мл).
Суммируем "фоновую" и "превышающую" концентрации: 2,00104 мг/мл.
(Может, наши калькуляторы в разных Китаях делали? Тогда - вполне возможно...).
Вообще у вас другое решение. После того как я нашла 2 г/л или 2 мг/мл по вашему решению, я эту концентрацию перевела в моль/л, а только потом подставляла в формулу. Так что у кого-то из нас ошибка в решении. По уравнению БЛБ нельзя рассчитывать в других единицах. Наверное поэтому не сходится.
-
В интернете и в учебнике нашла совершенно два разных описания дифференциального метода низкого поглощения. Первых два фото с учебника. Последнее с интернета. Вопрос вызывает концентрация раствора сравнения. В учебнике написано С2=0, а в интернете вообще концентрация раствора сравнения больше исследуемого. Проясните ситуацию, пожалуйста...

-
1 час назад, chemist-sib сказал:
Виктория, попробуйте еще раз пересчитать превышение концентрации над раствором сравнения - т.е., дробь 0,398/(4000х5). У меня упорно получается число, в два раза меньшее вашего. С учетом титра раствора сравнения - в итоге, 2,00104 мг/мл.
Хм, пересчитала, но по-прежнему все так. Где-то ошибка....
-
2 часа назад, chemist-sib сказал:
Чес-слово, разбираться в чужих формулах - это еще "то удовольствие". Давайте, я лучше вам "на пальцах", лады? Есть концентрация хрома в растворе сравнения. Концентрация его же, в исследуемом растворе, выше - поскольку есть дополнительная оптическая плотность. И есть молярный коэффициент поглощения (т.е., гипотетическая оптическая плотность раствор с концентрацией аналита 1 М в кювете с толщиной слоя 10 мм). По вот этой избыточной ОП, с учетом бОльшей толщины кюветы, по этому коэффициенту поглощения находите концентрацию аналита - молярную, переводите ее в массовую, суммируете с концентрацией в растворе сравнения и - фсе! Надеюсь, идею поймете, а уж с формулами - сами попробуйте...
Понятное дело, что удовольствия никакого, но на пальцах ничего не решается, к сожалению.Не знаю, я считала так, правильно ли или нет.Вроде аналогичная задача сошлась с таким же расчетом. А вот как вы объясняли я так и не поняла
И не совсем ясно, как понять, что в задаче использовали метод высокого, а не низкого поглощения. Формулы то разные
-
2 часа назад, chemist-sib сказал:
Правильно! И тот (раствор исследуемый) и другой (раствор сравнения) содержат один и тот же аналит, оба они окрашены - в разной степени. Прибор регистрирует разность степеней окрашивания - в этом и есть "дифференциальность" метода. И к той концентрации, что определяется по разности окраски, нужно добавлять ту, что содержится в растворе сравнения.
Тогда такой вопрос: как понять( в последней задаче) по какой формуле рассчитывать? Это метод высокого или низкого поглощения? Вот я рассчитала m(Cr)=T(Cr)*V=0,004 г/мл* 25 мл =0,1 г. С(Cr)=0,1г/50мл= 2 мг/мл это концентрация раствора сравнения. А дальше Aотн=el(Cx-Cсравн) или Аотн=еl(Cсравн-Сx)?
И еще: я нашла в книге, что в методе низкого поглощения концентрация раствора сравнения равна нулю( как в абсолютном способе измерения). А в интернете(фото ниже) вообще написано, что концентрация раствора сравнения больше концентрации исследуемого раствора... Что-то я теперь совсем не понимаю, что здесь происходит. Следующие две фотографии с учебника
Помогите, пожалуйста....
-
6 часов назад, chemist-sib сказал:
"Тупо" графиком можно пользоваться, если условия построения его и условия анализа исследуемой пробы - одинаковы. Здесь это присутствует ("...и при тех же условиях..."). Но, для объяснения несколько непривычного вида градуировочного графика, "игнорирующего" точку (0; 0) и уходящего "в минус" - надо бы понимать эту суть - фотометрирование не относительно "пустой" пробы, а относительно содержащей некое количество аналита. И, относительно ее, какие-то пробы тоже будут уходить в этот "минус". Такое вот приложение дифференциальной спектрофотометрии на практике. Теперь - угу?..
А, значит это задачка на дифференциальную спектрофотометрию, теперь понятно. А вот эта задача тоже на дифференциальную спектрофотометрию? : относительная оптическая плотность раствора комплекса хрома с дифенилкарбазидом равна 0,398 при длине поглощающего слоя 5 см. Рассчитать концентрацию хрома в мкг/мл,если раствор сравнения был приготовлен разбавлением 25 мл стандартного раствора хрома с титром T(Cr)=0,004 в колбе на 50 мл, а молярный коэффициент поглощения комплекса хрома равен 4000. Т. Е если в задаче у меня указана концентрация раствора сравнения, то это дифференциальный метод, я правильно понимаю?
-
Из навески стали массой 0,2542 г после соответствующей обработки получили 100 мл раствора, содержащего диметилглиоксимат никеля. Оптическую плотность этого раствора относительно раствора сравнения, содержащего 6 мг никеля в 100 мл равна 0,34. Для построения градуировочного графика взяли 3 стандартных раствора с содержанием 4,8,10 мг никеля в 100 мл и получили при тех же условиях относительные оптические плотности -0,240; 0,240; 0,460; w(Ni)-? Вопрос: зачем в задаче дано: 6 мг никеля в 100 мл? Вроде задача решается методом градуировочного графика и не ясно, где это использовать....
-
1 час назад, yatcheh сказал:
Да всё правильно. Соотношение то же самое, просто вы вложили другой смысл в значение n. Для соотношения
T1 = T^n
величина n = C1/C, Если С1 = 2*С (увеличение концентрации вдвое), то n = 2.
T1 = T^2
Если концентрация уменьшается в 10 раз, то С1 = 1/10*C, и n = 1/10 (а не 10):
T1 = T^(1/10)
При T = 0.367, значение T1 = 0.905
Всё верно

Благодарю за ответы!


-
2 часа назад, yatcheh сказал:
Сначала концентрацию увеличиваем вдвое, а потом, эту новую концентрацию - увеличиваем ещё вдвое.
Получается три значения коэфф. пропускания - 0.367 > 0.135 > 0.0182, соответствующие увеличению концентрации в 2 и ещё в 2 раза.
Все ясно! Кстати, у меня ещё есть задание, где концентрация уменьшается в 10 раз. Я посчитала так и у меня получилось, что связь T и Т1 другая ( выделено маркером). Посмотрите, пожалуйста, правильный расчет?
-
12 часов назад, yatcheh сказал:
Да. Тоже не срабатывает. Потеря знака. Величина Т всегда меньше единицы, логарифм(Т) всегда отрицательный. А -0.435 бОльше, чем -0.870. Деление одного на другое даёт отношение модулей. И тут хоть на пупе вертись - ничего не изменишь.
Ни отношение коэффициентов пропускания, ни отношение их логарифмов не имеет физического смысла.
Может кто-то другой что-нить умное скажет...

Меня осенило! Правило должно быть таким:
При увеличении концентрации в n раз оптическая плотность увеличивается в n раз.
При увеличении концентрации в n раз модуль логарифма коэффициента пропускания увеличивается в n раз.
Теперь ни что ни чему не противоречит

Да, вроде получается логично. Единственное, что меня ещё напрягает в расчете, так это строчка (на фото выделена). Первое, когда мы считаем при Т=0,367 вроде понятно, и результат получается как при увеличении концентрации вдвое, т.е T1=0,135. А вот когда берём Т=0,135 и получается Т=0,0182 это мы считаем просто при другой оптической плотности или при уменьшении концентрации вдвое?
-
18 часов назад, yatcheh сказал:
Ясно, тут вас подвело округление. Похожее на "e" число - чистая случайность.
T/T1 = 10^0.870/10^0.435 = 10^(0.870-0.435) = 10^0.435 = 2.723Отношение T/T1 при увеличении концентрации в n раз будет зависеть от исходной концентрации C:
T/T1 = 10^(elC1)/10^(elC) = 10^(el*(C1 - C))
если С1 = n*C, то
T/T1 = 10^(el*(n*C - C)) = 10^(elC*(n-1))
В правой части присутствует величина С.
После всех сокращений получитсяT1 = T^n
При Т = 0.367 Т1 = 0.367^2 = 0.135 тогда T/T1 = 2.718
При T = 0.135 T1 = 0.135^2 = 0.0182 и тогда T/T1 = 7.418
Никакого постоянного отношения T/T1 при n=2 нету. А вот отношение логарифмов при любом Т будет равно 1/n:lg(T)/lg(T1) = 1/n
lg(0.367)/lg(0.135) = 0.5005
lg(0.135)/lg(0.0182) = 0.4998
То есть:
При увеличении концентрации в n раз оптическая плотность увеличивается в n раз, а логарифм коэффициента пропускания уменьшается в n раз
У-ф-ф-ф... В трёх соснах заблудился, ей-богу

Вот блин, кажется пропускание меня дальше не пропустит... Что-то и я теперь снова в трех соснах заблудилась. Так если у нас lgT/lgT1=1/n, то для нашего случая изначально Т=0,367 и lg(0,367)=-0,435. Затем, когда увеличили концентрацию в 2 раза, T1=0,135 и lg(0,135)= -0,869. Получается, что логарифм при увеличении концентрации увеличивается в 2 раза : -0,435*2=-0,869. Или если так записать: lg(0,367)/lg(0,135)=0,5005=1/2, т.е lg(0,135)=2lg(0,367). Куда мозги зашли... Не, ей богу не понимаю. У меня выходит так
-
16 часов назад, yatcheh сказал:
Ясно, тут вас подвело округление. Похожее на "e" число - чистая случайность.
T/T1 = 10^0.870/10^0.435 = 10^(0.870-0.435) = 10^0.435 = 2.723Отношение T/T1 при увеличении концентрации в n раз будет зависеть от исходной концентрации C:
T/T1 = 10^(elC1)/10^(elC) = 10^(el*(C1 - C))
если С1 = n*C, то
T/T1 = 10^(el*(n*C - C)) = 10^(elC*(n-1))
В правой части присутствует величина С.
После всех сокращений получитсяT1 = T^n
При Т = 0.367 Т1 = 0.367^2 = 0.135 тогда T/T1 = 2.718
При T = 0.135 T1 = 0.135^2 = 0.0182 и тогда T/T1 = 7.418
Никакого постоянного отношения T/T1 при n=2 нету. А вот отношение логарифмов при любом Т будет равно 1/n:lg(T)/lg(T1) = 1/n
lg(0.367)/lg(0.135) = 0.5005
lg(0.135)/lg(0.0182) = 0.4998
То есть:
При увеличении концентрации в n раз оптическая плотность увеличивается в n раз, а логарифм коэффициента пропускания уменьшается в n раз
У-ф-ф-ф... В трёх соснах заблудился, ей-богу

Ухх... Теперь все ясно, а я уже обрадовалась, увидев значение экспоненты
 , Спасибо, что помогли разобраться!
, Спасибо, что помогли разобраться! 


-
48 минут назад, yatcheh сказал:
Да, я тут завис...
У меня по другому получается:
T = T0^(C/C0)
Kоэффициент пропускания при увеличении/уменьшении концентрации в n раз уменьшается/увеличивается в степени n.
То есть "во сколько раз" - не скажешь. Если концентрация в два раза увеличивается, то коэффициент пропускания будет равн квадрату исходного. Скажем, для 0.9 - 0.81, а для 0.1 - 0.01
Если в три раза - куб. Степень, короче. Степенная функция.
P.S. Честно говоря, с этим коэффициентом пропускания я изрядно затупил. Казалось бы... ан - нет

А как у вас экспонента получилась?
Взяла цифры с левой задачи, просто чтобы какие-то были. Посчитала следующим образом. Интересно, это случайность значение экспоненты или это всегда так будет выходить? Прилагаю расчёт
















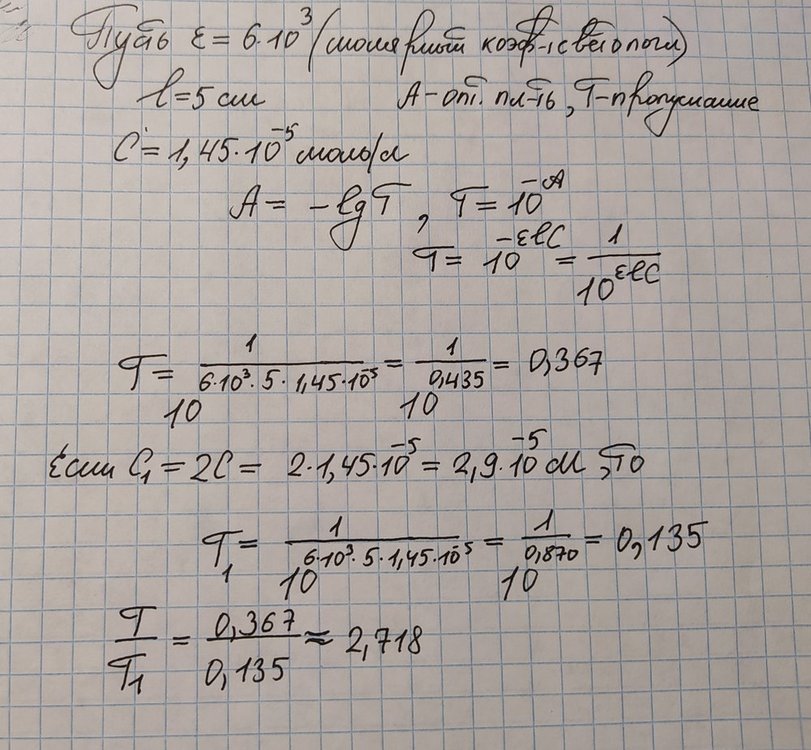
Приготовление растворов
в Решение заданий
Опубликовано
Благодарю, все понятно!