
SeaDoo
-
Постов
530 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные SeaDoo
-
-
25.12.2022 в 18:45, RET сказал:
Что-то не слышал чтоб сульфогруппа легко отщеплялась, какие-то единичные случаи могут быть, а просто так не отщепляется.
Не важно Na там или кислота. Фосфатная он может легче, поэтому сама уходит.
Нет, я имел ввиду, если в рибофлавине заменить фосфатную группу на сульфогруппу!!! (ну т.е. если фосфатная может отщепиться, на ее место сульфогруппа не встанет?)
-
24.12.2022 в 15:57, chemister2010 сказал:
Пишут, что можно получить свободную кислоту осторожным подкислением. В кислой среде отщепляется фосфатная группа. Как и у рибофлавина вещество боится света.
Ага, и как это на практике реализовать? Для "Желтый солнечный закат", по совету одного уважаемого форумчанина, делал рН 1, вроде получилось (сейчас как-раз уточняющие эксперименты провожу). Т.е. осторожное это сколько в цифрах или как еще определить, что уже все - натрий отцепился?
зы а то, что боится света - да это не важно... мне бы понять как ведет себя фосфатная группа...
А КСТАТИ, если уж фосфатнпая легко отщепляется, нельзя ли ее заменить на сульфогруппу???????????? ВОТ ЭТО БУДЕТ НОМЕР!!!
В форме кислоты, конечно!
-
22.12.2022 в 17:17, RET сказал:
Может и уксусная кислота прокатить, если хватит силы.
Можно фосфорную, но нафтолы обычно сульфированные so3Na (у меня такие есть), диазотируемый амин без солевой группы.
Будет проблема растворимости. И 'сульфировать' придется чистый нафталин или бензол фосфорной.
Концевые ch3 (хоть cf3) можно, поменяется цвет, и свойства.
"Может и уксусная кислота прокатить, если хватит силы." - Есть солянка.
"Будет проблема растворимости. " - ну у того-же Рибофлавина натриевой соли - фосфорная группа очень хорошую растворимость дает...
"Концевые ch3 (хоть cf3) можно, поменяется цвет, и свойства." - Вот именно на это и хотелось бы посмотреть!!!
-
21.12.2022 в 23:32, chemister2010 сказал:
1) Можно. Подкисляете сильной кислотой и получаете кислую форму.
2) Теоретически можно, но фосфоновые группы легче отваливаются, труднее получаются и будут иметь совсем другие свойства.
3) Тогда это будет не рибофлавин и вам надо будет доказывает его биологическую активность и проверять токсичность.
1) Ок, СПС. Значит можно по аналогии с кисллотной формой того-же "Желтый солнечный закат" (в смысле устойчива молекула в кислой среде). рН 1, нормально будет?
2) Было-бы очень интересно сравнить именно с сульфогруппами. (на счет отрыва я не сильно беспокоюсь - условия мягкие)
3) Не в контексте мед\пищ.
-
07.11.2022 в 00:45, Химические элементы сказал:
Искусственные алмазики...
Искусственные алмазики...
ммм, а почему желтые? примеси или дефекты решетки? А люминисценция у них есть? (уф или фиолетвыми диодами если светить?) И кстати, было бы не плохо, рядом алмазы, графит и сажу...
А вообще на счет компании - это КРУТО конечно!!!
-
разбавить до жидкого состояния...
затем осадить (есть же хим. коагулянты)
или высушить и далее уже выщелачивать и декантировать... (после высушивания обычно все укрупняется)
или отжечь!
-
Всем добра!
Собственно коммерчески доступный сабж (в виде пищевого красителя) существует в 2х формах E101 и E101II (т.н. "натриевая соль").
1) Нельзя-ли "отцепить" Na и перевезти в чисто кислотную форму? (по аналогии с некоторыми азокрасителями, которые существуют как форме натриевой соли, так и кислоты)?
2) Нельзя-ли при синтезе азокрасителей вместо сульфо группы (SO3H) подставить фосфорную? (PO3H2 наверно получиться, или все-таки PO3H ?) Если по конкретней "Желтый солнечный закат" (который есть сульфированный "Судан-I".
3) Нельзя-ли при синтезе Рибофлавина (конкретнее E101II) две КФГ (концевые функциональные группы) CH3, заменить на одну N(CH3)*2 по аналогии с "Метиленовам синим", к примеру? (в позиции [это важно] "нижней по рисунку" CH3 ?
-
-
хотелось бы стабильности параметров и это, как сказать, ну чтоб можно было в отчетике указать - сорбент такой-то, подвижность в-ва (Pt или как-ее там) такая-то... Да и толочь килограмм силикагеля, как-то нехоца...
-
Всем добра!
Вот дошел ход до препаративной очистки...
Где взять сорбент (наполнитель) для колонки? (самодельной)
23.07.2022 в 12:34, yatcheh сказал:В лохматые времена, когда таких приборов не было, делал я флаш на самодельной колонке 40*2.5 см. Заполнял обеспыленным силикагелем "5*40 нм". Давил азотом 1-1.5 атм. Нагрузка - 3-4 г вещества. Очищал фосфорорганику. Элюент - смесь ацетонитрила и гексана. Для Rf = 0.25 процесс занимал 4-5 часов.
фосфорорганику - "новичёк"? ?
-
17.12.2022 в 17:56, Никибосс сказал:
ИМХО не получиться... Я тоже когда-то пытался... растворение пульпы или ее многократная промывка (выщелачивание), декантирование (центрифугирование) и потом уже классический электролиз.
-
ну да, наверно гидрокарбонат там и будет (если не фосфат)
-
30.08.2022 в 12:54, Lеоnid сказал:
Так больше 10% или все же меньше? Знак неравенства не перепутали?
да да, меньше конечно, пардоньте плиз)))
30.08.2022 в 12:54, Lеоnid сказал:Сдуру можно и ... сломать, а позвольте осведомиться - зачем вообще туда стеклянный электрод помещать?
нууу... условия эксперимента: нейтрализовать 10% ортофосфорную кислоту КОН до такого-то рН...
-
и кстати да, еще вопрос: а может ли концентрированная (80-85%) ортофосфорная к-та повреждать хим.стекло? А при нагревании? А можно ее хранить в стеклянной бутылке (химическая бутылка из темно-зеленого стекла)?
-
Может ли ортофосфорная кислота повредить стеклянный электрод рН метра?
(слышал, что ортофосфорная кислота может повреждать стекло).
Кислота разбавленая > 10%, температура комнатная.
-
ВСЕМ СПАСИБО за обсуждения! пошел определять)
-
-
-
Всем добра!
Имеется некоторое кол-во в-ва, как определить фосфат меди или карбонат меди или их смесь?
-
23.07.2022 в 06:59, ruso16 сказал:
Мензурок как навоза. Есть и без носика.
А еще есть китайские вазы. Стаканы. Высокие с тонким дном. Литров до 10 видел. У вас Китай ближе.
ну это понятно, хотелось бы лаборатоного класса...
хотя если помните где видели "Высокие с тонким дном. Литров до 10 видел. " - подскажите.
-
нет-нет, Вы не поняли, есть такие приборчики - которые хроматографически чистят В-во под давлением... используются даже для БАДов...
все автоматизированно - нажал на кнопочку - получил результ...
мне надо грубо говоря из 85% красителя, получить максимально близкий к 100%. (на сколько это возможно). городить 6и метровую колонну с мизерным КПД (даже по времени) ну как-бы не хочется... флэш-хоматография работает быстро, за счет давления, но крайне-миниатюрная по длинне колонка смущает (качество разделения). Да, и подвижность молекулы красителя и полупродуктов и темболее соли, имхо кардинально различаются, поэтому я думаю состав не так уж важен... (а индусы на контакт идут крайне плохо, и MSD выпросить у них, как у жадины снега зимой...)
я имел ввиду вот примерно такие приборы
-
Всем добра!
Нужны цилиндрические тонкостенные стеклянные сосуды, по типу химического стакана В-2, (высокие, тонкостенные, без носика, без верхней "юбочки").
Для кристаллизатора. Весь инет перерыл, кроме вазы для цветов - нечего нет, но вопервых это ваза, а не лаб.посуда, а во вторых там как правило дно толстое - а это плохо...
Как они правильно называются и где их взять?
-
Всем добра!
Когда-то давным-давно мой учитель, разделял нитроанилины хроматографической колонкой высотой 6 метров (!).
Сейчас я понимаю с этим с легкостью может справиться Флэш-хроматография? Или нет? А "D" и "L" изомеры может разделить (например глюкозы)?
Но это чисто теоритический вопрос... А на практике можно ли "почистить" органический краситель (допустим "желтый солнечно-закатный" - водорастворимый. Имеется квалификации "тех". Фирма производитель заявляет о концентрации >85%. Что входит в остальные 15% - пояснить не могут. (фирма индийская, на контакт идет тяжело) в "остатках" могут быть как полупродукты синтеза, так и соли - хлориды и\или фосфаты)
Количество - от нескольких, до нескольких десятков грамм.
ЗЫ поиск в интернете не дает особых результатов (ну чтоб студенту почитать на досуге)
-
провел опыт: разбавленную солянку нейтрализовал избытком КОН - на глаз без цветная прозрачная...
провел тестовый опыт: в воду на полоске фильтровальной бумаги ввел хлорное железо, до еле-заметного желтого окрашевания, прилил КОН - нечего не произошло!!!
в воду капнул хлорное железо, 1 каплю (с полоски фильтровальной бумаги) - до заметного окрашивания, прилил КОН - сразу выпал красно-бурый осадок.
вывод: реакция не очень чуствительная...
все опыты проводились в 100мл хим стакане, с дис.водой. КОН - "ХЧ"
попробую с роданидом...

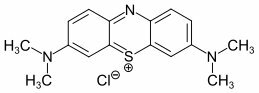



Рибофлавин, парочка вопросов.
в Органическая химия
Опубликовано
Ок, так значит нужно в процессе синтеза присоединять вместо фосфатной сульфо (а не в готовом веществе менять) так?