
ВНС
-
Постов
626 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные ВНС
-
-
СH3-CH2-CHBr-COOH --(NH3, -NH4Br)--> СH3-CH2-CHNH2-COOH

Два дипептида:
NH2-CH(C2H5)-CO-NH-CH(C3H7)-COOH
NH2-CH(C3H7)-CO-NH-CH(C2H5)-COOH
Можно проще:
C3H7OH + PCl5 ----> C3H7Cl + POCl3 + HCl
C3H7Cl + Mg ----> C3H7—Mg—Cl
C3H7—Mg—Cl + CO2 ----> C3H7-COOMgCl --(HCl, -MgCl2)--> C3H7-COOH
Или ещё проще:
C3H7OH + PCl5 ----> C3H7Cl + POCl3 + HCl
C3H7Cl + NaCN ----> C3H7-CN --(H2O, H+, -NH4+)--> C3H7C-COOH
Видимо, С5Н12?
CH3-C(CH3)2-CH3 (2,2-диметилпропан , или неопентан)
(СH3)4C --(Br2, hv, -HBr)--> (CH3)3C-CH2Br (1-бром-2,2-диметилпропан, или неопентилбромид)
Большое спасибо
-
В задании не очень понятно какие нужно написать дипептиды?
Здесь можно дать формулы любых дипептидов??
-
Требуется рассмотреть строение молекул H2Se; ICl3; TeCl2 с позиции метода валентных связей, 1) указать квантовые состояния валентных электронов в атомах, образующих связи в молекулах; 2) форму и валентные углы между связями; 3) нарисовать модели и определить полярны или неполярны молекулы. Задание 1 я,вроде нашел, а вот 2 и 3 никак точно не могу сформулировать ответ Помогите, пожалуйста
Кто может дать ссылку на хороший учебник?
-
Каким образом из α-броммасляной кислоты можно получить α-аминомасляную кислоту? Примените проекционную формулу полученной кислоты, чтобы показать асимметричный атом углерода в ней. Напишите формулы возможных дипептидов, в молекулах которых содержатся по одному остатку α-аминомасляной и α-амино-валериановой кислот.
Помогите, пожалуйста, с этим заданием
И еще одна реакция(или не одна?) Как из пропилового спирта получить масляную кислоту??
Здесь что-то нашел ,правильно или нет не знаю
C3H7OH + PCl5 C3H7Cl + POCl3 + HCl
C3H7Cl + Mg C3H7—Mg—Cl
C3H7—Mg—Cl + CH2O + H2O СН3—(СН2)2 –СH2ОН + MgOHBr
СН3—(СН2)2 –СH2ОН + 2O СН3—(СН2)2 –СООН + H2O
В задании не очень понятно какие нужно написать дипептиды?
-
Требуется рассмотреть строение молекул H2Se; ICl3; TeCl2 с позиции метода валентных связей, 1) указать квантовые состояния валентных электронов в атомах, образующих связи в молекулах; 2) форму и валентные углы между связями; 3) нарисовать модели и определить полярны или неполярны молекулы. Задание 1 я,вроде нашел, а вот 2 и 3 никак точно не могу сформулировать ответ Помогите, пожалуйста
-
Каким образом из α-броммасляной кислоты можно получить α-аминомасляную кислоту? Примените проекционную формулу полученной кислоты, чтобы показать асимметричный атом углерода в ней. Напишите формулы возможных дипептидов, в молекулах которых содержатся по одному остатку α-аминомасляной и α-амино-валериановой кислот.
Помогите, пожалуйста, с этим заданием
И еще одна реакция(или не одна?) Как из пропилового спирта получить масляную кислоту??
Здесь что-то нашел ,правильно или нет не знаю
C3H7OH + PCl5 C3H7Cl + POCl3 + HCl
C3H7Cl + Mg C3H7—Mg—Cl
C3H7—Mg—Cl + CH2O + H2O СН3—(СН2)2 –СH2ОН + MgOHBr
СН3—(СН2)2 –СH2ОН + 2O СН3—(СН2)2 –СООН + H2O
-
При прокаливании 1,56 г смеси карбоната цин¬ка с оксидом цинка получили 1,34 г оксида цинка. Вы¬числить состав исходной смеси (в процентах по массе).
будьте добры, помогите))
1,56 - 1,34 = 0,22г это масса выделившегося СО2
0,22г СО2 соответствуют Х г ZnCO3
44г 125г
mZnCO3 = 125*0,22\44 = 0,625г
W%ZnCO3 = 0,625\1,56 *100% = 40,064%
W%ZnO = 100 - 40,064 = 59,936%
Извините, когда писал свой ответ,не видел Ваших ответов(для plick и Filgor)
-
Вполне правдоподобная величина.
Спасибо огромное за помощь
-
Осталась последняя задача, подскажите, пожалуйста формулы, и еще - здесь данных хватает для решения или нет?
Кто-нибудь сможет помочь с решением?
-
Это означает, что катодом будет все-таки х.с.э.
Тогда,
0,358 = 0,163 - ЕН2, откуда ЕН2 = - 0,195 В.
рН = - 0,195 / (- 0,059) =
Там не 0,163, а 0,281 - я пересчитал по Вашей формуле
Ест = 0,281 - 0,358 = -0,077В
рН = - (-0,077\0,059) = 1,3
Так?
-
Для металлов одна формула, для х.с.э. - другая. В ней учитывается концентрация восстановленной формы - знак обращается.
Считайте, что равна.
А отчего Вы так уверены, что х.с.э. - именно катод?
Понял, тогда Е = 0,222 - 0,059lg[KCl] = 0,222 + 0,059 = 0,281В
Тогда Ест = Ех.с.е + ЭДС = 0,281 + 0,358 = 0,639В
Ест = Е + 0,059lg[HCl]
lg[HCl] = Ecт\0,059 = 0,639\0,059 = 10,83
рН = -lg[H+] = -10,83
Только тогда рН получается с минусом да и величина большая Опять где-то не так?
-
Верное.
E = Eo - 0,059lgaCl-
ЭДС по определению положительная величина.
А откуда эта формула E = Eo - 0,059lgaCl- Я всегда решал например для металлов E = Eo + 0,059lg[Me+]
Активность Cl- не равна концентрации KCl??
И еще: ЭДС у меня положительна, просто чтобы найти Еанода нужно Екатода - ЭДС
В общем я теперь запутался в решении
-
Я нашел для электрода Cl-\AgCl\Ag потенциал равен +0.222 , сомневаюсь верное значение или нет
Чтобы найти потенциал электрода нужно Е = 0,222 + 0,059lg[KCl] = 0,222 - 0,059 = 0,163В
Тогда Ест = Е - ЭДС = 0,163 - 0,358 = -0,195
Здесь все верно?
Дальше будет Ест = Е + 0,059lg[HCl]
lg[HCl] = Ecт\0,059 = -0,195\0,059 = - 3,3
рН = -lg[H+] = 3,3
Похоже на правду но правильно решено или нет - не знаю???
Проверьте, пожалуйста, решение
-
для реакции CO + Cl2 = COCl2 даны mисх(Cl2)= 11,5г, mпрод = 13,826г Чере реактор пропускается электромагнитное излучение с длиной волны λ = 380 нм и энергией Е = 82,6 Дж Измерения показали, что энергия Е1 = 34 Дж Рассчитайте квантовый выход реакции и сделайте вывод о механизме протекания фотометрической реакции
Помогите, пожалуйста, с решением
Осталась последняя задача, подскажите, пожалуйста формулы, и еще - здесь данных хватает для решения или нет?
-
По справочнику определите потенциал х.с.э. в 0,1 н. KCl.
Установив его потенциал, через ЭДС определите потенциал водородного электрода, EH2
pH = - 0,059EH2
Я нашел для электрода Cl-\AgCl\Ag потенциал равен +0.222 , сомневаюсь верное значение или нет
Чтобы найти потенциал электрода нужно Е = 0,222 + 0,059lg[KCl] = 0,222 - 0,059 = 0,163В
Тогда Ест = Е - ЭДС = 0,163 - 0,358 = -0,195
Здесь все верно?
Дальше будет Ест = Е + 0,059lg[HCl]
lg[HCl] = Ecт\0,059 = -0,195\0,059 = - 3,3
рН = -lg[H+] = 3,3
Похоже на правду но правильно решено или нет - не знаю???
-
По какой формуле решается задача?
Здесь нужны какие-нибудь табличные значения?
-
Элемент состоит из стандартного электрода,находящегося в растворе электролита HCl и хлорсеребряного электрода с концентрацией KCl 0,1н Вычислить рН раствора, содержащего электролит, если ЭДС = 0,358В
Подскажите ход решения, пожалуйста
-
для реакции CO + Cl2 = COCl2 даны mисх(Cl2)= 11,5г, mпрод = 13,826г Чере реактор пропускается электромагнитное излучение с длиной волны λ = 380 нм и энергией Е = 82,6 Дж Измерения показали, что энергия Е1 = 34 Дж Рассчитайте квантовый выход реакции и сделайте вывод о механизме протекания фотометрической реакции
Помогите, пожалуйста, с решением
По какой формуле решается задача?
-
для реакции CO + Cl2 = COCl2 даны mисх(Cl2)= 11,5г, mпрод = 13,826г Чере реактор пропускается электромагнитное излучение с длиной волны λ = 380 нм и энергией Е = 82,6 Дж Измерения показали, что энергия Е1 = 34 Дж Рассчитайте квантовый выход реакции и сделайте вывод о механизме протекания фотометрической реакции
Помогите, пожалуйста, с решением
-
Действительно, не глянул в книжку, понадеявшись на память, а старушка подвела. Тогда за основу можно принять предложение Ivan96. Но и в этом случае для определения достаточно двух образцов. Кислоту лучше взять концентрированную соляную - в ней растворение идёт намного быстрее.
Огромное спасибо всем!
-
-
-
Спасибо Вам за помощь
-
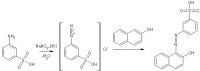
На м-сульфанилин подействуйте азотистой кислотой в присутствии разбавленной серной кислоты при температуре 0 °С, на полученный продукт – β-нафтолом. Напишите уравнения реакций. К какому классу соединений относят конечное вещество? Какое практическое значение имеют соединения этого класса? Дайте примеры
Помогите, пожалуйста с этим заданием

Метод валентных связей
в Решение заданий
Опубликовано
Нигде не могу найти 100% ответов. Помогите, кто знает . А как правильно рисовать молекулы?