-
Постов
3565 -
Зарегистрирован
-
Посещение
-
Победитель дней
1
Тип контента
Профили
Форумы
События
Сообщения, опубликованные qerik
-
-
После того как поработал с кобальтом, слегка тошнило, но руки я мыл, может совпадение))
Если прошло больше суток, то уже в принципе ничего страшного не должно случиться.
Чтобы сильно отравиться, надо около 10грамм проглотить.
-
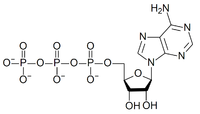
Химическое строение,биологическая роль и локализация в растительной клетке АТФ и АДР.
АДР - это что такое за зверь?
АТФ:

Основной источник энергии, содержит в себе 3 макроэргических связи, каждая по 40кДж. Синтезируются в растительных клетках в ходе фотосинтеза (небольшое кол-во) и в ходе окисления органических веществ. Являются универсальным источником энергии, поэтому распространяются по всей клетке.
-

проп-1енол-1
-
1. Купите копеешный CaCl2.
4. Фторопласт.
1. Задумаюсь над этим.
4. Куплю пару метров в ближайшее время.
В ходе эксперимента - почему бы и нет?
Но все же лучше будет добавлять воду, т.к. кислоты летит меньше, чем пара.
Решил обвязать проволокой колбу, дабы осколки не разлетались, если таки взорвется, и пробка не вылетала.
В местах соприкосновения проволоки с колбой не будет повышенной вероятности возникновения трещин вследствие неравномерного теплового распределения?
-
Нет. Буквенные локанты вообще не рекомендуются к использованию. Допускаются только в составе полутривиальных названий.
Хм. Хорошо.
А в данном случае, если бы был не 1-бромпропен-1ил, а, например, 1-бромоктен-1ил, то он бы имел приоритет перед амино-группой? Или от длины углеродной цепи радикала приоритет не меняется, а имеет значение только положение радикала по отношению к главной группе?
-
Осознал. 1 и 2е название равнозначны по ИЮПАК?
Где не искал старшинство радикалов - везде отписываются общими словами, есть какая-нибудь таблица по этому поводу?
п-α-бромпроп-α-енил о-гидроксианилин может быть такое название?
-
Хм, попробую дать название.
Возможно 1-гидроксо3-(1-бромпропен)анилин
или так: 1-(1-бромпропен)2-гидроксо3-аминобензол
или так: п-1-бромпропен о-гидроскоанилин
-
-
Например, пропанол-2 в пропанол-1 или же бутанол-2 в бутанол-1.
для пропанола:
дегидратация, присоединения бромоводорода в присутствии перекиси, добавление водного раствора KOH.
для бутанола, возможно, не подойдёт.
-
-
простите,не понял,вот это:
ΔM (нагревания) = 16. X+Y+Z = 0.6
можете объяснить?
Схематически можно изобразить так:
Me +1/2O2 = MeO
молярная масса смеси увеличилась на 16
9.6/16 = ?
-
X- n(Zn)
Y- n(Mg)
Z - n(Cu)
Zn + 2HCl = ZnCl2 + H2
Mg + 2HCl = MgCl2 + H2
2Cu + O2 = 2CuO
2Zn + O2 = 2ZnO
2Mg + O2 = 2MgO
ΔM (нагревания) = 16. X+Y+Z = 0.6
X+Y = 0.35 (из реакции с кислотой).
n(Cu) = 0.25
n(KOH) = 0.4
ZnO + 2 KOH + 2H2O = K2[Zn(OH)4]
n(Zn) = 0.2
а дальше все просто.
-
Из C2H5Br и CH3CH2CH2OH получить диэтиловый эфир
1. + KOH (H2O);
+H2SO4(к)
2. Если из пропанола - дегидратация, гидрирование, крекинг (можно ли это применить к пропану?), гидратация, +H2SO4(к).
-
1) Геттер? Это что бы кислород совсем не поступал? Нужен осушитель - силикагель подойдет.
2) В кислороде расплавленная сера наверняка загорится и весьма интенсивно. Я видел, как горит сера в кислороде, яркое пламя и очень высокая температура.
3) лучше пропитать насыщенным раствором ванадата аммония достаточно пористую пемзу и прокалить.
1. Силикагель было решено получать электролизом и дальнейшим прокаливанием из разведенного жидкого стекла, ибо кислоты катастрофически не хватает.
Будут какие-нибудь рекомендации по прокаливанию или там невозможно перегреть?
2. Для этого можно регулировать поток воздуха реостатом, также для того, чтобы пробка совсем не вылетела, планирую обвязать стальной цепью с длиной звеньев ~ 3-4мм. Не представляю, как предотвратить обратный ход олеума, давление внутри будет ой какое немаленькое, разве что делать батарею из 5-7 вентиляторов последовательно. Вентиляторы 8см компьютерные 12В, воздушный поток от 1 примерно 25 CFM. Трубку большей толщины вряд ли смогу найти, на выдув вентилятор тоже не поставишь - кислота металл мигом съест. Так что вопрос остается открытым.
3. По поводу ванадата аммония - уже нашел грамм 40, пемзу раскрошу до кусков 1-2мм в диаметре и буду помешивать в растворе периодически, потом ещё с ванадатом засыплю в трубку и согну её так, чтобы ванадат не высыпался, когда он будет там надежно лежать, прокалю над огнем. Имеет шанс на жизнь такой вариант?
4. По поводу резины: какие марки выдержат горячую концентрированную серную кислоту?
МС (маслостойкая) тут явно не подойдёт.
-
1) Кислород должен поступать сухой.
2) Пары серы в токе кислорода начнут гореть. Расширяющиеся газы выбьют пробку в колбе с серой.
3) Нужно регулировать поток SO2 (не слишком сильный), иначе к SO3 будет примесь SO2. Или делать катализатор с достаточно развитой поверхностью.
4) Трубку из которой пойдет SO3 нельзя опускать прямо в раствор серной кислоты. При колебаниях температуры велика вероятность, что может этот раствор перебросить в колбу с серой и в то место где будет катализатор.
1. Значит нужен геттер. Силикагель или барий с натрием подойдут?
2. Что нужно сделать, чтобы этого не допустить? Держать температуру строго 120 +- 5? Или есть более хитрый способ.
3. Поток можно регулировать температурой или краном (только какой кран олеум выдержит?). Катализатор думаю сделать в изгибе стеклянной трубки, туда насыпать порошок оксида ванадия и запечь со стеклом при нагревании, а потом ещё немного добавить на случай, если стекло закроет порошок.
4. Планирую трубку с дистиллятом и газом поместить в шарообразную колбу с длинным носиком. Можно ли их обоих в одну большую пробку вставить?
К носику подсоединить трубку и опустить в бОльшую емкость с избытком воды. Неусвоенный олеум - в вытяжной шкаф.
-
Я думаю не сплавятся они, карбонат аммония просто разложится
А если допустить такую возможность, что при давлении углекислый газ из карбоната аммония прореагирует с оксидом цинка с образованием карбоната?
-

слева направо сверху вниз
метилбутират
этилпропионат
метилизобутират
пропилацетат
изопропилацетат
+

бутилформиат
2-метилпропилформиат
1-метилпропилформиат
третпропилформиат
-
-
1) При разложении 20 г. карбоната кальция получено 20 г. оксида кальция. Какова массовая доля выхода продукта от теоретически возможного в процентах.
2) При окислении 7 л. оксида серы(4) кислородом получили 20 г. оксида серы (4). Каков выход продукта.
Эйнштейн с СТО нервно курит в сторонке.
3) Найдите объем водорода (л), необходимого для получения 256 г меди из оксида меди (II), если массовая доля выхода продукта составляет 80% от теоретически возможного.
CuO + H2 = Cu + H2O
n(Cu) = 4
n(CuO) = 4
mт(CuO) = 384г.
mп(CuO) = 480г
-
А чем не подходит выпаренный электролит? Если уж так нужно, по моему проще найти каких нибудь друзей ООО или ЧП/ИП и купить с их помощью хч или осч.
Сера есть, около 2-3 кг, через пару месяцев подходит срок утилизации.
Интерес не в кислоте, а в ходе эксперимента.
-
Проще другие способы получения рассмотреть.. Мне кажется таким способом как Вы предложили, очень и очень сложно получить сабж..
Другие способы получения слишком денежно- энерго- ресурсо- затратны, что собственно и не устраивает.
Способ хоть и сложный, но при достаточной экипировке (SO3 - воистину аццкая вещь) и определенном оборудовании, думаю, должно получиться.
Мне ж её не тоннами гнать, как максимум 2х литров хватит 60% для начала.
В общем, самое опасное место - усвоение.
Тогда предложение сделать аппарат для перегонки, в котором в первую колбу будет подаваться олеум, там все это дело будет кипеть, перегоняться во 2ю колбу, в 1ю по мере необходимости добавляем дистиллят. Хотя это не есть хорошо: в кипящую кислоту добавлять воду.
Кварцевые колбы есть, должны выдержать.
Попробую сделать эксперимент на паре грамм серы, как проведу - отпишусь.
-
Кончено, ещё глубже охлаждать надо..
Эх, действительно, кипит, родная, при растворении.
Возник вопрос по конденсации паров SO3, ибо не хочется их выпускать, да и серная кислота тоже испарится. Если переборщить с давлением - пойдёт через вентилятор, ему придёт конец да и тем людям, которые будут рядом, тоже станет несладко.
Значит нужен источник тепла низкой интенсивности (электроплитка?) и хороший охлаждающий аппарат (тазик с сухим льдом?).
Или надо достать систему охлаждения из холодильника, переварить и её использовать.
-
Если память мне не изменяет растворение SO3 очень экзотермическая реакция, хотя я могу ошибаться..
Охлаждения проточной водой стенок хватит или надо ещё глубже охлаждать?
Если будет закипать, тогда лучше зонтик и в вытяжном шкафу.
По такому поводу: где можно найти кислотоупорную резину?
-
S + O2 --> SO2 Внутри колбы это точно произойдет... А вот дальнейшие окисление 2SO2 + O2( V2O5) -->2SO3 без катализатора не пойдет..
В принципе, есть горелка под 800 гр, над ней можно будет согнуть стекло, сделать "кармашек" для оксида ванадия. Только вот где его достать?
V2O5 не будет реагировать с SO2, SO3? В данном случае он как катализатор, это понятно, но все-же не будет идти паразитарная реакция? Ванадий амфотерен, а значит и его оксиды - тоже. Но высший оксид, наверное, проявляет больше кислотные свойства. Много его не хочется тратить.
А по поводу остальных узлов какие замечания/предложения?






Электролиз Fe2(SO4)3
в Решение заданий
Опубликовано
10-водный сульфат железа (III) плавится при 170 градусах, разлагается при 500+
Как можно расплавить хлорид натрия?