-
Постов
10617 -
Зарегистрирован
-
Посещение
-
Победитель дней
47
Тип контента
Профили
Форумы
События
Сообщения, опубликованные M_GM
-
-
Есть разные обозначения для разных констант равновесия.
Константа равновесия вычисленная через молярные концентрации обозначается КС,
- через парциальные давления Кр, Эта обозначение читается "Ка-пэ", т.е. буквица "р" понимается как символ давления, латинская буква "р".
- через мольные доли веществ в равновесной смеси - Кх.
Судя по заданию, если вы его точно скопировали, нужно найти константу Кр, т.е. выраженную через парциальные давления
Итак: константы "Ка-цэ", "Ка-пэ" и "Ка-икс"
-
 1
1
-
-
13.06.2022 в 17:36, Ukt,P сказал:
1)CuSO4 + 6NH3 + 2H2O → [Cu(NH3)2](OH)2 + (NH4)2SO4.
1 - азот не уравнен
2 - для медноаммиачного комплекса характерно К.ч.= 4. здесь [Cu(NH3)2](OH)2 у меди К.ч.= 2.
Что странно, тем более что речь идет о "избытке раствора аммиака"
-
 1
1
-
-
Возможность протекания ОВР определяется ЭДС реакции,
которая в свою очередь равна разности ОВ потенциалов (ОВП)
ЭДС = ОВП(окислителя) - ОВП(восстановителя)
Стандартные ОВП типичных окислителей и восстановителей приводятся в справочных таблицах
Для реакции 2 окислителем является сопряженная пара (MnO2+4H+/Mn2++2H2O)
восстановителем - ( I2/2I=). По данным таблиц ОВП(окислителя) = 1,23 В,
ОВП(восстановителя) = 0,54 В, ЭДС = 1,23 - 0,54 =0,69 В
ЭДС > 0 - следовательно реакция возможна
-
 1
1
-
-
Пиши формулу угарного газа и
уравнение его реакции с оксидом меди (именно он "может восстановить до металла 10г оксида меди")
по этому уравнению рассчитывай, сколько литров угарного газа было в 11,2 л смеси
Ну а дальше всё просто

-
А кто сказал, что основание должно быть неорганическим?
-
-
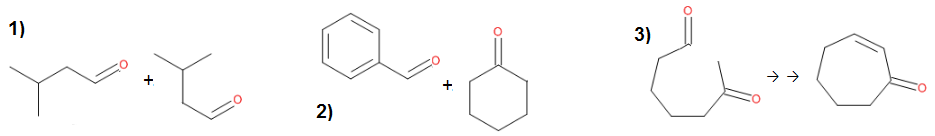
А что непонятного? Молекула рвётся по двойным связям, концевые атомы окисляются до карбоксильных групп:
Циклогексадиен-1,4 :
CH=CH COOH HOOC
/ \ / \
CH2 CH2 → CH2 + CH2
\ / \ /
CH=CH COOH HOOC
В случае циклогексадиена-1,3 вторым продуктом должна бы получиться щавелевая кислота HOOC-COOH,
но она легко окисляется дальше до углекислого газа
-
Надо найти К равновесия.
В состоянии равновесия v(пр) = v(обр), т.е. k(пр)[А] = k(обр)[В]
откуда Кравн = [В]/[А] = k(пр)/k(обр) = 20/12 = 5/3 = 1,667
Поскольку молярные массы изомеров равны, то [В]/[А] = m(В)/m(А) =1,667
Имеем систему двух уравнений:
m(В)/m(А) =1,667
m(В)+m(А) =10
Решаем

-
 1
1
-
-
Следует сразу учесть, что у вас 2 атома серы:
2S- -14e → 2S+6
Fe+2 -1e → Fe+3
Следовательно восстановитель суммарно отдаёт 15е
-
 1
1
-
-
Надо строить график и по графику находить данные для расчётов
-
06.06.2022 в 13:48, мимо_шёл сказал:
Раствор натрий силиката массой 61г с массовой долей соли 2%, смешали с избытком хлоридной кислоты. Вычислите массу образованного осадка.
...
m(NaCl)-?
А ты считаешь, что у тебя NaCl выпадет в осадок?

-
 1
1
-
-
Неправильно считаешь Кр.
Не учитываешь коэф-ты в уравнении реакции
-
 1
1
-
-
Те же условия те же вещества - значит К равновесия будет иметь то же значение
По первому эксперименту рассчитывайте Кравн и используете для обсчёта второго эксперимента
-
 1
1
-
-
03.06.2022 в 02:00, Вадим Вергун сказал:
(x(27+16*3/2)+(1-x)*(23+16))/(x*27+(1-x)*23) = 1.75
x=0.25
Если исправить 23 в этой строчке на 24, может и удастся пропихнуть её как решение ...
Если еще посчитать то, что надо и прийти к правильному ответу
-
Пишите уравнение реакции и думаете, почему масса пластинки увеличилась
-
Впервые запах стал видимым !!!

Интересно, если в условии сказано, что к раствору NaOH добавили серной кислоты,
вы тоже не сможете утверждать, что при этом прошла реакция?
Пока не увидите (пальчиком
 ), что пробирка нагрелась?
), что пробирка нагрелась?
-
 1
1
-
 1
1
-
-
Пиши свои полуреакции, будет видно, почему не сходится и где ошибка
-
31.05.2022 в 19:54, dmr сказал:
Что не помешает приготовить его прозрачный однопроцентный раствор,
добавить туда сколько получится азотной кислоты и утверждать,
что прошла реакция CH3COO(-) + H(+) = CH3COOH
без видимых признаков её протекания.
-
-
 1
1
-
-
0,88 моль/л - результат более правдоподобный.
Но!
Расчёт осмотического давления ведется по формуле, где все величины должны быть в системе СИ,
а литр - внесистемная единица, а значит и моль/л.
Поэтому в данных расчётах надо использовать концентрацию в моль/м3
См =0,88 моль/л = 0,88*103 моль/м3 = 880 моль/м3.
Если же вы берёте концентрацию в моль/л вы давление получаете в кПа.
-
Неверно, поскольку 5% - это массовая доля хлорида натрия в растворе
и позволяет найти найти массу вещества по известной массе раствора
Найденное значение СМ - просто дикое, должно получиться около 1 моль/л ~ 1000 моль/м3
-
Всё верно, на мой взгляд.
Единицы измерения не везде пишешь

Вот это вот, например что такое? в чём измеряется?
Такое впечатление, что массу в граммах посчитал.
-
В растворе есть избыток ионов калия. Наличие одноимённых ионов уменьшает растворимость соли
Исходный то раствор перхлорат натрия? Судя по уравнению реакции?
В растворе будет 0,04 моль перхлорат-ионов и 0,09 моль ионов калия
После протекания реакции в растворе останется 0,05 моль избытка ионов калия
концентрация которых будет равна 0,05/0,5=0,1 моль/л
ПР=[K+ ]*[ClO4- ], где [ClO4- ] =s, [K+ ]=s+0,1
Получаем уравнение s(s+0,1) = 1.1*10-2, откуда находим s
-
 1
1
-
-
Лучше так:
1|Fe+3 -3e -> Fe+6 восстановитель-1 | -3 |
3|N+5 +2е -> 3N+3 окислитель | +6 | +3 | 2
--------------------------------------------| |
Fe0 -6e -> Fe+6 восстановитель-2 | -6 | 1
-----------------------------------------------------
2Fe+3 -6e + 6N+5 +12е + Fe0 -6e = 2Fe+6+ 6N+3+ Fe+6
2Fe+3 + 6N+5 + Fe0 = 3Fe+6 + 6N+3
-------------------------------------------------------
2Fe(NO3)3 + Fe + 12Na2CO3 = 3Na2FeO4 + 6NaNO2 + 12CO2
Здесь
1|Fe+3 -3e -> Fe+6 восстановитель-1 | -3 |
3|N+5 +2е -> 3N+3 окислитель | +6 | +3 | 2
коэффициенты 1 и 3 берутся из состава частицы Fe(NO3)3,
числа +3 | 2 относятся и к железу(+3) и к азоту, т.е. к сумме двух первых уравнений


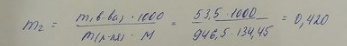
Константа равновесия и молярные концентрации
в Решение заданий
Опубликовано
Конечно.