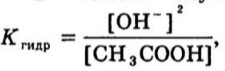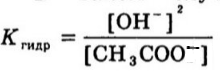-
Постов
10617 -
Зарегистрирован
-
Посещение
-
Победитель дней
47
Тип контента
Профили
Форумы
События
Весь контент M_GM
-
Начните с того, что выясните, что такое "фосген" и напишите уравнение реакции. Неплохо также выяснить, сколько останется СО и хлора, когда прореагирует 51%СО
-
Бутандиовая кислота, 2СO2 + MnSO4 + MgSO4 Пишите электронные уравнения Только что делали нечто похожее:
-
Поддержу. Только тогда и получится - 8е И коэффициенты баланса будут другие. Дальше показывайте, думаю все получится
-
В продуктах сгорания у нас три элемента углерод, водород и ... кислород! Значит эти три элемента могли быть и в исходном веществе (кислород не обязательно)
-
ω-3-кислоты имеют двойную связь у третьего атома углерода считая с конца: 1 - - 2- - 3 CH3CH2CH=CH-CH2(CH=CHCH2)4(CH2)2CO2H - это ω-3-кислота А это: 1 - - 2-5 - - 6 CH3(CH2)4-CH=CHCH2CH=CH(CH2)7CO2H - ω-6-кислота
- 2 ответа
-
- 1
-

-
Это надо вспомнить классификацию аминокислот, и формулы аминокислот, скрытых под обозначениями Arg, Pro, ... и т.д.
-
Пишите, как реагирует спирт с бромоводородом, (хотя бы на примере этанола) Зная плотность по гелию находите М вещества, используя массовые доли находите, сколько в молекуле водорода и углерода и всё станет ясно. Здесь: "массовой долей H – 58.32%" видимо опечатка. Надо читать "массовой долей H – 5,832%" Но и это значение не подходит. По молярной массе неизвестное вещество С4Н9-Br, но в нем массовая доля водорода равна 6,57%
-
- Потому, что при перегонке отбираем фракцию с Ткип близкую с Ткип чистого вещества - Вода тоже летучее вешество, к тому же она часто образует азеотропы и перегоняется вместе с очищаемым веществом. Поэтому лучше ее удалить предварительно - с небольшой скоростью, позволяющей контролировать температуру отгоняемых паров. - степень чистоты можно определить по показателю преломления очищенной жидкости, сравнив его со справочным значением - что вверху, что внизу можно определить посмотрев в справочнике плотность орг. жидкости, и вспомнив плотность воды. Если не вспомнили - тоже посмотреть в справочнике!
- 1 ответ
-
- 1
-

-
Поскольку тиосульфат бария плохо растворим, единственное что здесь возможно - реакция обмена, где тиосульфат бария выпадает в осадок.
-
Водород в ряду напряжения стоит для рН=0 т.е для 1н раствора кислоты При рН=7 потенциал водородного электрода = -0,41 В, где-то на уровне железа Так что только железо и стоящие перед ним металлы теоретически могут вытеснять водород из такого растора Но если учесть оксидные пленки, то реально - щелочные и щелочноземельные, например натрий. А в алюминиевых кастрюлях мы переспокойненько кипятим воду при рН=7
-
Стоящие в начале ряда напряжений, щелочные и щелочноземельные, например натрий.
-
От состава и строения кислоты, отображаемого структурной формулой. Т.е грубо говоря, "от формулы кислоты"
-
Тогда понятно, зря я пересчитывал на год.
-
Дополним: Мольная часовая производительность: n(C5H10)=95238/70=1360,542 кмоль/ч. Чтобы получить данное количество пентена необходимо, чтобы в пентен превращалось 1360,542 кмоль/ч пентана, массой 97959 кг Одновременно будет получаться водород 1360,542 кмоль/ч, массой 97959 - 95238 = 2721 кг/час С учетом селективности превращения в пентен, при этом всего будет расходоваться 97959/0,75=130612 кг/ч пентана при этом 32653 кг/ч пентана будет превращаться в побочные продукты, массой 32653 кг/ч (Не очень понятно, зачем надо было пересчитывать приход/расход на один час, а затем снова на год? Можно было сразу работать с годовыми величинами) Приход: Пентан, 1567347 т/год. Выход: Пентан, не вошедший в реакцию 470204 т/год. Пентен, 800000 т/год Водород, 2721*(350*24) = 22857 т/год Побочные продукты 32653*(350*24) = 274286 т/год Всего =470204+800000+22857+274286 = 1567347 т/год
-
А расход из 1) Пентена; - задан 2) Водорода, который образовался из реакции дегидрирования пентана;- можно рассчитать 3) Пентан, который вообще не прореагировал. - рассчитали 4) Побочные продукты - можно рассчитать по закону сохранения массы И приход будет совпадать с расходом!
-
Точнее: Чтобы получить данное количество пентена необходимо, чтобы в пентен превращалось 1360,542 кмоль/ч пентана, массой 97959 кг С учетом селективности превращения в пентен, при этом всего будет расходоваться 97959/0,75=130612 кг/ч пентана при этом 32653 кг/ч пентана будет превращаться в побочные продукты С учетом конверсии пентана для этого в реактор должно подаваться 130612/0,7=186589 кг/ч пентана при этом 55977 кг/ч пентана не будет подвергаться конверсии и уходить с продуктами реакции За год расход пентана составит 186589*24*350/1000=1567347 т/год, при этом из отходящих газов реактора может быть возвращено в производство 470204 т/год пентана При условии 100%-ного возврата расход пентана составит 1097143 т/год
-
Ну посчитай на калькуляторе [H]=Кw/[OH] = 10-14/9,4*10-6 Чтобы делить на 9,4 надо сначала числитель дроби записать так: 10*10-15. 10/9,4 ~=1 Да, тут видно ошибка: [H]=Кw/[OH] = 10-14/9,4*10-6 =~ 1*10-9 Вообще в этом источнике что-то много ошибок. Например в фразе: "В таком случае из уравнения (2) следует, что " формулу следует читать так:
-
Вот где вы там С0 и С-2 увидели, вот что интересно? Окисляется углерод ...☰С-ОН - у него степень окисления? и окисляется углерод ...-СН3 - - у него степень окисления?
-
Всё может быть: а) ошибки при переписывании б) опечатки в ответе или в условии задачи
-
5,6 - это, я думаю, рОН этого раствора Вот, из уравнения (1) видно, что реакция раствора должна быть щелочная, pH>7. Из уравнения (3) можно найти Кг = Kw/Кд А из уравнения (2), переписав его так: Кг = [OH]2/Cсоли найти концентрацию гидроксид-ионов
-
А если соль образована слабой кислотой и сильным основанием, какая среда будет в ее растворе кислая или щелочная? А гидролиз этой соли идет по катиону или по аниону? И хорошо бы увидеть уравнение реакции гидролиза в ионной форме, какие там ионы образуются Н(+) или ОН(-)?