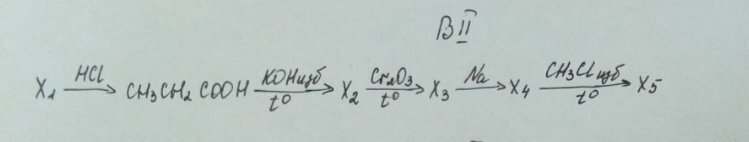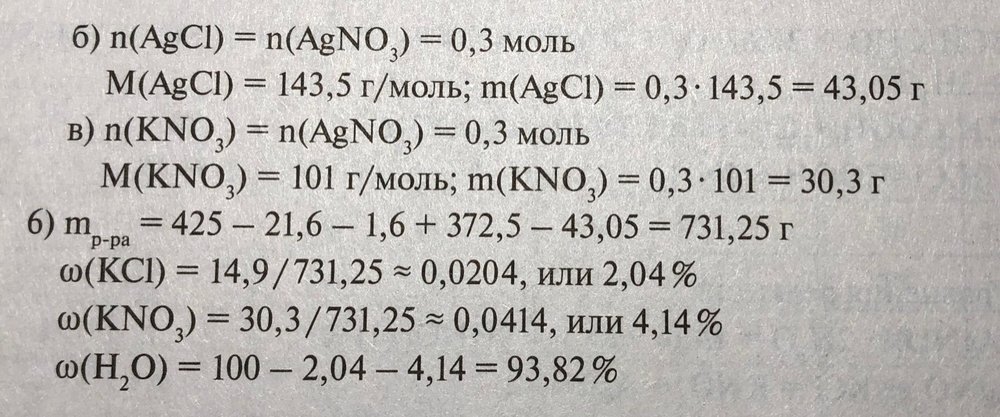Поиск
Показаны результаты для тегов 'ЕГЭ'.
Найдено 44 результата
-
циклогексадиен-1,4 и окисление перманганатом калия с гидроксидом калия с образованием малоната калия, манганата калия и воды ( напиши уравнение реакции с коэффициентами)
-
Хлорид железа (III), гидроксид натрия, карбонат калия, сульфат цинка, гипохлорит натрия, хлорид меди (II) Из предложенного перечня выберите два вещества, между которыми возможна реакция ионного обмена, не приводящая к образованию осадка или выделению газа. Запишите молекулярное, полное и сокращённое ионное уравнения реакции с участием выбранных веществ.
- 29 ответов
-
- егэ
- егэ по химии
-
(и ещё 2 )
C тегом:
-
В задаче 34 ЕГЭ нужно было рассчитать количество сернистого газа, который выделяется при окислении двух твердых растворимых бромидов. При расчёте по условиям задачи оказалось, что концентрированная серная кислота в составе олеума находится в недостатке по отношению к бромидам. Возник вопрос - может ли вода, которая образуется в ходе процесса окисления, захватываться ангидридом и нивелировать исходный недостаток кислоты? Понятно, что в задаче это не учитывали. Но стало интересно, почему это считается очевидным авторами, что даже указаний на пренебрежение вторичными реакциями нет (хотя обычно на это так или иначе в школе указывают). Ведь по всем законам ангидрид - сильный водоотнимающий агент. Разве он не сможет в ходе реакции захватывать образующуюся воду, давая нам серную кислоту и добивая процесс до полного окисления всей соли, даже при исходом недостатке серной кислоты (примерно в 2 раза)? Заранее спасибо!
-
Будет ли проходить ОВР между H2O2 KNO3 H2SO4 ?
-
Великие химики этого форума, пожалуйста, рассудите. Вернулся после ЕГЭ, написав там вот такую реакцию: NaNO2 + H2SO4 = NaNO3 + SO2 + H2O Такая реакция возможна?
-
Образец тригидрата нитрата меди (II) разделили на две части так, что общее число электронов во второй части оказалось больше общего числа электронов в первой части в 2 раза. Первую часть кристаллогидрата прокалили до постоянной массы. Выделившиеся газы собрали и охладили, их объем при нормальных условиях составил 14 л. Из второй части кристаллогидрата приготовили насыщенный раствор при 40°C (растворимость кристаллогидрата при 40°C составляет 381 г в 100 г воды) и провели электролиз до тех пор, пока на инертном аноде не выделилось в 2,5 раза меньше газа, чем объем газов, выделившихся при разложении первой части кристаллогидрата. Вычислите массовые доли веществ, находящихся в растворе после электролиза. В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения искомых физических величин).
-
- егэ
- электролиз
-
(и ещё 3 )
C тегом:
-
Объясните, пожалуйста, МАКСИМАЛЬНО подробно, почему n(H)=2n(H2O).
-
Доброго времени суток! Мой вопрос может прозвучать максимально абсурдно и бредово. В школе нам говорят именно заучить реакции, говорят про исключения и т.д. Так набираются несколько реакций, затем десяток, затем еще один и так далее. Такое количество реакций для сдачи егэ, по-моему, достаточно сложно выучить. Есть ли какие-либо законы, принципы и т.п., с помощью которых можно облегчить себе жизнь в заучивании реакций (как органика, так и неорганика) именно для егэ?
-
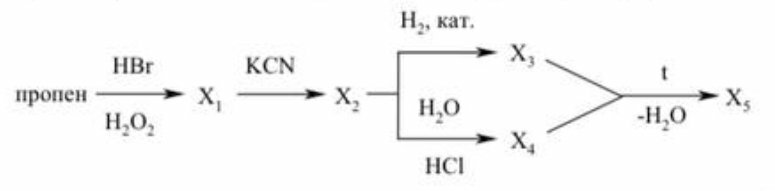
X3 это 1- аминобутан X4-масляная кислота, что нужно сделать, чтобы получить X5? Нужно получить x5 в одну стадию?
-
Здравствуйте, нуждаюсь в подробном решении задачи: 17 литров смеси этилена с водородом пропустили над нагретым платиновым катализатором. После пропускания над катализатором плотность по водороду газовой смеси равна 10.8. Определите содержание водорода в исходной смеси (указать объем в литрах, округлить до целого числа). Ответ: 10 литров Заранее большое спасибо!
- 2 ответа
-
- газы и их смеси
- егэ
-
(и ещё 2 )
C тегом:
-
Здравствуйте, подвернулась вот такая вот задача, очень буду рад подробному решению: При действии воды на 15 г смеси карбида и гидрида кальция выделился газ с плотностью по водороду равной 4,3. Определите массу гидрида кальция в смеси. Ответ округлите до целого числа. Правильный ответ: 7 Знаю, что при двух разных реакциях получается 2 разных газа, ацетилен и водород. Составил соотношение между ними, приравнял к количеству молей гидрида кальция и карбида, но выходит 9.5.
-
Молярная масса углерода= 100-51,064-29,787-6,343= 12,806% Моли водорода=6,383 Азота=2,127 Кислорода = 3,191 Углерода = 1,064 Истинная формула получилась CH6O3N2 что очень странно. Где я допустила ошибку? Помогите пожалуйста, спасибо
-
Помогите пожалуйста решить цепочку. Я думаю Х1 это соль - пропионат калия. Х2 не знаю, в ступоре. Помогите пожалуйста. Может там должен получиться бензол?
-
Выбор между CuSO4 и ZnSO4 при реакции с NH3 в растворе
Misha20062006 опубликовал тема в Решение заданий
В двух колбах находились бесцветные растворы веществ X и Y. В обе колбы добавили избыток водного раствора аммиака. В колбе с веществом X осадок сначала выпал, а затем растворился, а в колбе с веществом Y осадок выпал и не растворился в избытке реагента. Из предложенного перечня выберите вещества X и Y, которые обладают описанными свойствами. CuSO4 H2SO4 ZnSO4 Fe2(SO4)3 K2SO4 При решении этого задания у меня возник вопрос, почему правильным ответом считается 34. То есть как вещество X взят именно ZnSO4. Почему не подходит CuSO4. Видел похожую тему на этом форуме, где человек прописал эти реакции. Они идентичны, но тогда почему не подходит CuSO4? > -
Здравствуйте, объясните, пожалуйста, почему в этой задаче нельзя взять H3PO4 вместо K3PO4? (Правильный ответ 24)
-
CaO + CO2 = CaCO3 + Q Я решал задание из ЕГЭ на равновесие. Там был вопрос о том, куда сместится равновесие, если добавить аргон (при постоянном объёме). Я думал, раз слева есть газ, то равновесие сместится вправо, ибо если мы добавим ещё газа, пусть и другого, то повысится давление, однако оказалось, что равновесие практически не смещается. Подскажите, пожалуйста, в чём я не прав?
-
Из предложенного перечня внешних воздействий выберите все воздействия, которые приводят к увеличению скорости химической реакции Fe(тв.) + 2H+ = Fe2+ + H2(г.) 1) увеличить концентрацию ионов железа 2) увеличить концентрацию ионов водорода 3) уменьшить давление 4) уменьшить концентрацию кислоты 5) увеличить температуру В ответах написано что правильные: 235, но я не могу понять как уменьшение давления в этой реакции может увеличить скорость
-
HELP!! Иду на апелляцию ЕГЭ. Мне не засчитали эту реакцию. Я ее нашел в учебнике Лидина "Неорганическая химия в реакциях 2007", сборнике ЕГЭ с вариантами, в интернете и в ответах на решуЕГЭ. Возможна ли реакция на самом деле? Какие условия ее протекания? В каких еще источниках можно посмотреть эту реакцию (чем больше тем лучше)? Как мне еще аргументировать экспертам, что эта реакция возможна и ее нужно засчитать? Спасибо за помощь. P.S. Часто находил эту реакцию, где образуется не H2SO4, а просто S. В Лидине есть и та и другая реакция.
-
-
Здравствуйте! При решении задачи столкнулась с неточностью в ответе. В решении, указанном составителями сборника, в ответе не учитывается концентрация HNO3, хотя при расчёте массы раствора массу азотной кислоты не вычли. То есть в растворе она есть, но её массовую долю не находят. Можете ли объяснить, почему? Или же это просто неточность или опечатка? Заранее благодарю за помощь. Прикрепляю условия задачи и решение:
- 1 ответ
-
- егэ
- егэ по химии
- (и ещё 7 )
-
Предлагаю качественную подготовку по химии и математике, а также подготовку к сессионным экзаменам и олимпиадам по химии любого уровня сложности. Химия - любое направление, математика - алгебра, линейная алгебра, математический анализ. Опыт преподавания более 10 лет. Индивидуальный подход работы для каждого ученика в зависимости от уровня подготовки и способностей. Наука и преподавание моё любимое дело, а за плечами большой опыт и множество благодарных учеников, успешно сдавших ЕГЭ, вступительные экзамены и дипломные работы.
-
Органическая Цепочка ЕГЭ, не понимаю последнюю реакцию
ARMAGEDON_MINOR опубликовал тема в Решение заданий
бутадиен-1,3 --(+KMnO4+H2O)--> X1 --(+HBr (избыток))--> X2 --> этин Мои мысли таковы: из бутадиена получаем либо двухатомный спирт с двойной связью посередине (он такой существует вообще?), либо четырёхатомный спирт. Дальше соответственно либо дибромпроизводное с двумя гидроксогруппами, либо тетрабромпроизводное. Но даже если так, то как же из этого получить этин?? Несколько позже в другой цепочке встретилась реакция, в которой нужно из оксалата калия получить формиат калия. После этих двух цепочек появилась мысль, что, наверное, существует какая-то реакция, с помощью которой можно разрывать сигма-связь. А я о ней не знаю. Есть ли такая? Или, может быть, всё гораздо проще и я чего-то не замечаю? -
Установите строение непредельного спирта, если известно, что 11,2 г его могут прореагировать с 4,6 г. натрия или присоединить 64 г брома. Какие продукты образуются при гидратации и дегидрировании этого спирта?