-
Постов
3834 -
Зарегистрирован
-
Посещение
-
Победитель дней
35
Тип контента
Профили
Форумы
События
Сообщения, опубликованные ash111
-
-
В 19.01.2024 в 23:18, aversun сказал:
Сульфурол летуч, улетит....
Я его от воды перегонкой сушил, правда я тогда не знал что это называется сульфурол.. Он кипит около 60°С на 0,2 mm Hg, так что единственное что может быть - что он летит с паром (у меня то в нем воды было процентов десять, но для мицунобы это было уже критично). Только даже если так, это не проблема, просто собираешь это пар в приемнике, и оттуда экстрагируешь.
А вот касторовое масло - для меня странно.. какие там коэффициенты распределения - одному богу известно. Считает для него logP около нуля, сколько раз надо экстрагировать касторовым маслом, а потом из него, короче я бы не рискнул с таким заводиться
-
 1
1
-
-
В 18.01.2024 в 23:34, terri сказал:
Доброго времени суток!
Есть водная смесь шоколадного цвета и запаха, в которой находится 1% сульфурола.
Кто бы что посоветовал, как бы его выделить?
Пробовала прибавить нерастворимый в воде растворитель. Растворитель исчез в этой смеси, как в черной дыре,
не образовав никакого второго слоя.
Вот не знаю, пойдет ли сульфурол с водяным паром...
Заранее большое спасибо за все мнения!
упарить воду досуха, вытягивать оттуда вашим нерастворимым в воде растворителем. упаренную воду тоже проэкстрагировать можно, там уже не будет никакой черной дыры.
-
В 18.01.2024 в 21:17, Razor8 сказал:
так то если представить что в растворе есть толуол, вода и немного бромоводорода, то через некоторое время там все превратится в бензиловый спирт и небольшое количество бензилбромида.
бромоводород будет потихоньку окисляться кислородом воздуха, бромировать метил, тот в свою очередь иногда разваливаться в бензиловый спирт.
с фантазией у вас полный порядок. Сделайте документалку про рождение и развитие жизни на Земле в параллель с постепенным превращением толуола в бензиловый спирт.
Довольно необычно будет.
-
В 13.01.2024 в 13:28, chemister2010 сказал:
Что-то не могу найти примеров 1,1,1-триацетоксизамещенных веществ. Нашел только (CH3COO)2CHOCH3.
Ну потому что их нет, вообще. Я уже писал про это, ортоэфиры можно еще получить, но уже даже они дико реакционноспособные.
У автора приступы безудержной фантазии.
Нам на фирму заходили заказы на синтезы ортоэфиров с остатками сложнее метила и этила - кажется 75% из них так и не сделали, потому что сложно всё - заставить реагировать, выделять, чистить. А автор хочет три ацетила. Я уже молчу о том насколько токсичной была бы такая байда.
-
В 10.01.2024 в 10:29, Светлана1998 сказал:
В чем может быть причина?
в ограниченной растворимости
понизили температуру, часть вещества выпала. прогрейте снова до 40-50 градусов и оно опять растворится
-
В 09.01.2024 в 18:01, IronFenyx сказал:
Какая разница? Они ж всё равно замещаются.
нет, водороды нуклеофильно не замещаются, разве что на металлы, но не в вашем случае.
В 09.01.2024 в 18:01, IronFenyx сказал:Вот такой (вложение).
без шансов. уже объяснял почему.
В 09.01.2024 в 18:01, IronFenyx сказал:при чем тут ацетил, если ацетил это CH3CO
окей, ацетатом, я оговорился, имея в виду условный конечно же ацетат. Ацетатом не заместите. Даже один галоген, не говоря уже обо всех.
В 10.01.2024 в 07:20, IronFenyx сказал:А концы этой молекулы в обязательном порядке облепить хвостами
Херня, не получится.

вот такое чтото - нормально.
В 10.01.2024 в 07:20, IronFenyx сказал:только где такой спирт взять длинный и с 4-мя гидроксилами кучкой в самой середине?...
совершенно верно, нигде.
-
В 09.01.2024 в 14:58, Difizik сказал:
Физхим? Насколько помню ничего подобного там не было. Физическая химия описывает химические явления с точки зрения физики, в книги же описаны основы, да и при том, там нет ни слова про термодинамику, фотохимию и т.д., возможно вы имели ввиду какие-то отдельные темы или разделы, в которых дана физическая характеристика, например подобное было в предисловии к радиоактивности в рамках строения атома. Может быть я вас не так понял или мы говорим про разные вещи, но я читал "Общую химию" Глинки 84-го года под редакцией Рабиновича, никакого упоминания про разделы физической химии я там не помню, но конечно никаких глубоких знаний из неё вы не получите, опять же повторюсь в ней только основы основ.
Органической химии в этой книжке - три страницы. Неорганическая - в объеме школы. Аналитической нет. Остается какая? чем вообще этот томище заполнен? не помню уже, но выбора какбы особо нет
у вас она есть - зафоткайте оглавление)
А, ну да, общая химия это так и называется, как книжка, но она ж по сути физическая.
-
В 06.01.2024 в 19:11, Епифооон сказал:
как идет присоединение всяких элементов к углеродной цепи как влияет их радиус как влияет электронное облако на присоединение и тд.
реутов, курц,бутин, мгушное издание. там в основном все есть.
Если тебя интересуют элементы вообще все типа там железа и кальция и марганца, то в целом можно сказать следующее: идет хреново, а когда идет хорошо, по получается такая гадость, что лучше бы оно шло плохо)
В 06.01.2024 в 19:11, Епифооон сказал:1,10дихлордекан и ацетиленид натрия, вот что в этом случае будет получаться
ничего. дибром надо брать. с дибром - зависит от концентрации, что получится..)
В 06.01.2024 в 19:11, Епифооон сказал:Сможет ли декан дотянутся до двух натриев в цикл ? Или будет прямая длинная цепь ?
и так и так можно сделать, подбором условий, но если честно то всегда будет некая смесь.
В 06.01.2024 в 19:11, Епифооон сказал:1,2дихлорпропан плюс условно нитрит натрия, куда встанет NO2 группа ?
нуклеофил всегда атакует наименее стерически затрудненные позиции при прочих равных)
но опять плохой пример, получается смесь нитро-соединения и алкоксинитрита
В 06.01.2024 в 19:27, HE KOT сказал:Если что, есть реакция в школе CH3-CH2-CH2-Cl + Na-C☰CH === NaCl + CH3-CH2-CH2-C☰CH
имеется в виду динатрийацетилен, я так понимаю, если вопрос в том, замкнется ли он в цикл или останется линейным
В 06.01.2024 в 19:27, HE KOT сказал:3) CH2(Cl)-CH(Cl)-CH3+ 2NaNO2 --> CH2(NO2)-CH(NO2)-CH3 + 2NaCl опять же ЕГЭшная реакция))
ой, слезы из глаз.. а нет, это кровь
В 06.01.2024 в 19:32, Difizik сказал:Н.Л.Глинку, а именно "Общую химию", там в целом описывается всё, в том числе и органика.
там описано всего по чайной ложке. абсолютно бесполезная книжка, ну может разве что физхимия там более-менее. Органика/неорганика там на школьном уровне. ужасная книга. терпеть ее не мог.
-
В 08.01.2024 в 21:19, IronFenyx сказал:
Идея именно заместить все водороды на эфирные остатки.. а
галогены, может быть, а не водороды? речь была про хлор если я все правильно помню
В 08.01.2024 в 21:19, IronFenyx сказал:Если все водороды заместить, то нету на что нападать И СТЕРИКА мешает..
какая разница какая стерика если не на что нападать)))
В 08.01.2024 в 21:19, IronFenyx сказал:Эфир устойчивый получается..
какой эфир??)
В 08.01.2024 в 21:19, IronFenyx сказал:Ацетилом три галогена заместить не получится, просто забудьте об этом. даже три йода. Если замещать спиртами, это называется ортоэфир, метил- и этил-ортоэфиры известны, а все прочие - попробуй получи. И да, это реагент для получения ацеталей из кетонов, например. Берется кетон, ортоэфир чуть больше эквивалента, туда бросается кристаллик TsOH или любой кислоты и реакция происходит по щелчку пальцев. Это к разговору о том, насколько они устойчивые, инертные и вообще безопасные для человека. Это страшная гадость - ортоэфиры. Просто нарисуйте структуру которая вам примерно нужна, тогда можно посмотреть что из этого нормальное и можно сделать.
-
В 08.01.2024 в 20:48, IronFenyx сказал:
А шо если не карбоксил, а бутоксид алюминия?
Сильное основание, если на втором от галогена атоме углерода есть водород, то пойдет элиминирование вместо замещения. Алкен будет. Ну и самое херовое что от этого алюминия вы потом не отобьетесь, это будет страшнейшая неразделяющаяся чача, можно ее развалить более-менее насыщенным раствором NH4Cl, но как собирать продукт в ваших условиях, я не очень понимаю.
Вообще я советую перед тем как чтото химичить, представить себе в голове весь предстоящий процесс, от смешивания реагентов до получения финальной субстанции. Ознакомиться со всеми физикохимическими свойствами того, с чем предстоит работать. Потому что иначе потом нежданчики будут вылезать один за другим, и весь процесс обратится в мучение без ясных перспектив.
-
В 08.01.2024 в 20:43, IronFenyx сказал:
Идея сделать дешевле чем в магазе
обычно эта идея провальная ибо даже с учетом наценок магазина у производителя на порядок ниже входящие цены на сырье.. Ну и потом госты же не просто так созданы, тут уже один деятель вон хотел делать искусственные жиры похожим способом, но, кажется, вовремя одумался. В гостах прописаны технические характеристики продукта, если по-простому то лицензированный продукт по идее (по идее, вы знаете где мы живем) проверен и не содержит опасных примесей, а у вас с подобными идеями эти примеси будут, с большой долей вероятности. Продукты неполного этерифицирования, с остатками галогенов, а это довольно таки гадостная вещь ибо гидрофобная и содержит галогены - прямая заявка в канцерогены. Ладно бы у вас была некая "хорошая" реакция что без анализа вы бы могли с высокой долей вероятности сказать что всё прошло и полученное может тоже гадость, но не настолько уж и злая. Но у вас-то натурально чача какая-то будет, и методами анализа вы очевидно не располагаете, чтобы результат своих действий оценить. Поэтому опасненько это все, а здоровье, как известно, дороже всего, и не только в фигуральном ключе. В общем - я предупредил)
-
В 08.01.2024 в 20:07, yatcheh сказал:
Ты с неактивированным алкилхоридом помотыляйся!
это да, это да? бесспорно
В 08.01.2024 в 20:31, IronFenyx сказал:ДМСО не пойдет вместо ДМФА (вы его имели в виду)?
Пойдет, но от него очень сложно избавляться, если надо выделить продукт. Эмульсии просто чудовищные образуются. С ДМФА проще.. и его можно отогнать на роторе, ДМСО только на масляном насосе и меееедленно
В 08.01.2024 в 20:31, IronFenyx сказал:удачи) много галогенов вам явно задачу очень усложнят, если честно. у вас экологический чтоли какойто проект, типа взять страшную полихлорированную гадость и из нее сделать чуть меньшую гадость?
В 08.01.2024 в 20:31, IronFenyx сказал:Сульфокислоты вместо карбоновых не лучше? Мне-то пофиг какой эфир - с сульфогруппой даже интереснее было бы.
Ну нееет? наоборот, эфиры серных кислот на галогены нуклеофильно меняют, мезилаты, тозилаты и так далее, чаще всего.
-
В 08.01.2024 в 20:05, Difizik сказал:
Хотя выходит конечно странно, если бы у меня под рукой не было бумажки от учителя, где синем по белому написано про гипотезу, задачи и цели проекта я бы в первую очередь подумал о своей несостоятельности, но выходит так что доля моей вины здесь меньше, чем кажется.
да успокойся, посмеялись - забыли. Не зафлуживай тему?
-
В 08.01.2024 в 19:48, Difizik сказал:
Меня интересовали комплексные соединения меди, никакого частного случая, вопрос то был в другом, дать общую характеристику комплексным соединениям меди, если она есть конечно.
комплексных соединений меди туева хуча, и у вас уточняли, комплексообразование меди с чем вас интересует. Нет никакой общей характеристики, ну разве что то, что это комплексы d-металла. Координационное число может быть разным, степень окисления может быть разной, лиганды могут быть сильные и слабые, здесь необходимо уточнение, одно перечисление вышеописанного займет два урока?
А вы на вопрос о лигандах уткнулись в свою медь. Это тупняк, да ? ниче, бывает
-
В 08.01.2024 в 15:34, IronFenyx сказал:
А тут вроде бы должна реакция легче идти..
хлор просто очень слабополяризуемый. поэтому его заместить относительно сложно, только если он неким образом не активирован, как например в бензилхлориде или аллихлориде.. вот бром или йод - совсем другое дело. Но два галогена при одном атоме углерода это все равно плохо, какой бы галоген там ни был, вон дийодметан алкилирует пирокатехин только при долгом нагревании, а йодметан при комнатной и с разогревом. Понятно, не последнюю роль играет и стерика. Истерика это всегда плохо)
В 08.01.2024 в 15:34, IronFenyx сказал:Может не в этом случае, конечно..
явно не в этом
В 08.01.2024 в 15:34, IronFenyx сказал:А как вариант хлорбензолов?
Никак. Там вообще почти нуклеофильное замещение не идет, в промышленности этот хлор замещают при температурах выше 200 градусов и под давлением, причем это на хорошие нуклеофилы он так замещается типа первичных аминов и спиртов. И это уже SnAr, не обычное Sn1/2
В 08.01.2024 в 15:34, IronFenyx сказал:Но первые два летучие и сильно не нагреешь...
Диметилацетамид можно взять, бутанол, да много вариантов..
В 08.01.2024 в 19:12, yatcheh сказал:Карбоксилаты - хреновые нуклеофилы. Вот и вся байда. Реакция идёт, но как препаративная - полное говно.
Не скажи) нормальная тема, много раз спасала) выходы близки к количественным в случае метилйодида, бензилхлорида/бензилбромида, с первичными йодидами/бромидами можно рассчитывать на в целом хороший выход, ну, с вторичными конечно уже хуже, хотя все равно похоже по выходам с Мицунобой. Берется кислота в DMF, кидается туда поташ 1,2-1,5 эквивалента и добавляется галогенид 1,5 эквивалента, мешается ночь. Можно погреть если надо, обычно несильно) Если кислота довольно сильная как в примере ниже, можно взять гидрокарбонат натрия.
Один раз надо было 2-бром-4-хлор-3-никотиновую кислоту этерифицировать, так вот только таким методом и получилось)
-
В 08.01.2024 в 15:11, dmr сказал:
Ну а как ещё то ответить на такое))
Все правильно ответил, а вот автор тупит)
-
В 08.01.2024 в 12:55, Alihru сказал:
А пройти мимо вы не пробовали?
Тот ответ не приняли, что плохого в том, что я задала вопрос еще один раз?
еще и грубит, лучше бы чат джипити для себя открыла))
 В 08.01.2024 в 12:46, HE KOT сказал:
В 08.01.2024 в 12:46, HE KOT сказал:О наличии карбонильной группы
Ведь эти соединения получаются при замещения С=О группы на -N=N-R
К слову, озазоны - это гидразоны, у которых
С=О
С-ОН (вот эта группа перейдёт в С=О)
Поэтому будет присоединение ещё и по этой группе
И будет получаться
С-N=N-R
C=O +N≡N-Ar --- (-H2O) -->
--> C-N=N-R
C-N=N-Ar
Обобщим: образование гидразонов даёт возможность доказать, что глюкоза имеет карбонильную группу, а озазонов то, что эта карбонильная группа соединения с гидроксильной группой.
Как-то так!
заморачиваешься сильно!) надо забить в чат джипити, скопировать оттуда ответ и убрать из него тупняк)
-
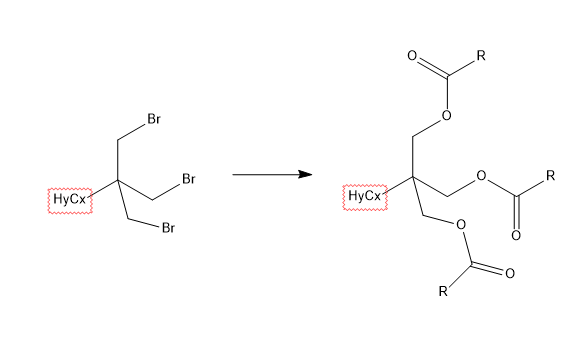
В 08.01.2024 в 09:12, IronFenyx сказал:
В общем, есть такая группа реакций - хлоралканы с солями карбоновых кислот.
есть, да
В 08.01.2024 в 09:12, IronFenyx сказал:вуаля, готов эфир.
не так чтобы вуаля, но можно
В 08.01.2024 в 09:12, IronFenyx сказал:А на практике интересуют условия реакции.
нужно чтото такое, в чем и то и другое растворяется. Спирт (метанол, этанол, изопропанол), спирт/вода, ДМФА, ДМСО, чтото полярное и необязательно апротонное.
В 08.01.2024 в 09:12, IronFenyx сказал:Хлорсодержащие будут не типа дихлорэтана
А вот это плохо, даже дихлорэтан уже плохой алкилятор. Для него придется это все дело кипятить, долго и нудно
В 08.01.2024 в 09:12, IronFenyx сказал:более высококипящие или даже твердые (например гексахлорэтан).
более высококипящие - это плюс (можно выше греть), твердые - пофиг (главное чтобы растворялись, а растворяется хлорорганика в органике обычно хорошо, очень кстати жировую ткань любит, это так, к слову), и да, гексахлорэтан - без шансов. Сущность алкилирования состоит в том что молекула алкилятора неким образом полярная или поляризуемая хотя бы, а гексахлорэтан и неполярный, и оччень плохо поляризуемый, и все эти хлоры это чудовищная стерика. Поэтому о таком можно даже не думать.
-
-
В 06.01.2024 в 19:51, yatcheh сказал:
У коисталлогидратов всё строго. Не проучается дека - идите в жопу со своими гексами. Кристаллизуюсь безводно!
ого, тут даже квантование нервно курит в сторонке)) тока непонятно если все так строго почему в реахимовских банках кристаллогидраты всегда такие мокрые)
-
В 07.01.2024 в 15:48, yatcheh сказал:
Вероятно, тут нужен всё-таки окислитель, запускающий радикальную реакцию димеризации. Скажем, перекись, приводящую к бис-феноксильному бирадикалу, который уже и раскисляется йодом:
2 HO-Ar + 2H2O2 -> *O-Ar-Ar-O* -(I2)-> IO-Ar-Ar-OI
Тимоьный радикал такого рода должен быть довольно стабильным из-за стерической загруженности.
Самый стабильный радикал там должен быть на изопропильном углероде, мало того что третичный, еще и бензильный. Но в целом да, такие штуки синтезируют в помощью всяких одноэлектронных окислений, типа трехвалентного железа и БИДы
В 07.01.2024 в 19:22, A.Schmidt сказал:Вещество йодид тимола не является уникальным и известно химикам и фармацевтам давно. Помимо основного распространённого названия йодид тимола оно имеет множество синонимов: Annidalin, Aristol, Bithymol diiodide, Diiododithymol, Iodosol, Iodothymol, Iosol и т.д.
Интересен способ получения йодида тимола электролизом с инертными электродами раствора тимола, щёлочи и йодистого калия в воде.
Привожу принтскрин с иноязычного научного журнала (D.R.P., 64405, 1891 год):
Тайна раскрыта)) как пить дать там образуется трехвалентный йод и окисляет это все до дифенила
-
В 06.01.2024 в 20:19, BritishPetroleum сказал:
В гремучей ртути же есть азот, а тут он где?
новый, безазотный рецепт
-
 1
1
-
-
В 06.01.2024 в 18:11, Вольный Сяншен сказал:
Это же будет новая реакция. Может быть даже именная.
"Может быть меня даже наградят..." (с)
Посмертно??
В 06.01.2024 в 18:29, Wallic сказал:Метил ртути ацетат, а не просто метиловый эфир уксусной кислоты.
оо, новые идеи получения гремучей ртути, панятна
-

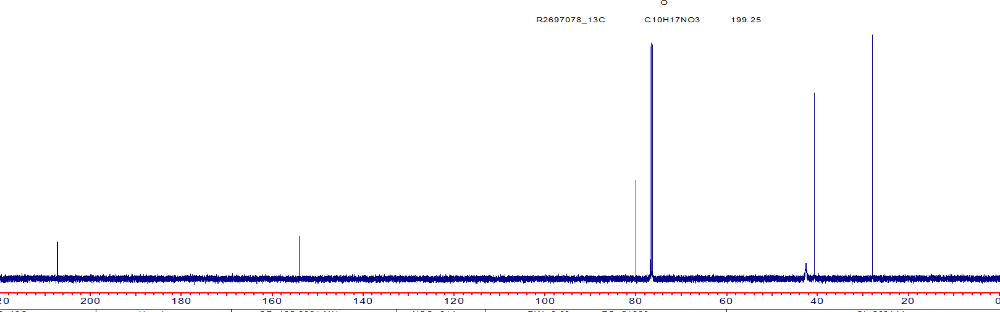
С углеродом, разгадывай, брутто формула на спектре))

.thumb.jpeg.252a9b1bb4bb2764898b676b40684489.jpeg)


Качественный анализ смеси органических красителей
в Органическая химия
Опубликовано
ГЖХ, конечно же, ну точнее GCMS. Один прогон и все понятно, где что и сколько. Правда если там лютая смесь углеводородов типа изомерных октанов, то вот с соотношением отдельных изомеров может быть проблема
У нас например все абсолютированные растворители проверяются именно GCMS, офигенная удобная штука, главное чтоб вещество было летучее