
Vladlenin
-
Постов
298 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные Vladlenin
-
-
Недавно прочёл пост, что люди отбеливают волосы с помощью гидроперита, почитал более подробно что куда зачем, оказалось, что кислородом (из H2O2) они убирают полисульфидные мостики, но в каких молекула - не ясно, решил гуглить из-за чего люди седеют, оказалось из-за понижения меланина, теперь стало вообще не понятно что это за способ отбеливания как он работает и т д.
Кто нибудь расскажет?
-
В 30.03.2024 в 21:21, Shizuma Eiku сказал:
Наоборот, формула CaCl(ClO) хорошо демонстрирует смешанность ионного состава кристаллической хлорной извести. Если быть еще более точным, то там и гидроксид-ионы есть, и вода.
Растворима хлорная известь в воде, глупость сказали.
В 1-м томе Б.В. Некрасова описано хорошо:
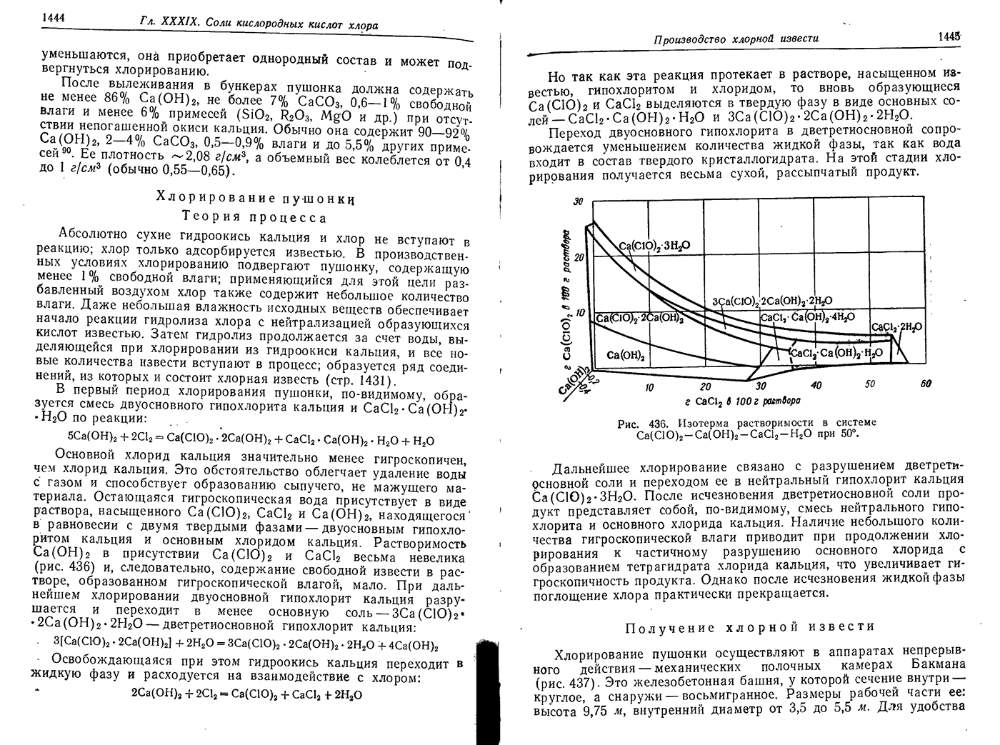
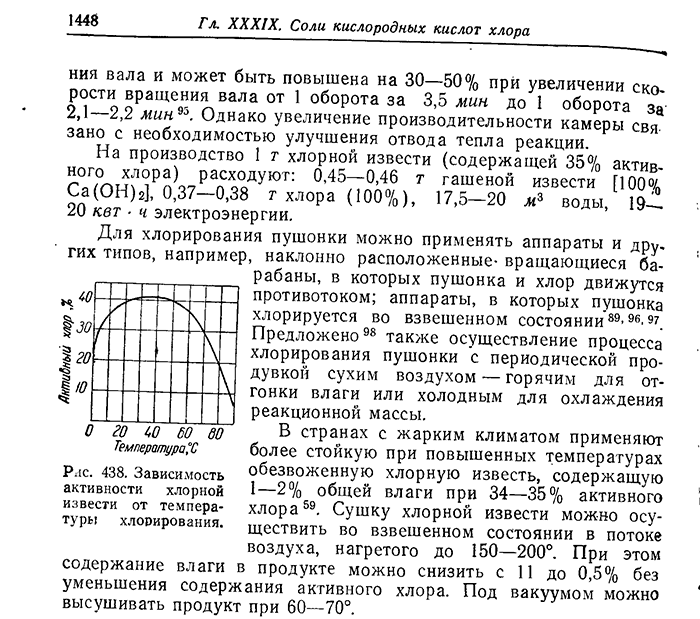
Вот технология получения хлорной извести и гипохлорита кальция (1970-е):
Так-с, спасибо, пойду с этим на кафедру что-ли, разбираться, ещё раз спасибо
-
В 29.03.2024 в 16:57, pauk сказал:
Бред! Вы по какой специальности обучаетесь? Подозреваю, что химия у вас непрофильный предмет.
Химико фармацевтический xD
-
В 29.03.2024 в 13:35, pauk сказал:
Ещё раз - никакого CaOCl2 нет! Есть Ca(OCl)2 и CaCl2. Оба хорошо растворимы в воде. А вот их смешанной соли - нема!
Существование этого соединения меня тоже выгоняет в ступор, но меня интересовала возможность написание его иона в методе полуреакции, т.к на кафедре мне сказали, что он не растворим(если отбросить то, что он шидролизуется), и поэтому его нужно писать как полное соединение, но если почитать наш любимый форум, но там будет противоположное.
И да, на кафедре мне сказали что он существует, но в сухом виде, а так же дополнил, что он у них имеется, но конечно не показали, хотя я бы на глаз его все равно не отличил бы
-
В 28.03.2024 в 23:02, pauk сказал:
Нас учили, что смешанной соли Ca(Cl)OCl в природе не существует. Хотя в учебниках Глинки и прочих нехимиков такое написание присутствует. Если вас устроит почитать что-нибудь про обычную хлорку, то пожалуйста, книжки о ней есть в сети:
Позин М. - Технология минеральных солей, 1949
Егоров А. П. и др. - Курс технологии минеральных веществ, 1950
Позин М. - Технология минеральных солей, изд. 4-е, в двух частях, 1974
Фурман А. А. - Хлорсодержащие окислительно-отбеливающие и дезинфицирующие вещества, 1976
Ахметов Т. Г. и др. - Химическая технология неорганических веществ, изд. 2-е, 2019
И др.Да в том то и дело, что не подходят, нужно узнать, caocl2 растворим или нет?
Не пойму, могу ли я писать полуреакцию с ним?
-
В 28.03.2024 в 20:12, Nemo_78 сказал:
2 Cl- -2e- => Cl2
2 OCl- + 4H+ + 2e- => Cl2 + 2H2O
Как-то так...
Т е он диссоциирует?
-
Ca(CL)OCl+H2SO4 - >Cl2+CaSo4 +H2O
-
Как сказано в заголовке - нужна книга(несколько страниц в книге) про Ca(CL) OCl.
Физические свойства, химические получение и т д
-
В 20.03.2024 в 18:22, Nemo_78 сказал:
Вопрос. Почему у Вас фактор эквивалентности иодида калия 1/2?
Z(KI) =1?
Если да, то я понял свою ошибку
-
Определить массу выделившегося йода при взаимодействии 0,5 л
раствора йодида калия (массовая доля соли 15 %, плотность раствора
1,12 г/мл) в кислой среде с избытком H2O2. При решении использовать
закон эквивалентов.
Как это понять??
Эквивалент у простого вещества?
Что я не так сделал, сразу спасибо за пояснение
-
В 07.12.2023 в 13:47, Nemo_78 сказал:
У меня что-то 1,605 г получилось...
Но считал оченно грубо.
Понял, принял, буду пытаться под этот ответ подогнать решение)
-
Сколько граммов хлорида аммония надо прибавить к 1л 0.05н. Раствора аммиака Kb=1.8*10^-5, чтобы концентрация oh ионов стала 10^-5 моль/л, а коэффициент активности ионов аммония принять равным 0.9.
Изменением объёма раствора после добавления соли пренебречь
Пожалуйста, распишите как это решать, ну или только ответ, спасибо
-
Мне стало интересно, куда можно пойти работать после химфака, сам туда уже врятли поступлю, т.к мат база, но просто интересно, куда можно? И если можноопишите свои Ощущения от работы.
-
В 30.05.2023 в 22:41, бродяга_ сказал:
какой электролиз? катодный или анодный?
после электролиза железа поверхность имеет повышенную активность и нужна защита.
самым распространенный метод обработать нитритом натрия а после сушки пропитка маслами воско-парафинавыми композитами
если не будет лако - краски.
на втором месте обработка фосфорной кислотой для создания фосфатной пленки.
Электролиз nacl, железка на катоде, понял, спасибо за пояснение, значит нужен лак, а если не сложно, из-за каких свойств железо после электролиза так бурно реагирует?
-
После электролиза железка покрылась ржавчиной.
Провел электролиз, очистил, помыл, высушили, достал, вроде чистая, прошло несколько часов, на железке появился ржавый налёт, не везде, но виден.
Что случилось, как это починить?
-
В 28.05.2023 в 14:16, Аль де Баран сказал:
Не, железка была на катоде, это больше не ржа какая то, а смолянистая жидкость которая прилипла к железке
-
В 28.05.2023 в 12:27, yatcheh сказал:
Я бы это назвал переацилированием, как частным случаем переэтерификации.
Всё-таки корнем слова "ацидолиз" является "лиз" - по-гречески что-то связанное с разделением.
Вы слишком много значения придаёте некоторым терминам, которые того вовсе не заслуживают. Если вас тянет ко всяким "научным" словам - называйте реакцию эфира с HI ацидолизом, хотя не замороченный химик скажет просто "расщепление"

Я даже не ожидал что небольшая шутка-поправка приведёт к такому...
-
В 28.05.2023 в 10:56, Аль де Баран сказал:
Ацидолиз сложных эфиров - это обменная реакция. Формально она аналогична вытеснению слабой кислоты из её соли более сильной кислотой: был один сложный эфир и кислота, стал другой сложный эфир и другая кислота. Структура соединений не нарушается, все они остаются при своих функциях. А у простых эфиров с иодоводородной кислотой происходит не обмен, а расщепление молекулы (реакция Цейзеля). Структура молекулы рушится, получаются соединения из других классов. Реагентов, способных расщепить сложный эфир - раз, два и обчёлся. Хотя реакцию Цейзеля тоже называют ацидолизом, но по существу это разные процессы.
Т.е ацидолиз-это взаимодействие сложного эфира с hi, а реакция Цейзеля-это взаимодействие простого эфира с hi?
У меня имелась информация с этого источника https://spravochnick.ru/himiya/spirty_prostye_efiry_tioly_i_sulfidy/vosstanovlenie_slozhnyh_efirov_i_karbonovyh_kislot_do_pervichnyh_spirtov/ , меня обманули?
-
Провел электролиз nacl для очистки металла от ржавчины, закончил, достаю железку, чищу её, а на ней как мазута такая то, я предполагаю, что это na[fe(OH)4].
1)Мои предложения верны?
2)Как от неё можно избавиться помимо использования каких либо кислот (Кислот вообще нет)?
-
В 27.05.2023 в 19:03, yatcheh сказал:
Так это не гидролиз. Это йодоводородолиз. Хм... какое слово богатое!
Химики, занимающийся этим на практике - йодоводородолизоводы. Химики, занимающихся теоретическими основами этого процесса - йодоводородолизоведы. Кандидаты технических наук, занимающиеся научным обоснование практического применения этого процесса - йодоводородолизоводоведы.
Я понимаю что это шутка, но на всякий, такая реакция называется-ацидолизу если мне память не изменяет
-
В 27.05.2023 в 01:51, Аль де Баран сказал:
Да ладно! Это чож такое получается? Выходит, мне в вузе подсунули неправильные учебники?
В них было написано, что простые эфиры щепаются иодоводородкой.
Незнаю, незнаю, ладно, былого не вернёшь назад
-
В 26.05.2023 в 21:12, Paul_S сказал:
Учебники лучше читай, брателло!

Ну... Может быть, проблема моя в том, что сильно углубился в вуз литературу, а там простые эфиры не сильно отличаются от сложных, ну чтож буду знать теперь
-
В 26.05.2023 в 20:20, Paul_S сказал:
в школьном курсе никакие простые эфиры не гидролиза, брателло

Жаль что такую информацию я узнал уже после егэ
-
В 26.05.2023 в 19:17, yatcheh сказал:
Как правило, но не все. Например, алкил-третбутиловые, или алкилбензиловые эфиры относительно нестойки в кислой среде.
Понял, принял, благодаоствую





Седина с помощью гидроперита
в Органическая химия
Опубликовано
А при чем тут гидроперит?