-
Постов
1016 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные Roman7474
-
-
12FeSO4+3O2--->4Fe2(SO4)3+2Fe2O3 какая температура нужна для этой реакции? В википедии понапишут...
-
Дело в том,что после растворения Fe2O3 остается лишняя кислота HCl в растворе.Ее жалко терять.Если я добавлю железо,а затем совместный гидролиз паром FeCl2, FeCl3 так можно?Причем хлориды прежде нужно высушить до образования кристаллов?
-
Fe2O3 + HCl ---> FeCl3 + H2O а как влево сместить реакцию?
-
Вы же говорили о 600°С, тогда 4FeCl3 + 3O2 = 2Fe2O3 + 3Cl2
Без доступа воздуха.
-
Вода, я ее просто не упомянул в продуктах, думал и так понятно, что воды улетит первой.
Это тогда разложение оксихлорида
-
А водород куда пропадает?Пока осадок не выпадет
Вероятно на Fe2O3 + Cl2
-
Возможно, если сместить равновесие добавкой, например, амимака
А много его добавлять?
На что разлагаются и разлагаются ли вообще Fe(OH)Cl2 и Fe(OH)2Cl при нагревании 600 С ?
-
В лучшем случае может дойти до азеотропа
Это понятно.Мне бы знать точно какой концентрации она получается.
-
А что за проект?Реактивы бесплатно раздают)))
-
Получится, но это отход, так сказать, производства.
Отходы производства никому не нужны.
Если смешать электролит плотностью 1.28 с избытком поваренной соли,затем все это перегнать с холодильником какой концентрации получится соляная кислота?Она будет без примесей?
-
А возможно ли гидролизом FeCl3 получить чистый Fe2O3 без примесей оксихлоридов например?Для этого поднять температуру?Обычно основные соли плохо растворимы, так что в этом случае, думаю, нет.
Более того, я думаю, что для железа подобные соединения вообще существуют, т.к. скорее всего гидролиз сразу идет до гидроокиси, вернее до Fe2O3*nH2O или до каких-то гидратированных оксихлоридов.
-
А Fe(OH)Cl2 и Fe(OH)2Cl растворимы в воде?
-
А если пар будет нагрет до 200 C и постепенно паоступать к FeCl3 гидролиз до конца пойдет?Как уже писали, смотря какой оксид. В лучшем случае это будет приблизительно так
Fe2O3 + 4FeCl3 + 3H2O = 6Fe(OH)Cl2
Fe2O3 + FeCl3 + 3H2O = 3Fe(OH)2Cl
-
Ну а разве NaCl + NH4HSO4 не сульфат натрия получится?А он то здесь причем?
Аммак покупать надо, с тем же успехом можно покупать и сульфат аммония - удобрение.
Аммиак покупать не надо,он летит при нагреве сульфата аммония.
-
Fe2O3+FeCl3+H2O + температура 100 C .Достаточно ли будет кислотности в результате гидролиза FeCl3 чтобы HCl прореагировала с Fe2O3 ? Хотел измельчить Fe2O3 таким способом.
-
надо просто попробовать реакцию с гидросульфатом аммония и NaCl, я думаю, реакция пойдет, можно поробовать добавить несколько капель серной кислоты (хоть разведеной), что бы увеличить контактное поле.
Сульфат натрия еще прочнее.Здесь смысал то в чем,чтобы можно было так сказать гонять по кругу вещества.Например осадил аммиаком какой-нибудь хлорид,а хлорид аммония снова до кислоты,кислота с оксидом и т.д.
-
Хлорид аммония к 300°С возгоняться начинает.
Ну,а как он возгоняется...Разделяется на NH3 и HCl. NH3 реагирует с гидросульфатом, HCl улетает.
-
Может гидросульфат будет как-то реагировать с NH4Cl ?
-
Шел бы диоксид азота из глушаков, здания все к херам потаяли бы от кислотных дождей.
Он там есть,но его не много.
-
Не понятно где пишут при 600 С каолинит переходит в свободные оксиды,где при 800 С. Какая температура на самом деле?
-
В глине есть легкоплавкие и тугоплавкие компоненты. При обжиге,легкоплавкие плавятся,и скрепляют тугоплавкий "наполнитель" в "монолит"
А как разрушить соединение Al2O3·2SiO2·2H2O на отдельные оксиды?
-
Почему при обжиге глина становится твердой? Al2O3·2SiO2·2H2O -что дают эти связи между молекулами?Ведь если взять по отдельности Al2O3 и SiO2 ,смешать и обжечь оно просто рассыпется.
-
Физически?Это как?Это же не масло с водой где само все разделяется.А щелочью окись алюминия надо растворять?А кто его знает, я не специалист по обогащению и флотации. Вы спросили
Я вам рассказал про один из процессов который реально применяется. Есть еще магнитная сепарация в сильном магнитном поле, есть электростатическая сепарация и т.д.
Вам же проще всего химически разделить щелочью (если не албфа-окись алюминия) или физически, по удельному весу, учитывая, что плотность гематита 5,25, а корунда 4, а если у вам гамма-окись, то даже меньше.
-


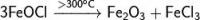
Оксиды железа
в Неорганическая химия
Опубликовано
Может при 300 C ? Он не должен разлагатся при этой температуре.